Содержание
- 2. 1891 год Ирландский физик Стони вел понятие ЭЛЕКТРОН (по-гречески «янтарь») – частица, которая переносит электричество. Английский
- 3. 1897 год ДЖ. Томсон предложил модель атома – «Пудинг с изюмом» электрон +
- 4. 1911 год Английский ученый Эрнест Резерфорд обосновал ядерную модель атома + ядро электронная оболочка -
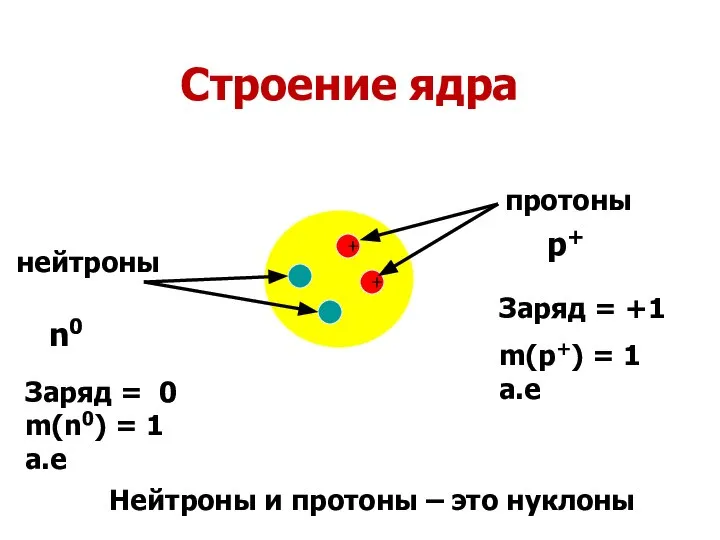
- 5. + + Строение ядра протоны нейтроны n0 p+ Заряд = +1 m(p+) = 1 a.e Заряд
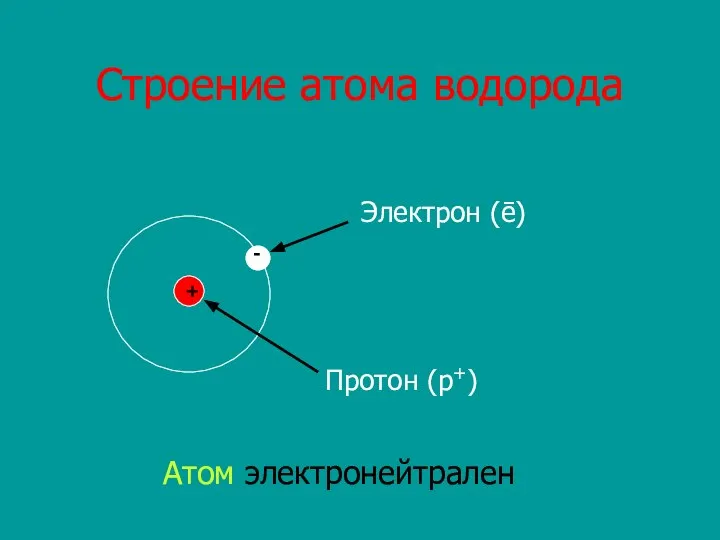
- 6. Строение атома водорода + - Протон (p+) Электрон (ē) Атом электронейтрален
- 7. Число протонов = заряду атомного ядра числу электронов = порядковому номеру элемента Mg 12 Заряд ядра
- 8. Масса атома – это масса его ядра. Число протонов + число нейтронов = массовое число (А)
- 9. Задание Укажите состав атома натрия Na 11 23 p+ = 11 ē = 11 n0 =
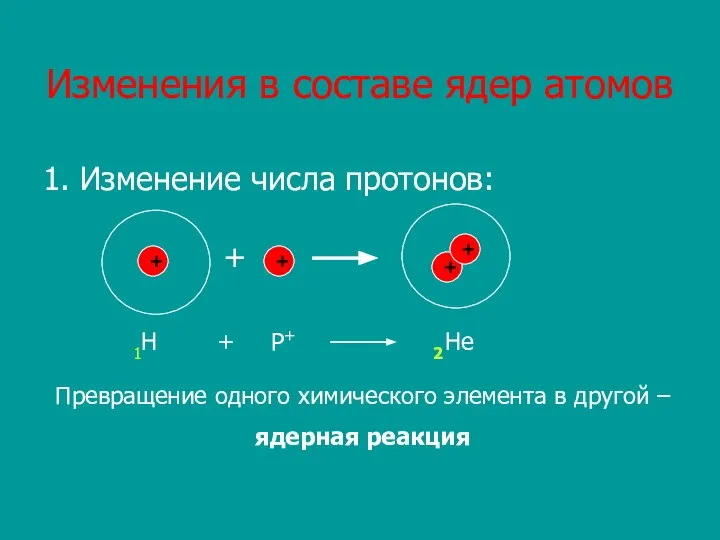
- 10. Изменения в составе ядер атомов 1. Изменение числа протонов: + + + + + 1Н Р+
- 11. Химический элемент – это вид атомов с одинаковым зарядом ядра (с одинаковым числом протонов в ядре)
- 12. 2. Изменение числа нейтронов в ядре: + 1Н + + + + 1 + n0 1Н
- 13. Изотопы водорода
- 14. 17 Сl 35 17 Сl 37 75% 25% Ar = 0.75 * 35 + 0.25 *
- 16. Скачать презентацию










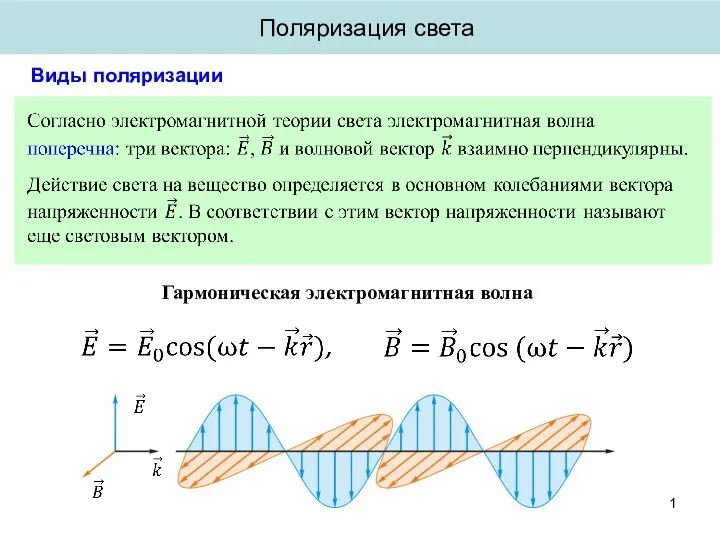 Поляризация света. Виды поляризации
Поляризация света. Виды поляризации Уравнения теории упругости. Напряженное состояние в точке. Гипотеза Сен-Венана. (Лекции 1-2)
Уравнения теории упругости. Напряженное состояние в точке. Гипотеза Сен-Венана. (Лекции 1-2) ОГЭ по физике 2018
ОГЭ по физике 2018 Физика конденсированного состояния
Физика конденсированного состояния Сила тяжести. Вес, невесомость, перегрузки
Сила тяжести. Вес, невесомость, перегрузки Newton’s Laws of Motion
Newton’s Laws of Motion Состав и характеристика атомного ядра
Состав и характеристика атомного ядра Импульс материальной точки
Импульс материальной точки Презентация Электрическое сопротивление человека
Презентация Электрическое сопротивление человека Термиялық өңдеу. Термиялық өңдеудің түрлері. Термиялық өңдеудің фазалық өзгерістері. Болаттын термиялық өңдеу
Термиялық өңдеу. Термиялық өңдеудің түрлері. Термиялық өңдеудің фазалық өзгерістері. Болаттын термиялық өңдеу Проводники и электростатическое поле
Проводники и электростатическое поле Явление электромагнитной индукции. Уравнения Максвелла
Явление электромагнитной индукции. Уравнения Максвелла Система уравнений Максвелла. Основные уравнения электродинамики
Система уравнений Максвелла. Основные уравнения электродинамики Pārejas procesi maiņstrāvas piedziņā
Pārejas procesi maiņstrāvas piedziņā Закон всемирного тяготения
Закон всемирного тяготения Презентация по физике "Історія вивчення атома." - скачать бесплатно
Презентация по физике "Історія вивчення атома." - скачать бесплатно Тема урока Элементарные частицы
Тема урока Элементарные частицы Презентация по физике Применение аккумуляторов
Презентация по физике Применение аккумуляторов Линза. Построение изображения в линзе. Формула тонкой линзы
Линза. Построение изображения в линзе. Формула тонкой линзы Реальные газы и пары. Общие свойства реальных газов
Реальные газы и пары. Общие свойства реальных газов Отклонения формы и расположения поверхностей
Отклонения формы и расположения поверхностей История создания швейной машинки
История создания швейной машинки Петрофизика. Физико-механические свойства горных пород
Петрофизика. Физико-механические свойства горных пород Взаимное притяжение и отталкивание молекул
Взаимное притяжение и отталкивание молекул Наблюдения - основа астрономии
Наблюдения - основа астрономии Распределение молекул по величине энергии
Распределение молекул по величине энергии Презентация по физике Термодинамика
Презентация по физике Термодинамика  Анималистика в металлопластике
Анималистика в металлопластике