Содержание
- 2. Химия Строение атома Химическая связь Строение твердого тела Химическая термодинамика Химическая кинетика Равновесие в химических системах
- 3. I. Строение атома 3 этапа развития учения о строении атома 1 – Натурфилософские представления об атомном
- 4. Строение атома. Физические модели строения атома Эрнест Резерфорд - Планетарная модель атома (1911 г.) Эрвин Шредингер
- 5. Корпускулярно-волновой дуализм свойств материи [проблема природы лучистой энергии - эл.магн.излучения(ЭМИ)] Электромагнитное излучение Волна: λ - длина
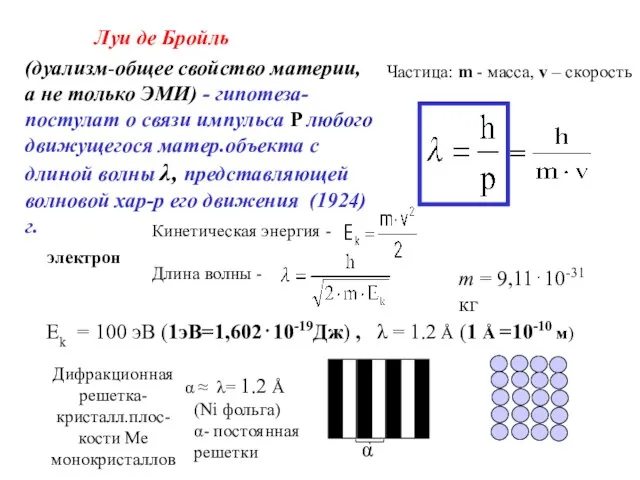
- 6. (дуализм-общее свойство материи, а не только ЭМИ) - гипотеза-постулат о связи импульса P любого движущегося матер.объекта
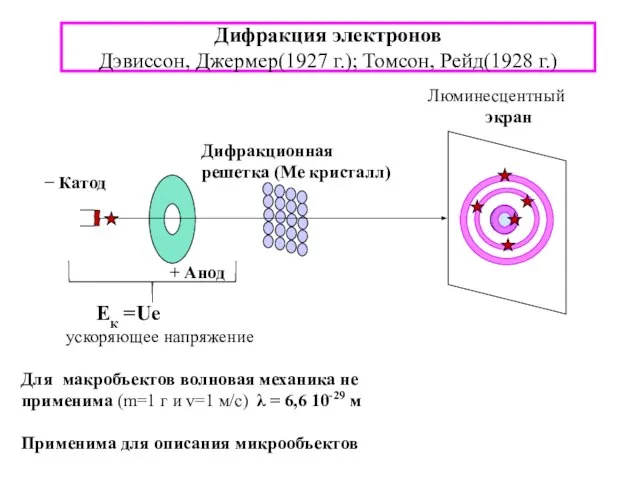
- 7. Дифракция электронов Дэвиссон, Джермер(1927 г.); Томсон, Рейд(1928 г.)
- 8. Принцип неопределенности [для микрочастиц(электрона)] Вернер Гейзенберг постулировал этот принцип в 1927 г. 0 ≤ Р ≤
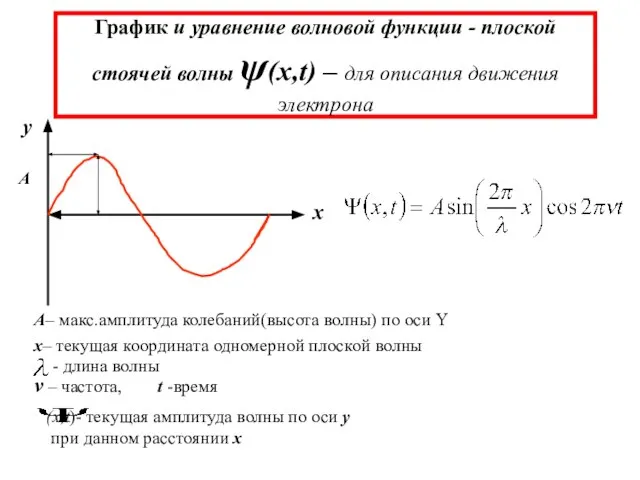
- 9. График и уравнение волновой функции - плоской стоячей волны ψ(x,t) – для описания движения электрона
- 10. Уравнение Шредингера 1. Уравнение отображает волновой характер движения электрона в пространстве с координатами (x,y,z) Ψ(x,y,z,t) -
- 11. λ → m, Ek E = Ek + V E - полная энергия V- потенциальная энергия
- 12. Физический смысл волновой функции Ψ(x,y,z) - пси функция - волновая функция Макс Борн, 1926 г. волновая
- 13. Электрон в одномерном потенциальном ящике(яме). Решение ур. Шредингера. Потенциальная яма (ящик) - область пространства, вне которой
- 14. Нахождение волновой функции состояния электрона в потенц.ящике Решение в явном виде - набор волн.функций Ψ(х), где
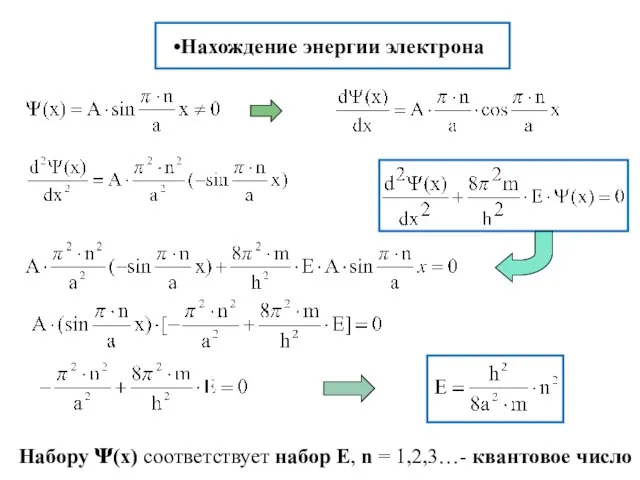
- 15. Нахождение энергии электрона Набору ᴪ(x) соответствует набор Е, n = 1,2,3…- квантовое число
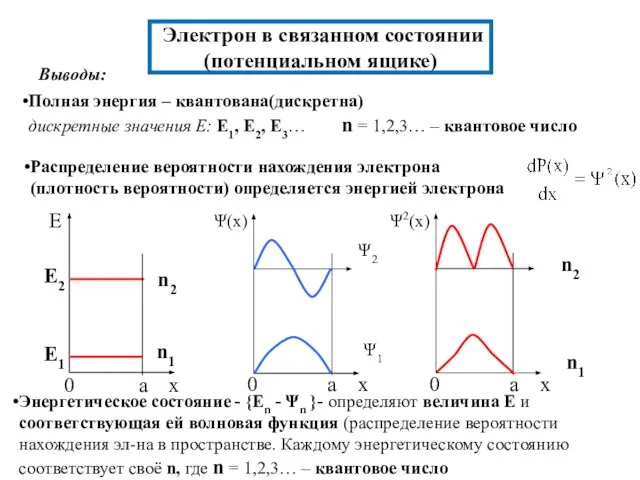
- 16. Электрон в связанном состоянии (потенциальном ящике) Выводы: Полная энергия – квантована(дискретна) дискретные значения Е: E1, E2,
- 17. Электрон в трехмерном потенциальном ящике Решение: a,b,c – параметры ящика nx, ny, nz – квантовые числа
- 18. Вырожденные энергетические состояния одно значение энергии – несколько наборов квантовых чисел - несколько волновых функций а
- 19. Квантово-механическая модель атома. Основное состояние атома водорода [k=1/4πε0] - константа в з-не Кулона x = r⋅sinϑ⋅cosϕ
- 20. Решение уравнения Шредингера для основного состояния атома водорода
- 21. Решение системы
- 22. Радиальное распределение электронной плотности. Понятие электронной орбитали 1.41 Å dV = 4πr2dr Объём сферич.слоя тощиной dr
- 23. Атом водорода в основном состоянии
- 24. Возбужденные состояния атома водорода Общий вид волновой функции - Ψ(r,θ,ϕ). Используя метод разделения переменных Ψ(r,θ,ϕ) представляют
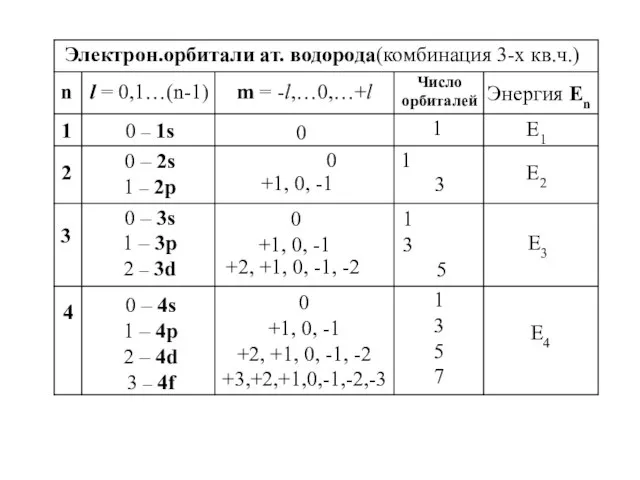
- 25. Квантовые числа главное : n = 1,2,3,4…∞ Определяет разрешенные (квантованные, дискретные) значения полной энергии электрона, размер
- 26. n l = 0,1…(n-1) m = -l,…0,…+l Число орбиталей Энергия Еn 1 E2 2 1 0
- 27. Энергетическая диаграмма орбиталей в атоме водорода n=1 E1s
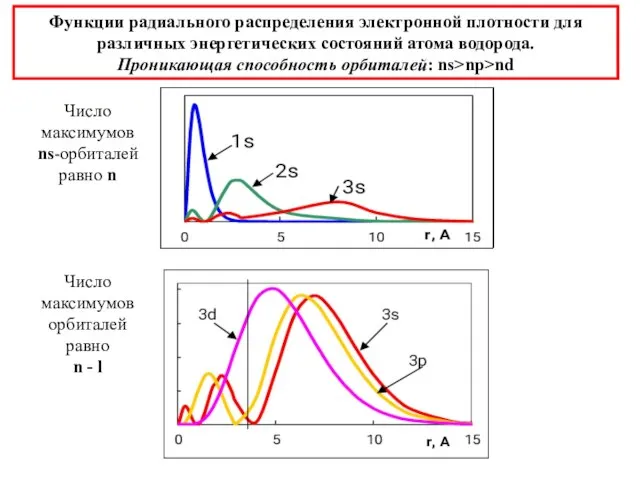
- 28. Функции радиального распределения электронной плотности для различных энергетических состояний атома водорода. Проникающая способность орбиталей: ns>np>nd Число
- 29. 1.7 Многоэлектронный атом (одноэлектронное приближение - водородоподобная система) Zэ = Z - σn,l Z – заряд
- 30. Зависимость энергии орбиталей Е от Z (заряда ядра) и от различия радиального распределения электронной плотности s,p
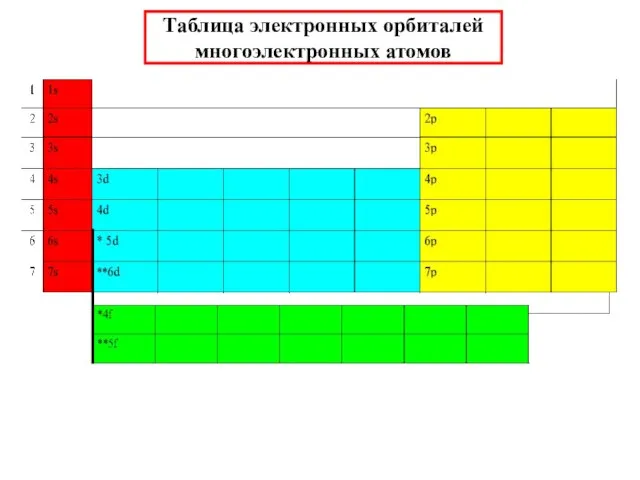
- 31. Таблица электронных орбиталей многоэлектронных атомов
- 32. Электронные конфигурации многоэлектронных атомов. Правила заселения электронами орбиталей 1. Принцип минимума энергии электронов. 2. Принцип (запрет)
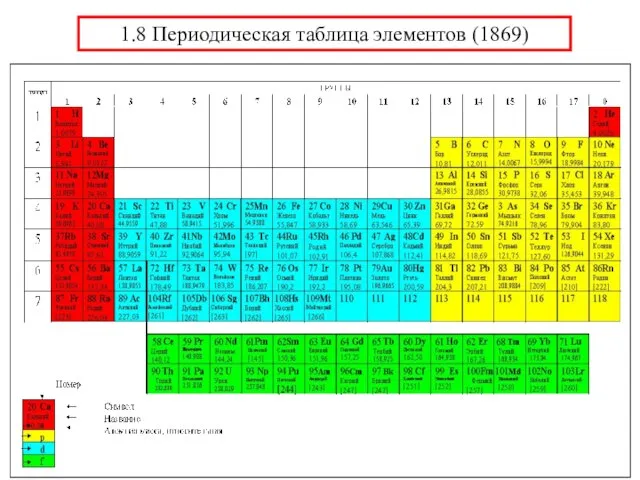
- 33. 1.8 Периодическая таблица элементов (1869)
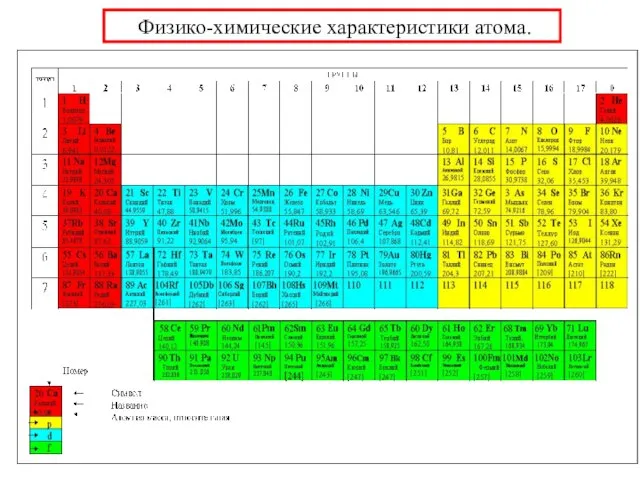
- 34. Физико-химические характеристики атома. Радиус атома и иона
- 35. Ковалентный радиус ( RA = rсв /2) и радиус иона
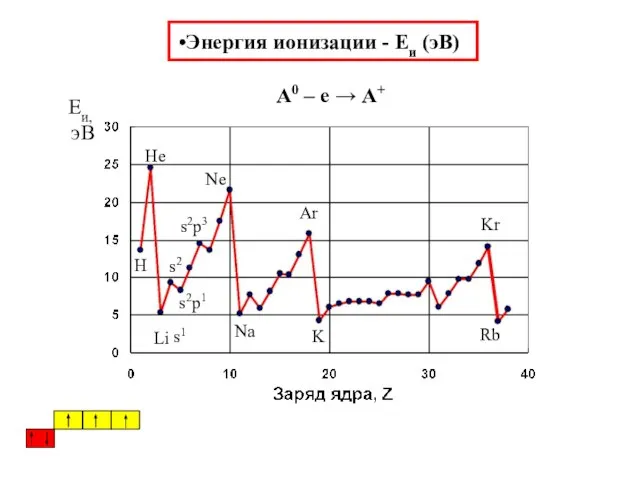
- 36. Энергия ионизации - Eи (эВ) А0 – е → А+ s1 s2 s2p1 s2p3
- 37. Энергия сродства к электрону – Е СЭ (эВ) A0 + e → A–
- 39. Скачать презентацию



![Корпускулярно-волновой дуализм свойств материи [проблема природы лучистой энергии - эл.магн.излучения(ЭМИ)] Электромагнитное](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/528578/slide-4.jpg)
![Принцип неопределенности [для микрочастиц(электрона)] Вернер Гейзенберг постулировал этот принцип в 1927](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/528578/slide-7.jpg)







![Квантово-механическая модель атома. Основное состояние атома водорода [k=1/4πε0] - константа в](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/528578/slide-18.jpg)












 Сила Лоренца
Сила Лоренца Электростатика
Электростатика Дифракционная решетка
Дифракционная решетка Движение с постоянным ускорением
Движение с постоянным ускорением Анализ и перспективы развития элегазового и вакуумного оборудования подстанций энергосистемы
Анализ и перспективы развития элегазового и вакуумного оборудования подстанций энергосистемы Заточка дереворежущих инструментов
Заточка дереворежущих инструментов Вертолет Ми-8МТВ. Топливная система
Вертолет Ми-8МТВ. Топливная система Основные положения МКТ (молекулярная физика)
Основные положения МКТ (молекулярная физика) Линии влияния. Лекция 2. Расчёт сооружений на действие подвижных и других временных нагрузок
Линии влияния. Лекция 2. Расчёт сооружений на действие подвижных и других временных нагрузок Судовые газотурбинные установки
Судовые газотурбинные установки История создания. Принцип работы. КПД. Влияние на экологию.
История создания. Принцип работы. КПД. Влияние на экологию. Физические основы гемодинамики. (Лекция 4)
Физические основы гемодинамики. (Лекция 4) Равновесное состояние кристаллической решетки. Фононы. (Лекция 5)
Равновесное состояние кристаллической решетки. Фононы. (Лекция 5) Магнитооптика ферромагнитных металлов
Магнитооптика ферромагнитных металлов Презентация по физике "Какие электроприборы есть на кухне?" - скачать бесплатно
Презентация по физике "Какие электроприборы есть на кухне?" - скачать бесплатно Лінійні кола
Лінійні кола Молекулярная спектроскопия. Энергетические уровни
Молекулярная спектроскопия. Энергетические уровни Дисперстік жүйелердің оптикалық қасиеттері
Дисперстік жүйелердің оптикалық қасиеттері Траншейный многоковшовый экскаватор
Траншейный многоковшовый экскаватор Условия равновесия тел. Момент силы. Виды равновесия
Условия равновесия тел. Момент силы. Виды равновесия Гидродинамика Солнца. (Лекция 6)
Гидродинамика Солнца. (Лекция 6) Ультразвуковой дальномер HC-SR04
Ультразвуковой дальномер HC-SR04 Реле контроля земли
Реле контроля земли Равноускоренное движение
Равноускоренное движение Методы измерения газопроницаемости
Методы измерения газопроницаемости Основные положения молекулярно-кинетической теории. Взаимодействие молекул и агрегатные состояние. Законы термодинамики
Основные положения молекулярно-кинетической теории. Взаимодействие молекул и агрегатные состояние. Законы термодинамики Модели расчета биполярных транзисторов VBIC, HICUM, MEXTRAM
Модели расчета биполярных транзисторов VBIC, HICUM, MEXTRAM Электричесие явления (10 класс)
Электричесие явления (10 класс)