Содержание
- 2. Простейшей моделью молекулярно-кинетической теории является модель идеального газа. Задача молекулярно-кинетической теории состоит в том, чтобы установить
- 3. Макроскопические параметры – величины, характеризующие состояние макроскопических тел без учета молекулярного строения тел. V, p, t
- 4. Температура характеризует степень нагретости тела (холодное, теплое, горячее).
- 5. Любое макроскопическое тело или система макроскопических тел при неизменных внешних условиях самопроизвольно переходит в состояние теплового
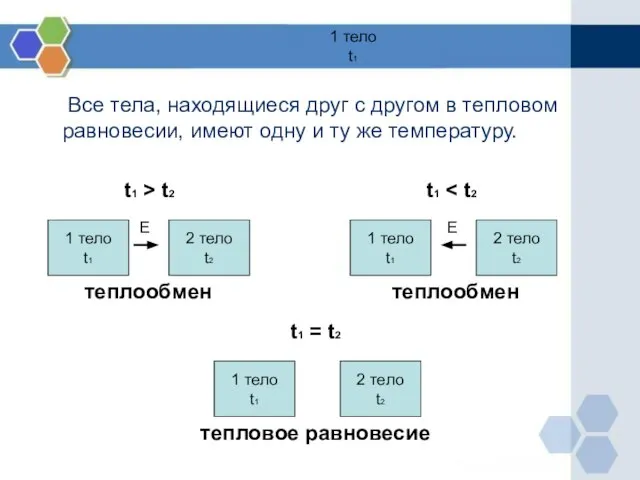
- 6. 1 тело t1 Все тела, находящиеся друг с другом в тепловом равновесии, имеют одну и ту
- 7. Для измерения температуры был создан термометр. В 1597 г. Галилео Галилей придумал первый прибор для наблюдений
- 8. В 1714 г. голландский учёный Д. Фаренгейт изготовил ртутный термометр. В 1730 г. французский физик Р.
- 9. Любопытно, что …на самом деле шведский астроном и физик Цельсий предложил шкалу, в которой точка кипения
- 10. 10 минут! с. 172 - 174 учебника Прочитать и выполнить краткий конспект с выводом формул. Записать
- 11. Абсолютный нуль температуры – предельная температура, при которой давление газа обращается в нуль при V –
- 12. Абсолютная шкала температур – шкала Кельвина. Т – термодинамическая температура. [Т] = К (кельвин)
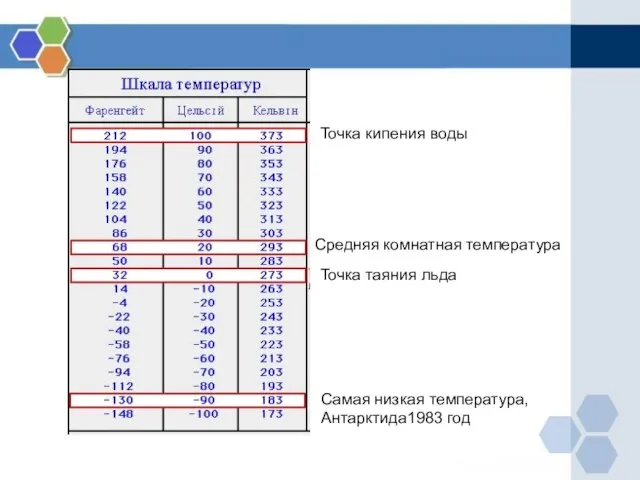
- 13. Самая низкая температура, Антарктида1983 год Точка кипения воды Средняя комнатная температура Точка таяния льда
- 14. Постоянная Больцмана Постоянная Больцмана связывает температуру Q в энергетических единицах с температурой Т в кельвинах. k
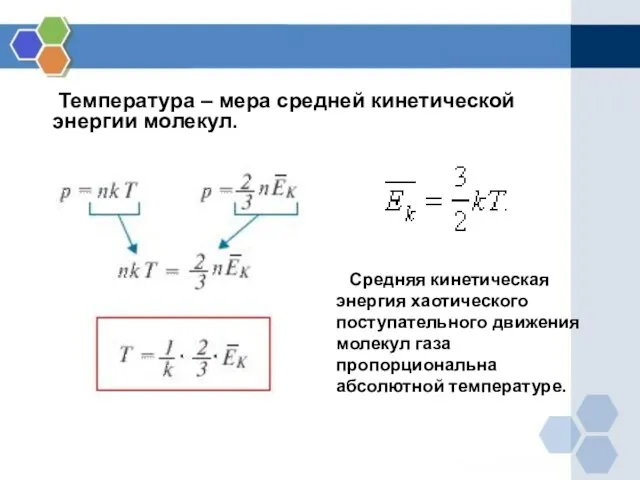
- 15. Температура – мера средней кинетической энергии молекул. Средняя кинетическая энергия хаотического поступательного движения молекул газа пропорциональна
- 16. Зависимость давления газа от концентрации его молекул и температуры.
- 18. Скачать презентацию









![Абсолютная шкала температур – шкала Кельвина. Т – термодинамическая температура. [Т] = К (кельвин)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1204666/slide-11.jpg)


 Гидравлика машин
Гидравлика машин Световые явления
Световые явления Давление твердых тел, жидкостей и газов
Давление твердых тел, жидкостей и газов Постулаты теории относительности
Постулаты теории относительности Вес тела и сила тяжести
Вес тела и сила тяжести Индукционные нагреватели. Перспективы и области применения
Индукционные нагреватели. Перспективы и области применения Теоретическая (техническая) механика. Статика
Теоретическая (техническая) механика. Статика Характеристики движения
Характеристики движения Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц
Коллоидные растворы. Молекулярно-кинетические и оптические свойства. Строение коллоидных частиц Плоская система сил
Плоская система сил Магнитные подшипники
Магнитные подшипники Аморфні та склоподібні матеріали. (Лекція 2)
Аморфні та склоподібні матеріали. (Лекція 2) Реальные газы, жидкости и твердые тела
Реальные газы, жидкости и твердые тела Давление. Единицы давления
Давление. Единицы давления Закон всемирного тяготения
Закон всемирного тяготения Интеллектуальная игра «Физбой»
Интеллектуальная игра «Физбой» Тепловозы. Устройство тепловоза
Тепловозы. Устройство тепловоза Кристаллические тела (10 класс)
Кристаллические тела (10 класс) Квантовые методы в медицине. Ядерный магнитный резонанс. Электронный парамагнитный резонанс. (Лекция 14)
Квантовые методы в медицине. Ядерный магнитный резонанс. Электронный парамагнитный резонанс. (Лекция 14) Теоретическая механика как наука и ее место среди естественных наук
Теоретическая механика как наука и ее место среди естественных наук Сила упругости. Закон Гука
Сила упругости. Закон Гука Електричний струм у газах
Електричний струм у газах  Подготовила учитель физики МОУ СОШ №1 р.п. Степное Бейбулатова Е.А.
Подготовила учитель физики МОУ СОШ №1 р.п. Степное Бейбулатова Е.А. Механика. Наука о движении тел
Механика. Наука о движении тел Энергия движущейся воды и ветра
Энергия движущейся воды и ветра Работа силы тяжести
Работа силы тяжести Оценка угла места в системах локации метрового диапазона
Оценка угла места в системах локации метрового диапазона «Интерференция света»
«Интерференция света»