Содержание
- 2. Термодинамика – раздел физики, представляет собой науку о превращениях различных видов энергии друг в друга. Общая
- 3. Техническая термодинамика Изучает закономерности взаимного превращения теплоты и работы, происходящие в макроскопических системах; Изучает свойства тел,
- 4. Теплота и работа Теплота и работа представляют две формы передачи энергии от одного тела к другому:
- 5. Рабочее тело В процессах превращения тепла в механическую работу всегда участвует некоторое промежуточное вещество (например, продукты
- 6. Состояния рабочего тела Стационарное – не изменяется во времени. Равновесное – одноименные интенсивные макропараметры имеют одно
- 7. Термодинамическая система (ТДС) Совокупность рабочих тел, обменивающихся энергией и веществом между собой и окружающей средой, –
- 8. Классификация ТДС Изолированные (замкнутые) – отсутствует обмен веществом и энергией с окружающей средой; Термодинамически изолированные –
- 9. Классификация ТДС Закрытые – отсутствует обмен веществом с внешней средой. Рабочее тело не пересекает границу системы
- 10. Основные термодинамические параметры При взаимодействии с окружающей средой рабочее тело переходит из одного состояния в другое.
- 11. Интенсивные – не зависят от количества вещества в системе; Удельные – отнесенные к единице количества вещества
- 12. Термодинамические параметры Макроскопические физические величины, характеризующие систему в состоянии равновесия, - термодинамические параметры состояния системы. T,
- 13. Основные параметры Абсолютное давление – Рабс, Па; давление, отсчитываемое от абсолютного нуля давления (абсолютного вакуума). Paбс=Ратм+Ризб,
- 14. Основные параметры Абсолютная температура – T, K; Т К=273,15+t°С. Удельный объем – ν = V/M, м3/кг.
- 15. Температура – это мера средней кинетической энергии молекул. Чем выше движение молекул, тем выше температура тела.
- 16. Термическое уравнение состояния рабочего тела Характеризует термодинамическое состояние вещества, находящегося в состоянии равновесия (во всей массе
- 17. Термодинамические процессы Равновесный – рабочее тело проходит непрерывный ряд равновесных состояний. Обратимый – процесс, допускающий возвращение
- 18. Теплоемкость Теплоемкость с - количество теплоты, необходимой для изменения на 1 градус единичной массы рабочего тела
- 20. Теплоемкость смеси газов Тогда соответственно массовая, объемная и мольная теплоемкости смеси: ; ; . Два последних
- 21. Теплоемкость газов зависит от протекания процесса: изохорная -массовая изохорная теплоемкость - объемная изохорная теплоемкость - мольная
- 22. Внутренняя энергия Совокупность всех видов энергии тела или системы в данном состоянии, не связанных с движением
- 23. Внутренняя энергия Идеальные газы – энергия взаимодействия равна нулю, энергия их теплового движения зависит от температуры:
- 24. Энтальпия Тепловая функция: Удельная энтальпия: где u – внутренняя энергия газа; pv – потенциальная энергия давления
- 25. Энтропия Энтропия – параметр, изменяющийся от количества переданной теплоты. При обмене энергией в форме теплоты: обобщенная
- 26. Тепловая теорема Нернста (ТРЕТИЙ ЗАКОН ТЕРМОДИНАМИКИ) При температуре, стремящейся к абсолютному нулю, энтропия вещества, находящегося в
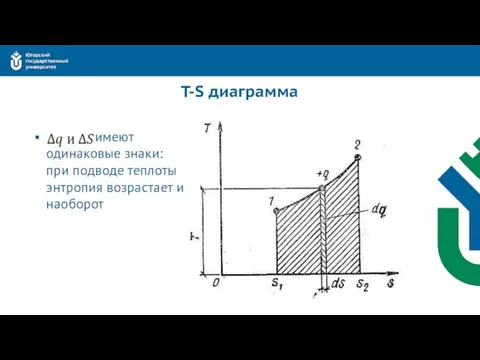
- 27. T-S диаграмма имеют одинаковые знаки: при подводе теплоты энтропия возрастает и наоборот
- 28. Идеальный и реальный газ Идеальный газ – отсутствуют силы сцепления между молекулами, молекулы материальные точки, не
- 29. Идеальный газ PV=RT - уравнение Клайперона где R - газовая постоянная, которая зависит от природы газа,
- 30. Термическое уравнение состояния идеальных газов где – газовая постоянная, Дж/(кг ·К); - универсальна газовая постоянная, 8314
- 31. Законы идеальных газов Закон Дальтона – давление смеси газов равно сумме парциальных давлений компонентов смеси: pi
- 32. Состав смеси, концентрации Мольная доля: Относительная мольная доля: Массовая доля: Относительная массовая доля:
- 33. Концентрации Объемная (мольная) доля: ri = Vi/V Vi - парциальный (приведенный) объем каждого газа V -
- 34. Реальные газы Для реальных газов необходимо учитывать взаимодействие между молекулами, т.к. обычно это достаточно плотные газы.
- 35. Реальные газы 2 способ. Уравнения с вириальными коэффициентами. А,В,С - вириальные коэффициенты. Уравнение считается наиболее точным
- 36. Уравнение состояния реальных газов 3 способ. Уравнение Ван-Дер-Ваальса Межмолекулярные силы отталкивания позволяют молекулам сближаться до некоторого
- 37. Уравнение состояния реальных газов Сила притяжения по направлению совпадает с внешним давлением и приводит к возникновению
- 39. Скачать презентацию

































 ОПТИКА Подготовка к ЕГЭ Учитель: Попова И.А. МОУ СОШ № 30 Белово 2010
ОПТИКА Подготовка к ЕГЭ Учитель: Попова И.А. МОУ СОШ № 30 Белово 2010 Второе начало термодинамики. Энтропия
Второе начало термодинамики. Энтропия Структурная схема объекта. (Лекция 5)
Структурная схема объекта. (Лекция 5) Строение атома. Опыты Резерфорда
Строение атома. Опыты Резерфорда Карбюраторные двигатели
Карбюраторные двигатели Аналитические методы в геохимии
Аналитические методы в геохимии Рівноприскорений рух прискорення
Рівноприскорений рух прискорення Диэлектрические потери и диэлектрическая спектроскопия
Диэлектрические потери и диэлектрическая спектроскопия Проводники в электрическом поле
Проводники в электрическом поле Измерение вершинных отрезков и рабочих расстояний
Измерение вершинных отрезков и рабочих расстояний Метод заряженного тела
Метод заряженного тела Понятие об энтропии
Понятие об энтропии Баллистическое движение
Баллистическое движение Изучение механизмов и их работа Тема: Повторение тем
Изучение механизмов и их работа Тема: Повторение тем Reassessment of nuclear power safety
Reassessment of nuclear power safety Ток и заряд в магнитном поле
Ток и заряд в магнитном поле Виды теплопередачи
Виды теплопередачи Момент сил. Сборка: Гусеница. Занятие №14
Момент сил. Сборка: Гусеница. Занятие №14 Энергетические машины и установки
Энергетические машины и установки Аттестационная работа. Образовательная программа внеурочной деятельности по физике и географии
Аттестационная работа. Образовательная программа внеурочной деятельности по физике и географии Установки для получения низких температур
Установки для получения низких температур DOMESTIC HOT WATER CIRCUIT
DOMESTIC HOT WATER CIRCUIT Управління потоками реактивної енергії
Управління потоками реактивної енергії Коллективные свойства ядер
Коллективные свойства ядер Сверхпроводящие кабели
Сверхпроводящие кабели Плоская система сходящихся сил
Плоская система сходящихся сил Урок-повторение по теме: «КИНЕМАТИКА» Составила: Орлова Елена Анатольевна учитель физики МБОУ Лицея №11 г. Химки
Урок-повторение по теме: «КИНЕМАТИКА» Составила: Орлова Елена Анатольевна учитель физики МБОУ Лицея №11 г. Химки Презентация по физике "Измерение атмосферного давления 7 класс" - скачать
Презентация по физике "Измерение атмосферного давления 7 класс" - скачать