Содержание
- 2. ТОПЛИВО
- 3. Топливо –горючие вещества, основной составной частью которых является углерод, применяемые для получения при их сжигании тепловой
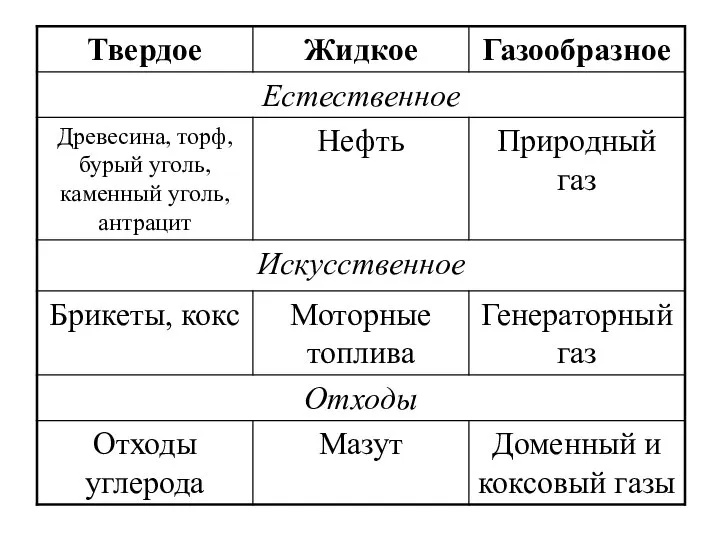
- 4. По физическому состоянию топливо подразделяют на твердое, жидкое и газообразное. Топливо, которое встречается в природных условиях
- 6. В состав топлива входят в виде сложных химических соединений, углерод С, Водород Н, кислород О, азот
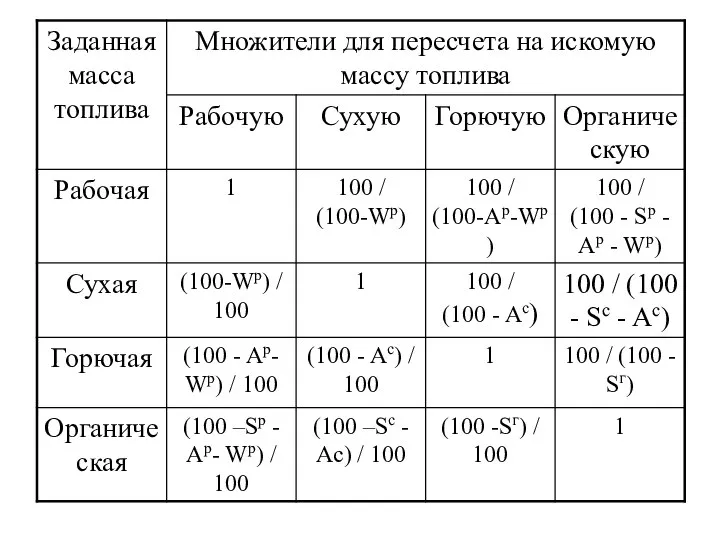
- 7. Элементарный состав топлива может быть задан рабочей, сухой или органической массами. Элементарный состав топлива задается в
- 8. сухая масса: Cс + Hс + Oс + Nс + Sс + Aс = 100 %.
- 9. При этом: Sp = Spл + Sрм – содержание в топливе серы, летучей серы и минеральной
- 11. Химический состав газообразного топлива задается в процентах по объему. Все расчеты, связанные с определением состава газообразного
- 12. Важнейшей составной частью топлива является углерод. При полном сгорании 1 кг углерода выделяется 34100 кДж тепла.
- 13. Кислород и азот относятся к негорючей массе топлива (к балласту). Сера содержится в топливе в виде
- 14. Негорючие минеральные примеси также являются балластом топлива. Твердый негорючий продукт полного окисления и разложения всех минеральных
- 15. Важным показателем качества топлива является выход летучих веществ и характеристика кокса. В состав летучих веществ, которые
- 16. Выход летучих веществ определяется в процентах к безводной и беззольной (горючей) массам топлива: Vг = Vа
- 17. ТЕПЛОТА СГОРАНИЯ ТОПЛИВА
- 18. Теплотой сгорания топлива называют количество тепла, которое выделяется при полном сгорании 1 кг твердого (жидкого) или
- 19. Различают высшую Qв и низшую Qн теплоту сгорания топлива. Теплота сгорания высшая больше, чем теплота сгорания
- 20. В практических расчетах пользуются теплотой сгорания низшей на рабочую массу топлива Qрв. Теплоту сгорания топлива приближенно
- 21. Для удобства расчетов и сравнения теплоты сгорания различных видов топлива пользуются понятием условное топливо. Теплота сгорания
- 22. Э = Qрн / 7000, если Qрн ккал/кг; Э = Qрн / 29,3, если Qрн МДж/кг;
- 23. Для смеси твердого или жидкого топлива с газообразным: Qрн см = Qр'н + k Qр''н. где
- 24. К древесному топливу относятся дрова и отходы деревообрабатывающих предприятий (опилки, обрезки, щепа и т.д.). Заготовку дров
- 25. Торф – продукт неполного разложения растений при недостатке воздуха и большой влажности. В зависимости от способа
- 26. Бурый уголь состоит из горючих веществ растительного происхождения и является следующей стадией обуглероживания за торфом. Бурые
- 27. Теплота сгорания каменных углей – 17,5 – 28,6 МДж/кг. Антрацит представляет собой наиболее обуглероженную разновидность каменного
- 28. Жидкое топливо получается главным образом путем переработки нефти. Из нефти получают керосин, бензин, смазочные масла и
- 29. Газообразное топливо представляет собой смесь различных газов. Природные газы содержат от 80 до 98 % метана.
- 30. ПРОЦЕССЫ ГОРЕНИЯ ТОПЛИВА
- 31. Горение топлива представляет собой химический процесс соединения горючих веществ топлива с кислородом воздуха, сопровождающийся интенсивным выделением
- 32. Процесс горения топлива условно можно разделить на две стадии: воспламенение и последующее горение. При нагревании топлива
- 33. Горение называется полным, если оно происходит при достаточном количестве окислителя и завершается полным окислением горючих элементов
- 34. РАСХОД ВОЗДУХА Теоретическое количество воздуха, необходимое для сгорания топлива, определяется по формулам горения составных элементов топлива.
- 35. Для 1 кг водорода требуется 8 кг кислорода: 4 кг Н2 + 32 О2 = 36
- 36. Так как, что массовая доля содержания кислорода в воздухе равна 0,232, то теоретически необходимое количество воздуха
- 37. Так как при нормальных условиях плотность воздуха равна 1,293 кг/м3, то объемный расход воздуха Vт для
- 38. где Ср, Нр, Sрл, Ор – элементарный состав топлива на рабочую массу, %. Для газообразного топлива
- 39. где СОт, Н2т и т.д. – содержание отдельных газов в газообразном топливе в процентах по объему.
- 40. Отношение действительного количества воздуха (Vд), подводимого в процессе горения, к теоретически необходимому количеству (Vо), называется коэффициентом
- 41. СОСТАВ ПРОДУКТОВ СГОРАНИЯ Условно считают, что продукты сгорания топлива (в м3/кг) Vг = Vсг + Vвп
- 42. При α = 1 объем сухих газов минимальный, т.е. Vд = Vт. Если α > 1,
- 43. Объем водяных паров при нормальных условиях (ρ = 0,805 кг/м3) Или
- 44. При α = 1 VH2Omin = 0,01(Н2S +H2 + 2CH4 + 0,124dг +C2H4) + 0,0161Vг где
- 45. Объем сухих газов при α > 1: Vсг = Vсгmin + (α - 1)VT Vсгmin =
- 46. ВОДОПОДГОТОВКА
- 47. Вода является в настоящее время основным рабочим телом и теплоносителем в теплоэнергетике. Но её использование связано
- 48. Основные определения Количество вещества, содержащегося в определенном объеме или массе раствора (в данном случае – воды),
- 49. где: g – массовое количество вещества, растворенное в растворе, кг; Vр – объем раствора, м3; ρ
- 50. Молярная концентрация См показывает число килограмм - молекул данного вещества, растворенных в 1 м3 раствора. где
- 51. Под кг-экв понимается количество вещества, равное его эквивалентной массе, т.е. Где n - валентность в данной
- 52. Водородный показатель Молекулы воды, как и многие другие вещества, диссоциируют на ионы: Н2О↔Н++ОН- При данной температуре
- 53. Реакция среды считается нейтральной, если, г-ион/л. Для этого случая можно написать:
- 54. В кислой среде, очевидно, должно быть , а в щелочной . Для ионов ОН -, наоборот,
- 55. Выражение рОН=-lgCон- - будет называться гидроксильным показателем. Следовательно, равенство после логарифмирования и умножения на – 1
- 56. Основные показатели качества воды
- 57. Щелочность Щелочностью воды называется общее содержание в ней веществ, обуславливающих при диссоциации или в результате гидролиза
- 58. В зависимости от того, какой анион присутствует в воде (НСО, CO или ОН -), щелочность называют
- 59. Жесткость Жесткостью воды Ж0 называется сумма концентраций катионов кальция и магния, выраженная количеством миллиграмм – эквивалентов
- 60. Между ними имеется место, следующее соотношение: Ж0=Жк+Жнк=ЖСа+Жмq. (2-I) Карбонатная жестокость обусловливается присутствующими в воде бикарбонатами кальция
- 61. При расчетах процессов умягчения воды осадителями как внутри, так и вне котельного агрегата, а также других
- 62. Сухой остаток Сухим остатком воды называется суммарное количество нелетучих веществ, присутствующих в воде в коллоидном и
- 63. При определении сухого остатка природных вод бикарбонаты кальция и магния переходят в карбонаты СаСО3 Мq и
- 64. Окисляемость Окисляемость характеризует загрязненность воды органическими веществами, это характерно для вод болотного происхождения. Они окрашивают воду
- 65. Все природные воды содержат газы, среди которых следует особо отметить кислород и углекислый газ, вызывающие коррозию
- 66. Прозрачность Прозрачность выражается в сантиметрах высоты столба воды, налитой в специальный стеклянный цилиндр, сквозь который (столб)
- 67. ПРЕДОЧИСТКА
- 68. Осветление воды Осветлением называют процесс удаления из воды грубодисперсных и коллоидных примесей. Удаление грубодисперсных загрязнений может
- 69. Фильтрованием называют процесс осветления воды путем пропуска ее через пористый материал, в порах которого вода оставляет
- 70. Потеря напора в фильтрующем слое (иначе называемая сопротивлением этого слоя) зависит от скорости фильтрования, высоты фильтрующего
- 71. ∆hмакс=(0,8 - 1,0)*105 Па для напорных и (0,2–0,3)*105 Па для открытых фильтров. Скорость фильтрования на осветлительных
- 72. Величина фильтроцикла зависит от многих факторов, среди которых необходимо отметить концентрацию взвешенных веществ в фильтруемой воде
- 73. Если через фильтр пропущено количество воды, равное Qф, то (2.1) где hсл – высота фильтрующего слоя,
- 74. Устройство зернистых осветительных фильтров Существуют разные типы и конструкции осветительных фильтров. Конструктивно наиболее простым является однопоточный
- 75. В открытых фильтрах 2 фильтрование происходит под напором столба воды h в самом фильтре. Они широко
- 76. Они полностью загружаются фильтрующим материалом, в котором размещаются сборно-распределительные устройства. Как видно из схемы, они позволяют
- 77. С целью повышения скорости фильтрования, получения обработанной воды более высокого качества и увеличения грязеемкости материала в
- 78. Обработанная вода подается в центральную трубу, которой и распределяется по высоте слоя материала. Фильтрование идет по
- 79. В верхней части фильтра укреплены дырчатое распределительное устройство 1 и воздушная трубка 7. Имеющиеся два люка
- 80. Наиболее ответственным элементом фильтра является сборно-распределительное устройство 9, предназначенное для равномерного распределения воды по сечению фильтра,
- 81. Фильтр диаметром с 2 до 3,4 оборудуются трубчатым распределительным устройством. Оно состоит (рис. 4-5) из коллектора1,
- 82. Эксплуатация осветительных фильтров Работа фильтра состоит из двух периодов: фильтрования воды (рабочего) и промывки фильтра (простоя).
- 83. Фильтр выводится из работы и ставится на промывку, если потеря напора достигла заданного предела или в
- 84. Эта скорость характеризуется интенсивность промывки iпр л/(м2ּс), показывающей количество литров воды, проходящее в 1 с через
- 85. При промывке обратным током фильтрующий материал расширяется, занимая большой объем; возникает движение зерен материала в восходящем
- 86. Несколько минут фильтр работает в дренаж с целью удаления первых минут порций воды. Эта операция является
- 87. Производительность фильтровальной установки, состоящей из тф фильтров, может быть выражена количеством поданной на фильтры осветляемой воды
- 88. где nм.ф – количество промывок каждого фильтра в сутки; τм.ф - время простоя фильтра на промывке,
- 89. КОАГУЛЯЦИЯ ВОДЫ
- 90. Сущность процесса Коагуляцией называется процесс укрупнения (слипания, свертывания) коллоидных частиц, завершающийся выпадением вещества в осадок, удаляемый
- 91. Коллоидные растворы отличаются высокой устойчивостью. Это значит, что коллоидные частички не способны к самопроизвольному соединению в
- 92. Спустя некоторое время после ввода в пробу определенной дозы коагулянта происходит помутнение воды. С течением времени
- 93. При введении в воду, например, сернокислого алюминия вначале происходит его гидролиз. Al2(SO4)3+6Н2О↔2Al(ОН)3+3Н2SО4 Образующая кислота нейтрализует щелочность
- 94. Коагулирующим действием обладает не Fe(OН)2, а гидрат окиси железа Fe(OН)3. Следовательно, при применении в качестве коагулянта
- 95. Ввиду этого коагулируемая вода должна обладать некоторыми минимумом щелочности, мг-экв/кг, определяемым выражением Щмин=Ккг+0,4 где Ккг –
- 96. Результатом коагуляции воды являются увеличение ее прозрачности и снижение окисляемости. Поэтому эти показатели и используются для
- 97. ПРЕДОТВРАЩЕНИЕ ОБРАЗОВАНИЯ ОТЛОЖЕНИЙ В ПАРОВЫХ КОТЛАХ И ТЕПЛООБМЕННИКАХ
- 98. Состав, свойства и количество отложений. В результате воздействия тепла и реагентов, а также вследствие испарения в
- 99. Накипью называют достаточно плотные отложения, возникающие на поверхности нагрева или охлаждения и способные нарушать нормальную работу
- 100. Отложения могут быть описаны их физическими свойствами и химическим составом. Из физических свойств отмечают цвет, твердость,
- 101. Для эксплуатации важно знать состав отложений, так как он часто позволяет вскрыть причину их образований. Химический
- 102. Щелочноземельные накипи, состоящие в основном из соединений кальция и магния. К таким соединениям относятся: СаСО3, СаSО4,
- 103. Медные накипи, содержащие значительную долю меди. Силикатные накипи, имеющие различный состав. Наиболее важным свойством накипных отложений
- 104. где tв – температура среди (воды); , - соответственно толщина и теплопроводность, Q- тепловой поток отложений
- 105. Количество вносимых в котельный агрегат накипи - и шламообразующих веществ Вр, кг может быть определено по
- 106. Так как t составляет около 8-10 тыс. ч и более, даже при малых Cп.в получаются большие
- 107. Образование отложений в паровых котельных агрегатах
- 108. Образование щелочноземельных отложений Для образования щелочноземельных отложений необходимо наличие в котловой воде достаточно высокой концентрации накипеобразователей,
- 109. Однако выпадение этих соединений в осадок становится возможным лишь при некоторых условиях. Одно из них состоит
- 110. При Ск* САн>ПР выпадение осадка неизбежно, если же Ск*САн Для возникновения осадка, например СаСО3 совсем необязательна
- 112. Скачать презентацию










































































































 Қаныққан бу
Қаныққан бу Оптика твердотельных лазерных систем и сверхсильных полей
Оптика твердотельных лазерных систем и сверхсильных полей История изобретения паровых машин
История изобретения паровых машин Подготовил ученик 11 класса МОУ «Сош п.Сланцевый Рудник» Матросов Дима
Подготовил ученик 11 класса МОУ «Сош п.Сланцевый Рудник» Матросов Дима ЭНЕРГЕТИКА Энергетическая политика в России имеет особое значение. 1. Это связано с географическим п
ЭНЕРГЕТИКА Энергетическая политика в России имеет особое значение. 1. Это связано с географическим п Зрение домашних животных
Зрение домашних животных Закон сохранения и превращения энергии
Закон сохранения и превращения энергии Physical Output
Physical Output Многоканальный эмиссионный спектрометр ДФС-7
Многоканальный эмиссионный спектрометр ДФС-7 Экономное расходование электроэнергии в быту Автор: Ильина Анна, МОУ СОШ № 35 7 класс
Экономное расходование электроэнергии в быту Автор: Ильина Анна, МОУ СОШ № 35 7 класс  Өлшеу қателіктері
Өлшеу қателіктері Методы наблюдения и регистрации элементарных частиц
Методы наблюдения и регистрации элементарных частиц Расчет давления и атомных напряжений в МД
Расчет давления и атомных напряжений в МД Электростатическое поле в вакууме
Электростатическое поле в вакууме Активные среды твердотельных лазеров
Активные среды твердотельных лазеров Фізика як наука
Фізика як наука Конденсатор. Накопитель заряда
Конденсатор. Накопитель заряда Электрический ток в газах
Электрический ток в газах Тема: “Вплив електромагнітного поля на живі організми Підготував учень 11-В класу Філіп Василь
Тема: “Вплив електромагнітного поля на живі організми Підготував учень 11-В класу Філіп Василь  Инерция. Билет 2
Инерция. Билет 2 Механические волны. Звук
Механические волны. Звук Электрическое поле (Лекция 2)
Электрическое поле (Лекция 2) Презентация по физике "Масса тела" - скачать бесплатно
Презентация по физике "Масса тела" - скачать бесплатно ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ И АЛЬБЕРТ ЭЙНШТЕЙН
ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ И АЛЬБЕРТ ЭЙНШТЕЙН  Электрическое поле. Напряженность поля. Принцип суперпозиции полей
Электрическое поле. Напряженность поля. Принцип суперпозиции полей Механикалық қозғалыс және оның түрлері. Кинематиканың негізгі түсініктері және теңдеулері
Механикалық қозғалыс және оның түрлері. Кинематиканың негізгі түсініктері және теңдеулері Густина. Одиниці густини
Густина. Одиниці густини Получение и передача переменного электрического тока
Получение и передача переменного электрического тока