Содержание
- 2. Уравнение состояния идеального газа. Газовые законы. Уравнение состояния идеального газа. Газовые законы.
- 3. Уравнение, связывающее основные параметры состояния идеального газа вывел великий русский ученый Д.И. Менделеев.
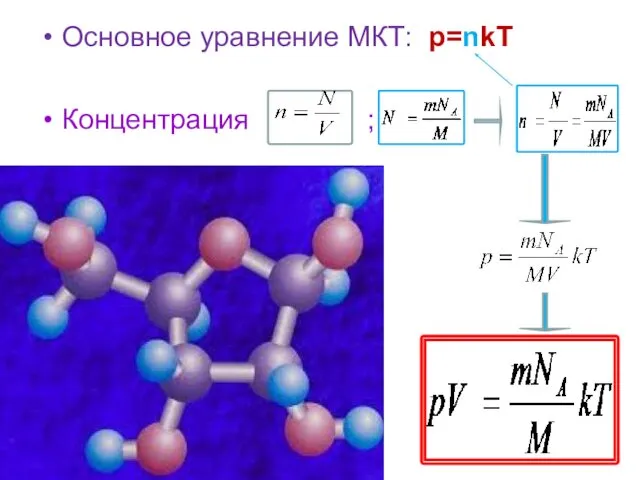
- 4. Основное уравнение МКТ: p=nkT Концентрация ;
- 5. NA –постоянная Авогадро k- постоянная Больцмана NAk= R – универсальная(молярная) газовая постоянная R = 8,31 Дж/моль·К.
- 6. Уравнение состояния для идеального газа произвольной массы. Уравнение Менделеева
- 7. Из уравнения состояния вытекает связь между давлением, объемом и температурой идеального газа, который может находиться в
- 8. Уравнение Клапейрона Для постоянной массы идеального газа отношение произведения давления на объем к абсолютной температуре в
- 9. Газовые законы С помощью уравнения Можно исследовать процессы, в которых один из трех параметров остается неизменным.
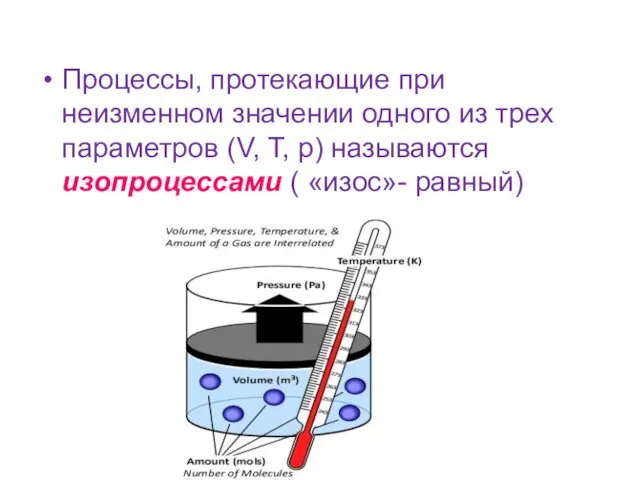
- 10. Процессы, протекающие при неизменном значении одного из трех параметров (V, T, p) называются изопроцессами ( «изос»-
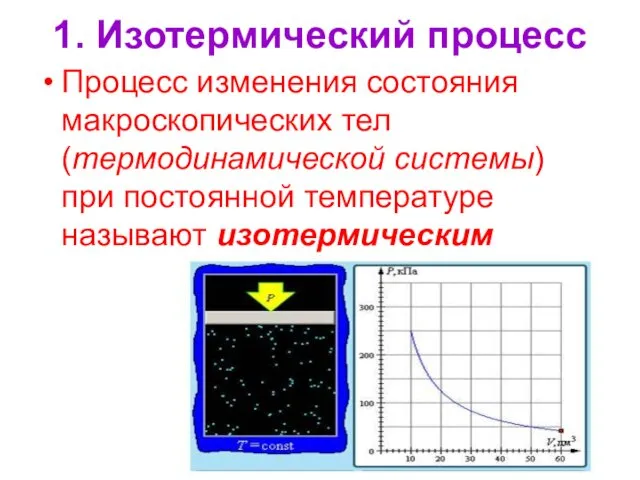
- 11. 1. Изотермический процесс Процесс изменения состояния макроскопических тел (термодинамической системы) при постоянной температуре называют изотермическим
- 12. Закон Бойля- Мариотта Для газа данной массы при постоянной температуре произведение давления газа на его объем
- 13. Зависимость давления от объема при Т=const изображают кривой, называемой изотермой. Т1
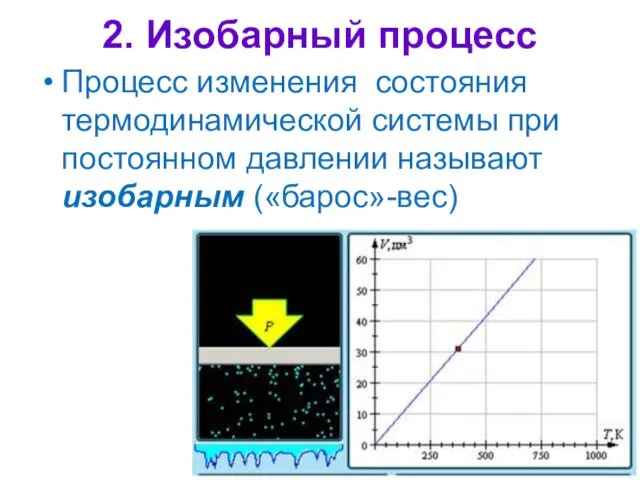
- 14. 2. Изобарный процесс Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным («барос»-вес)
- 15. Закон Гей-Люссака Для газа данной массы при постоянном давлении отношение объема к температуре постоянно при р
- 16. Графическая зависимость объема от температуры (изобара)
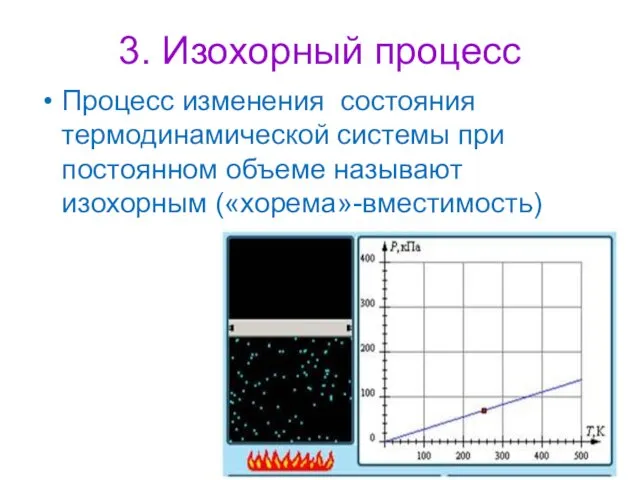
- 17. 3. Изохорный процесс Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным («хорема»-вместимость)
- 18. Закон Шарля Для газа данной массы отношение давления к температуре постоянно. Если объем не меняется При
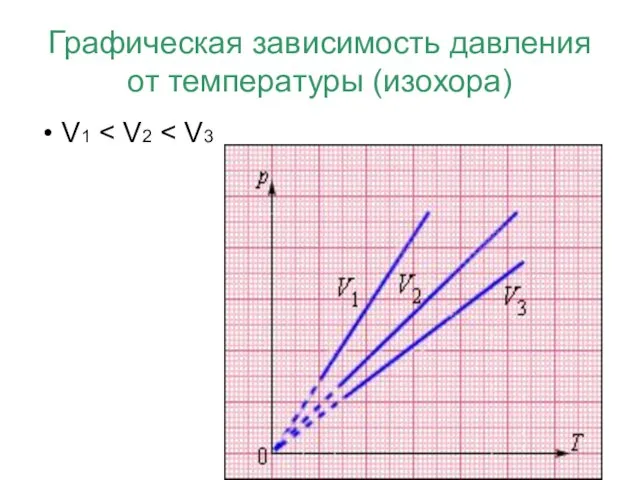
- 19. Графическая зависимость давления от температуры (изохора) V1
- 21. Домашнее задание §68,§69
- 23. Скачать презентацию














 Гравитационные взаимодействия
Гравитационные взаимодействия ІІ закон термодинаміки
ІІ закон термодинаміки  Аттестационная работа. Физический практикум в 11 классе с использованием лабораторного оборудования
Аттестационная работа. Физический практикум в 11 классе с использованием лабораторного оборудования Сушка. Три этапа в сушке материала. (Лекция 5)
Сушка. Три этапа в сушке материала. (Лекция 5) Лазеры. Принцип действия
Лазеры. Принцип действия Закон сохранения механической энергии. Механические колебания
Закон сохранения механической энергии. Механические колебания Магнитное поле в веществе. Лекция 18
Магнитное поле в веществе. Лекция 18 Электр зарядының сақталу заңы
Электр зарядының сақталу заңы Окружающий мир как иерархическая система. 9 класс
Окружающий мир как иерархическая система. 9 класс Первый закон термодинамики
Первый закон термодинамики Потери тепла через наружные ограждающие конструкции
Потери тепла через наружные ограждающие конструкции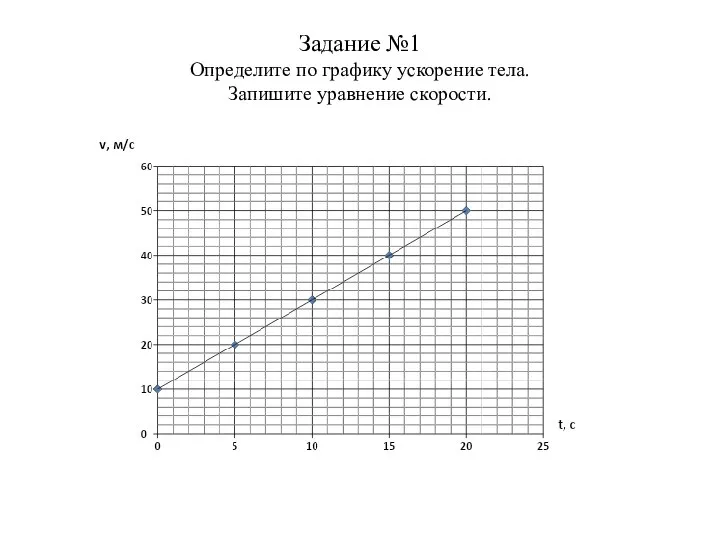 Определите по графику ускорение тела
Определите по графику ускорение тела Сравнение наблюдательных исторических данных о вспышках сверхновых 1054 года в Тельце и 1604 года в Змееносце с данными из электро
Сравнение наблюдательных исторических данных о вспышках сверхновых 1054 года в Тельце и 1604 года в Змееносце с данными из электро Презентация на тему “Ядерные реакции”
Презентация на тему “Ядерные реакции”  Закон Паскаля
Закон Паскаля  Презентация по физике "Атмосферное давление 7 класс" - скачать
Презентация по физике "Атмосферное давление 7 класс" - скачать  Презентация по физике "Електричний струм в рідинах" - скачать бесплатно
Презентация по физике "Електричний струм в рідинах" - скачать бесплатно Загадка Роберта Вуда (спектры и спектральный анализ)
Загадка Роберта Вуда (спектры и спектральный анализ) Химические методы получения нанопорошков: осаждение из растворов
Химические методы получения нанопорошков: осаждение из растворов Сила Лоренца. (Лекции 15-16)
Сила Лоренца. (Лекции 15-16) Техническое облуживание АКПП с гидравлическим приводом
Техническое облуживание АКПП с гидравлическим приводом Электрическое поле. Напряжённость электрического поля
Электрическое поле. Напряжённость электрического поля Внутренний фотоэффект в металлах
Внутренний фотоэффект в металлах Введение в электротехнику
Введение в электротехнику Изотермический процесс, нагрев
Изотермический процесс, нагрев Тепловые балансы ВТУ, их разновидности. Тепловой баланс теплотехнологического реактора
Тепловые балансы ВТУ, их разновидности. Тепловой баланс теплотехнологического реактора Многоэлектронные атомы. Взаимодействие атомов с излучением
Многоэлектронные атомы. Взаимодействие атомов с излучением Презентация-исследование
Презентация-исследование