Содержание
- 2. Влажный воздух Влажный воздух – это смесь сухого воздуха и водяного пара. По закону Дальтона для
- 3. Абсолютная и относительная влажности воздуха Абсолютная влажность воздуха – это масса пара в 1 м³ влажного
- 4. Влагосодержание влажного воздуха Влагосодержание воздуха – это масса водяного пара, приходящаяся на 1 кг сухого воздуха
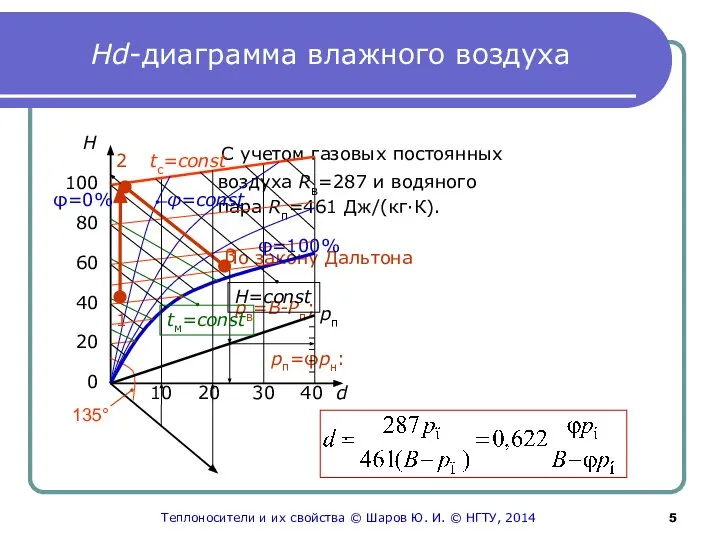
- 5. Hd-диаграмма влажного воздуха С учетом газовых постоянных воздуха Rв=287 и водяного пара Rп=461 Дж/(кг·К). По закону
- 6. К Hd-диаграмме Hd-диаграмма была предложена профессором Л.К. Рамзиным в 1918 году. Она удобна для исследования процессов
- 7. Процессы в Hd-диаграмме Цифры на оси ординат – это температуры сухого воздуха, °С и энтальпии влажного
- 8. I закон термодинамики для потока 1 кг/с газа в сечениях I и II перемещается на расстояние
- 9. Работа проталкивания Для ввода 1 кг/с в сечение I, надо совершить работу lI=-p1f1s1=-p1v1. В сечении II
- 10. Составляющие работы Работа на изменение кинетической энергии потока: l2=с22/2-с12/2, (3) где с1 и с2 – скорости
- 11. Последние составляющие работы В общем случае, между сечениями I и II газ может совершать техническую работу
- 12. Уравнение I закона термодинамики для потока Так как lтр=qтр, то они сокращаются. Перегруппируем члены полученного уравнения;
- 13. Изменения потенциальной и кинетической энергий газа Для газов gdz выражение I закона термодинамики для обратимого и
- 14. I закон термодинамики для обратимого, адиабатного потока Аналитическое выражение I закона термодинамики для обратимого, адиабатного изменения
- 15. Истечение газов и паров через суживающиеся сопла Рассмотрим обратимое, адиабатное истечение газа через суживающееся сопло. Для
- 16. Соотношения между параметрами Для адиабатного процесса: p1v1k=pvk, или p11/kv1=p1/kv. Выразим удельный объем из уравнения адиабаты и
- 17. Скорость истечения газа Вынесем за скобки первый член и найдем скорость обратимого истечения газа: . (2)
- 18. Массовый расход газа При адиабатном истечении p1v1k=p2v2k, откуда v2=v1(p1/p2)1/k. (4) Подставляем (4) и (2) в (3):
- 19. К гипотезе Сен-Венана и Вентцеля В формуле расхода газа (6) переменным является выражение в квадратных скобках.
- 20. Исследование на экстремум Чтобы найти mmax , надо исследовать функцию на экстремум, то есть: . Поделим
- 21. Критическое отношение давлений Если в выражение (7) для βкр подставить значения показателей адиабаты k газов, то
- 22. Критическая скорость истечения Подставив βкр в формулу (2), получим критическую скорость истечения: . (8) Если в
- 23. Гипотеза Сен-Венана и Вентцеля ● с Из формулы (9) следует, что критическая скорость истечения – это
- 24. Гипотеза Сен-Венана и Вентцеля ● c=cкр ● c=cкр: относительная скорость (a-cкр)=0; импульс разряжения никогда не дойдет
- 25. Комбинированное сопло (Лаваля) Комбинированное из сужающейся и расширяющейся частей сопло впервые применил шведский инженер Лаваль для
- 26. Режимы истечения Отношение β Суживающееся сопло Сопло Лаваля β>βкр c β=βкр c=cкр с=скр; β cкр. Действительная
- 27. Скорость истечения пара Скорость необратимого истечения пара можно найти из выражения (7) I закона термодинамики в
- 28. Истечение газов с учетом трения Из-за потерь части кинетической энергии газа на трение и завихрение действительная
- 29. Дросселирование газов и паров Если при движении газа он встречает местные сужения (вентиль, шайба), то происходит
- 30. Дросселирование – условно изоэнтальпийный процесс Потери на трение превращаются в теплоту, которая в адиабатном процессе воспринимается
- 31. Дросселирование газов Изменение энтальпии газа: h1-h2=cp(t1-t2). Для условно изоэнтальпийного дросселирования h2=h1, то есть t2=t1. Но это
- 32. Температура инверсии На предыдущем слайде изображено дросселирование воздуха при разных начальных температурах. При достаточно высокой начальной
- 33. Использование дросселирования для ожижения газов Снижение температуры газа при дросселировании, если tнач Для этого газ многократно
- 34. Дросселирование (мятие) пара Если мятию подвергается перегретый пар 1-2, то давление и температура его уменьшаются, а
- 35. Снижение работоспособности пара при дросселировании Из диаграммы хорошо видно, что работоспособность пара после дросселирования значительно падает
- 37. Скачать презентацию

































 Выполнил : учитель физики МОУ «СОШ № 47» г. Саратов Ересько Г.В.
Выполнил : учитель физики МОУ «СОШ № 47» г. Саратов Ересько Г.В. Магнит өрісі
Магнит өрісі Презентация по физике Сила тяжести
Презентация по физике Сила тяжести  Законы термодинамики Первый закон термодинамики является, в сущности, законом сохранения энергии, распространенным на все ма
Законы термодинамики Первый закон термодинамики является, в сущности, законом сохранения энергии, распространенным на все ма Строительная акустика. Транспортный шум
Строительная акустика. Транспортный шум Плавание судов
Плавание судов Щелочные АКБ. Электролит щелочных АКБ
Щелочные АКБ. Электролит щелочных АКБ Холодильные установки. Криогенные жидкости. Компрессоры
Холодильные установки. Криогенные жидкости. Компрессоры Расчет тихоходного вала одноступенчатого цилиндрического редуктора Предварительный расчет тихоходного вала Выбор материала в
Расчет тихоходного вала одноступенчатого цилиндрического редуктора Предварительный расчет тихоходного вала Выбор материала в Презентация УРОК ФИЗИКИ В 10 КЛАССЕ Броуновское движение Строение вещества
Презентация УРОК ФИЗИКИ В 10 КЛАССЕ Броуновское движение Строение вещества  Презентация по физике "Реакция электролиза" - скачать
Презентация по физике "Реакция электролиза" - скачать  Презентация Равномерное и равноускоренное движение
Презентация Равномерное и равноускоренное движение Давление
Давление Почему на рыхлом снегу лыжник не проваливается, а пешеход проваливается?
Почему на рыхлом снегу лыжник не проваливается, а пешеход проваливается? Қызыл спрайт
Қызыл спрайт Презентация по физике "Оптика 11 класс" - скачать
Презентация по физике "Оптика 11 класс" - скачать 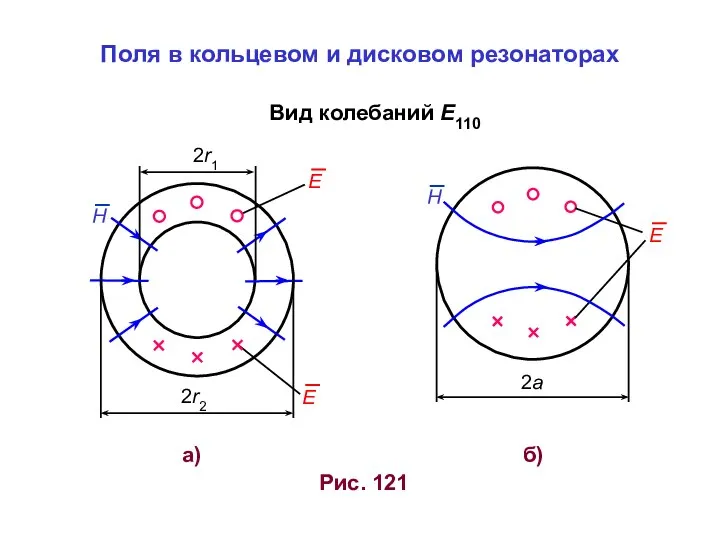 Поля в кольцевом и дисковом резонаторах
Поля в кольцевом и дисковом резонаторах Законы коммутации
Законы коммутации Хаос и катастрофы
Хаос и катастрофы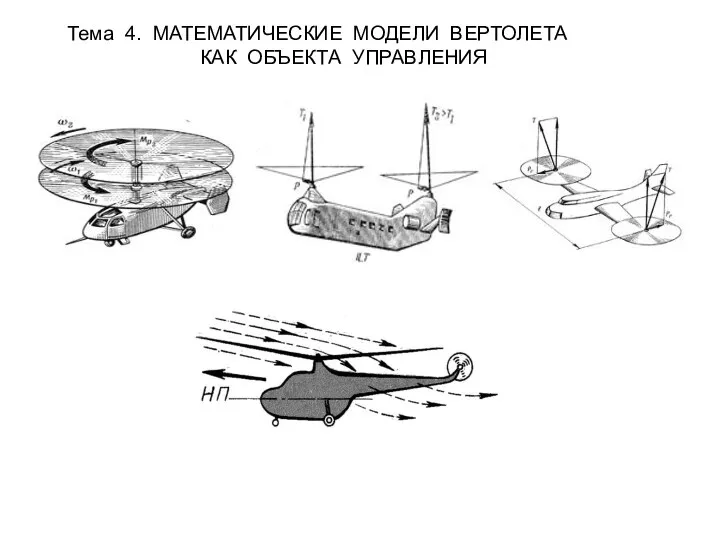 Тема 4. Математические модели вертолета как объекта управления
Тема 4. Математические модели вертолета как объекта управления Дыбыс тербелістері
Дыбыс тербелістері Зачем физика нужна инженеру Презентацию подготовили ученицы ХI класса «А» МОУ Аннинский лицей Семынина Инна Гончаренко Екатер
Зачем физика нужна инженеру Презентацию подготовили ученицы ХI класса «А» МОУ Аннинский лицей Семынина Инна Гончаренко Екатер Сильно легированные и некристаллические полупроводники
Сильно легированные и некристаллические полупроводники Электронная спектроскопия
Электронная спектроскопия Движение. Реактивный самолет
Движение. Реактивный самолет Трансформаторы. (Лекция 1)
Трансформаторы. (Лекция 1) Закрашивание Рендеринг полигональных моделей. (Лекция 7)
Закрашивание Рендеринг полигональных моделей. (Лекция 7) Середня швидкість
Середня швидкість