Содержание
- 2. При сравнении с бинарными металл - водородными системами, рассмотренными в предшествующей главе, системы водород - сплав
- 3. Поэтом следующий шаг заключается в разработке формализма, который учитывает распределение энергий местонахождения для атомов H. Этот
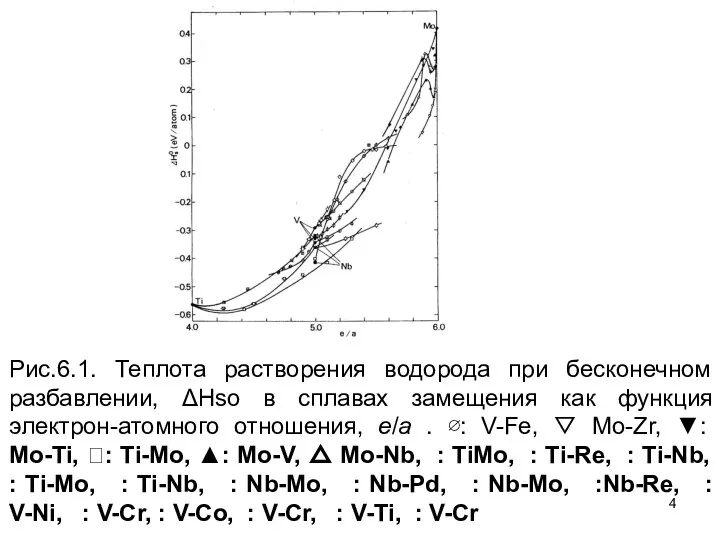
- 4. Рис.6.1. Теплота растворения водорода при бесконечном разбавлении, ΔHso в сплавах замещения как функция электрон-атомного отношения, e/a
- 5. Кроме того, крутые линии, наблюдаемые для Mo–V и сплавов Mo–Nb близко к Mo стороне, и широкий
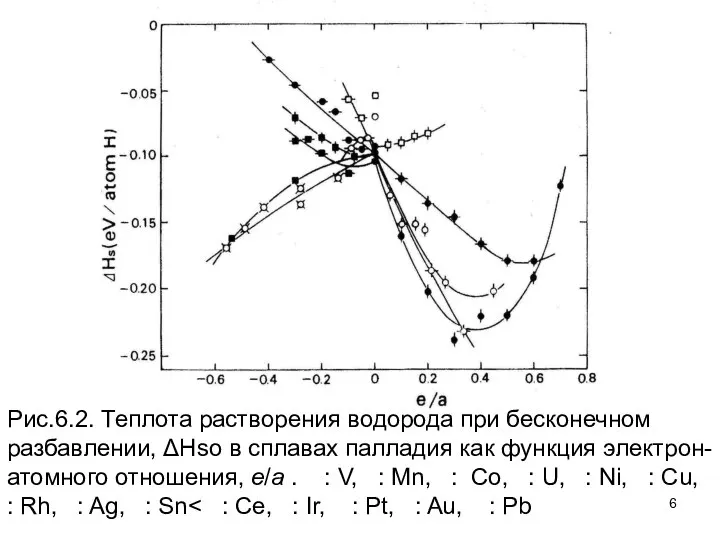
- 6. Рис.6.2. Теплота растворения водорода при бесконечном разбавлении, ΔHso в сплавах палладия как функция электрон-атомного отношения, e/a
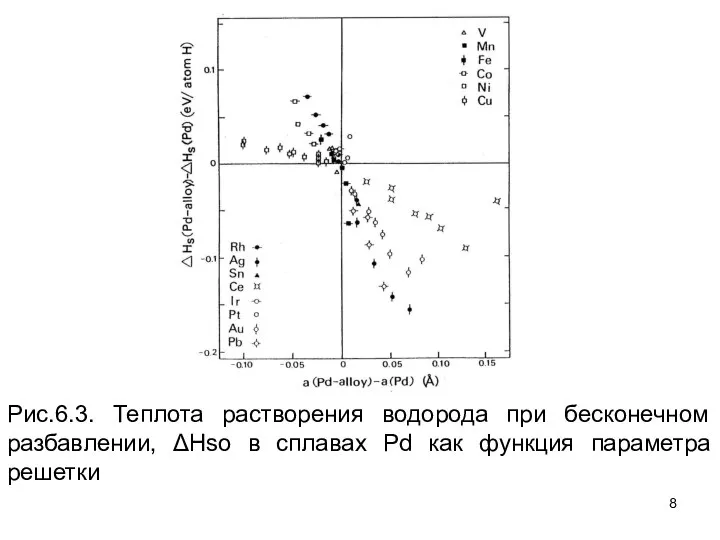
- 7. Фактически лучшая корреляция была найдена, когда значения ΔНso нанесены против постоянной кристаллической решетки, как это показано
- 8. Рис.6.3. Теплота растворения водорода при бесконечном разбавлении, ΔHso в сплавах Pd как функция параметра решетки
- 9. использование Ко = 1923 ГПа и vH = 2.8 Å3. Если мы включаем растворенные вещества Cu
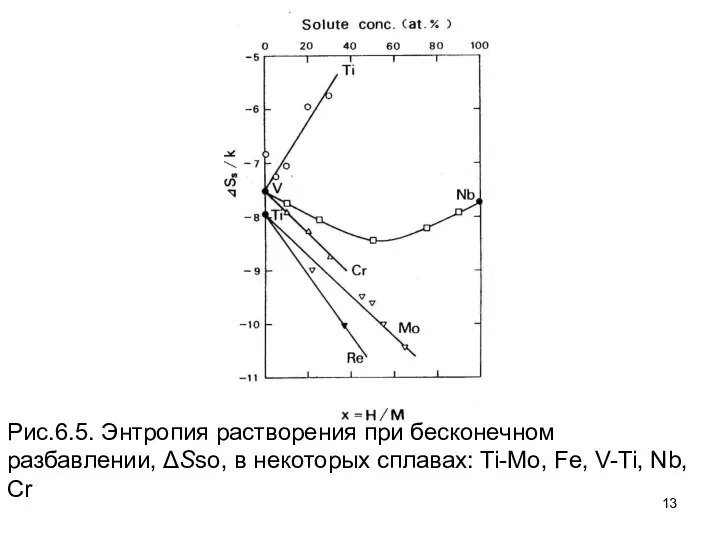
- 10. Интересные результатов по влиянию легирования могут быть получено при исследовании энтропии растворов при бесконечном разведении ΔSs.
- 11. Подобные наблюдения были сделаны в Ti, V и сплавах Nb, как это показано на рис. 6.5.
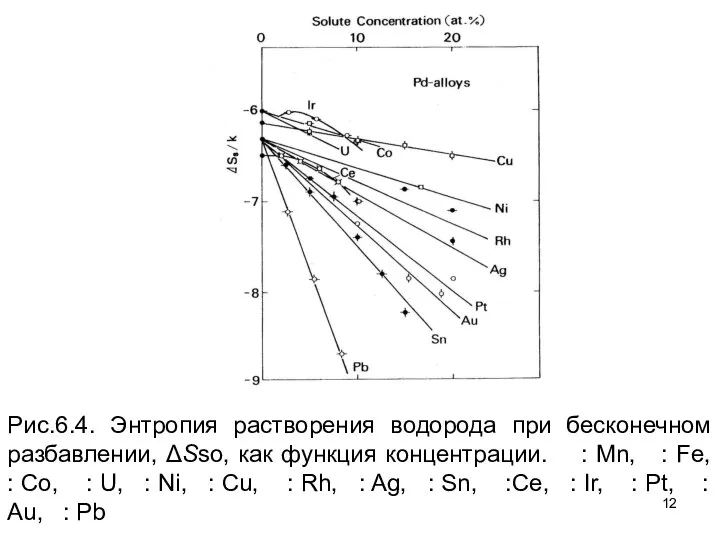
- 12. Рис.6.4. Энтропия растворения водорода при бесконечном разбавлении, ΔSso, как функция концентрации. : Mn, : Fe, :
- 13. Рис.6.5. Энтропия растворения при бесконечном разбавлении, ΔSso, в некоторых сплавах: Ti-Mo, Fe, V-Ti, Nb, Cr
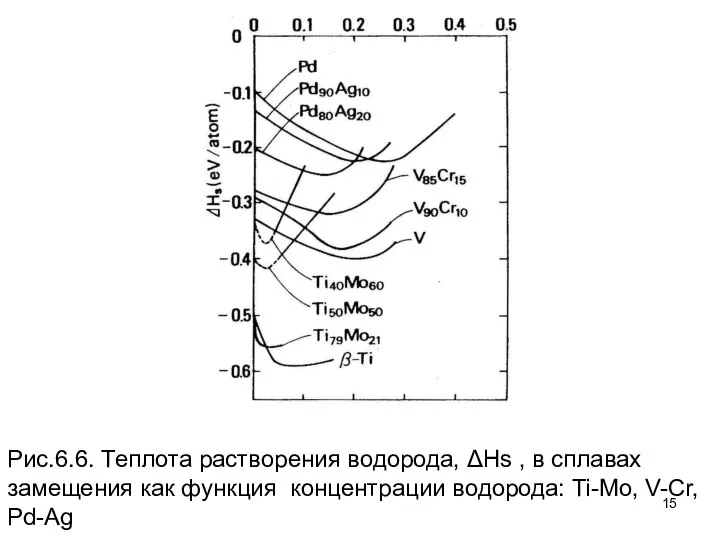
- 14. Теплоты растворения при более высоких концентрациях водорода также подтверждают этот вывод. Рисунок 6.6 показывает, что увеличение
- 15. Рис.6.6. Теплота растворения водорода, ΔHs , в сплавах замещения как функция концентрации водорода: Ti-Mo, V-Cr, Pd-Ag
- 16. Влияние легирования на предельную растворимость водорода в сплавах
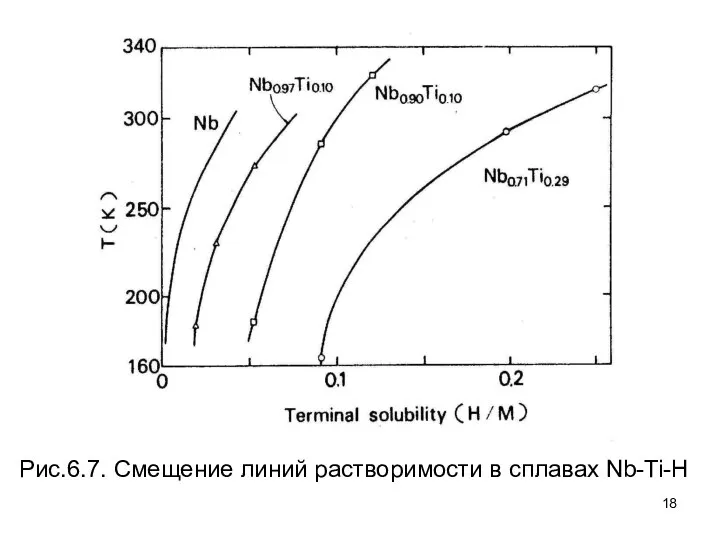
- 17. В легированных сплавах предельная растворимость водорода (Terminal Solubiliti of Hydrogen - TSH) при низких концентрациях растворенного
- 18. Рис.6.7. Смещение линий растворимости в сплавах Nb-Ti-H
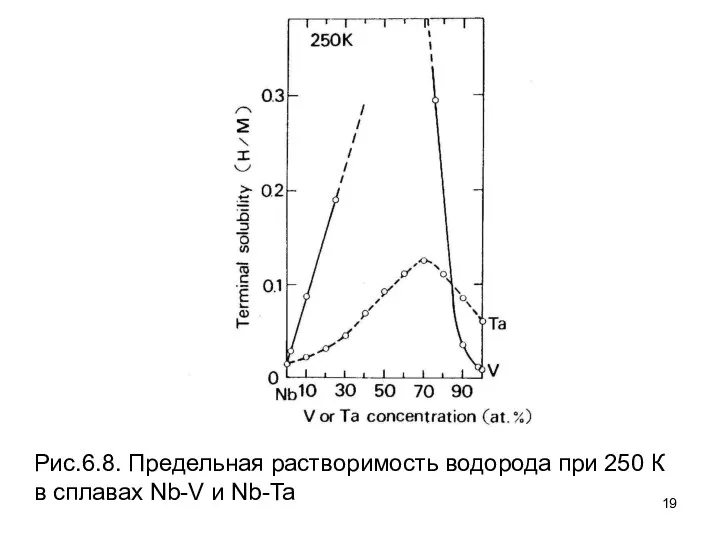
- 19. Рис.6.8. Предельная растворимость водорода при 250 К в сплавах Nb-V и Nb-Ta
- 20. Рассмотрим равновесное состояние между α и β фазами псевдобинарной системы МНx, где М = A1-yBy. Предположим,
- 21. Равновесное состояние, условие общей касательной может быть записано так: следовательно, Замена Для свободной энергии формирования гидрида
- 22. Отметим здесь, что левая часть – возрастающая функция x в концентрационном диапазоне, представляющем интерес: 0 Предполагается,
- 23. Растворение водорода. Захват и блокировка В большинстве предшествующих исследованиях принималось, что H атомы распределены по междоузлиям,
- 24. Так называемый двухямочный формализм (состояний) применяется к междоузлиям, которые имеют две различные энергии захвата или блокировки.
- 25. 6.14) из которого получаем (6.15) Здесь, как и прежде, концентрации написаны как отношения к числу М.
- 26. , r = N/No, x = n/No, rd = Nd / No, и Θ = exp
- 27. по сравнению с первоначальным родным металлом, не содержащим атомы растворенного вещества, химический потенциал, как и предполагалось,
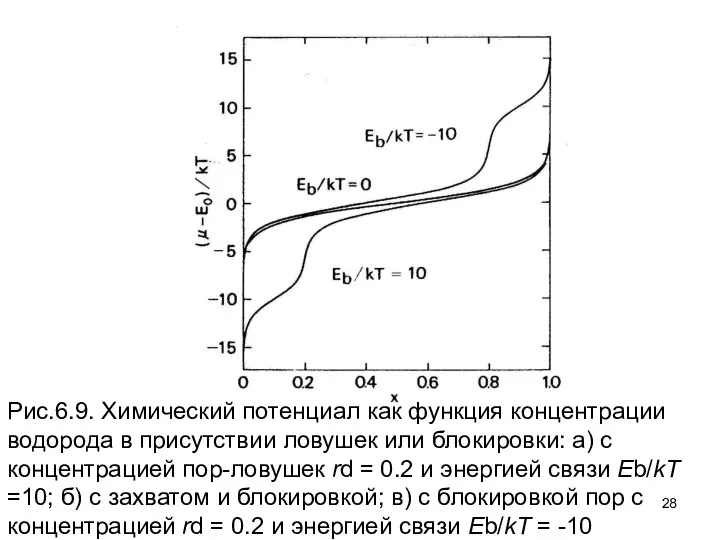
- 28. Рис.6.9. Химический потенциал как функция концентрации водорода в присутствии ловушек или блокировки: а) с концентрацией пор-ловушек
- 29. Рассмотрение как влияет легирование на спинодальный распад может быть выполнено, прибавляя терм – к химическому потенциалу
- 30. Водород в аморфных сплавах
- 31. Большинство аморфных сплавов сформированы в результате быстро охлаждая расплав к комнатной температуре или ниже при скоростях
- 32. Таким образом, при насыщении аморфных сплавов водородом или электролизе, или газовой фазы, должны быть приняты меры
- 33. Термодинамические свойства водорода в аморфных сплавах Рассматриваемые здесь аморфные сплавы имеют отрицательные теплоты растворения водорода. Они
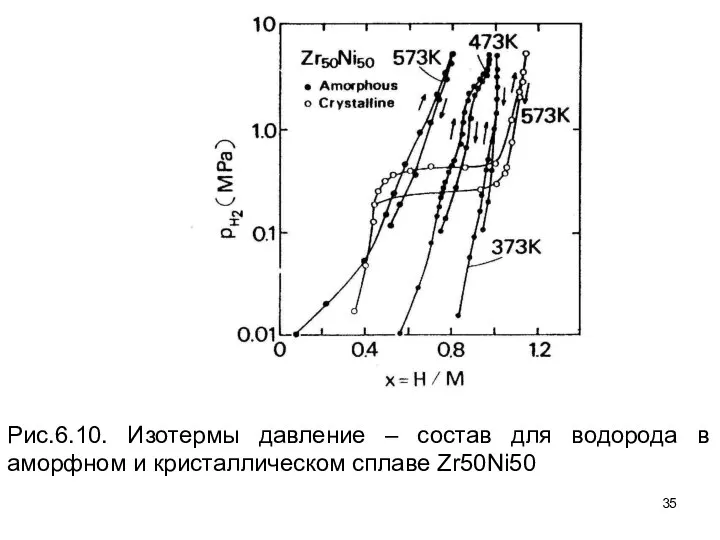
- 34. Типичные кривые p–x–T , измеренные для сплава Zr–Ni, показаны на рис. 6.10. Одно из наиболее характерных
- 35. Рис.6.10. Изотермы давление – состав для водорода в аморфном и кристаллическом сплаве Zr50Ni50
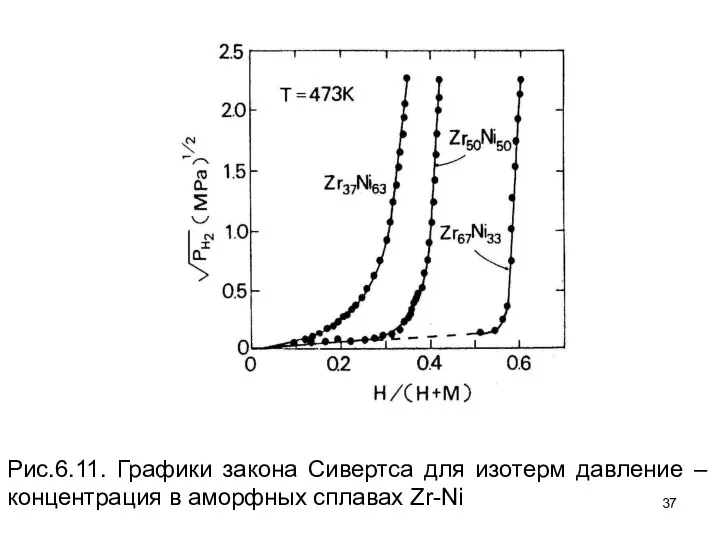
- 36. Рисунок 6.11 показывает, что закон Сивертса для аморфных сплавов практически не соблюдается. Положительное отклонение от закона
- 37. Рис.6.11. Графики закона Сивертса для изотерм давление – концентрация в аморфных сплавах Zr-Ni
- 38. . Как в кристаллических металлах и сплавах, гидрирование в большинстве случаев вызывает объемное расширение, с увеличением
- 39. Распределение атомов водорода по энергии местонахождения
- 40. Непрерывное распределение энергий местонахождения может быть описано в терминах местонахождения – функция энергетического распределения D (E)
- 41. Число H атомов, занимающих эти местонахождения, может быть расписано так где f(E) - функция распределения Ферми
- 42. Предположим, что энергетическое распределение по местонахождениям может быть представлено функцией Гаусса: Для kT где интеграл вероятности
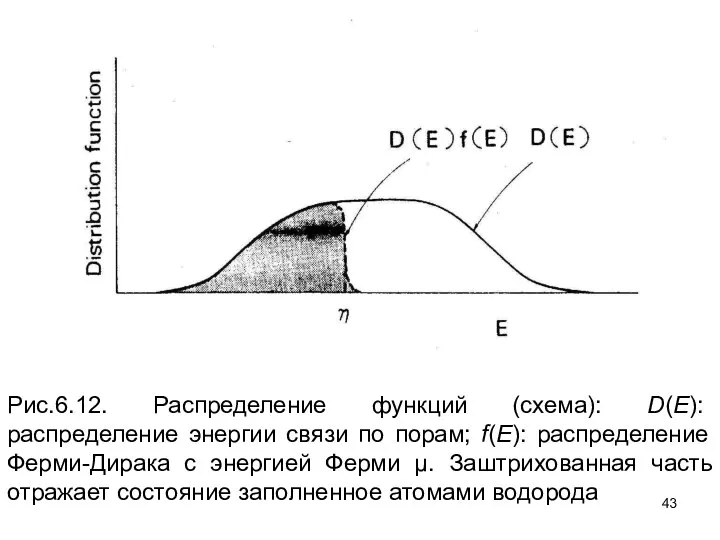
- 43. Рис.6.12. Распределение функций (схема): D(E): распределение энергии связи по порам; f(E): распределение Ферми-Дирака с энергией Ферми
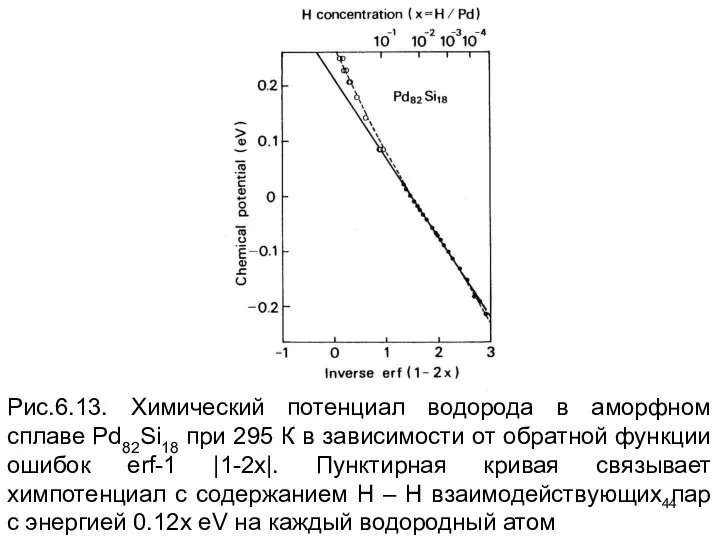
- 44. Рис.6.13. Химический потенциал водорода в аморфном сплаве Pd82Si18 при 295 К в зависимости от обратной функции
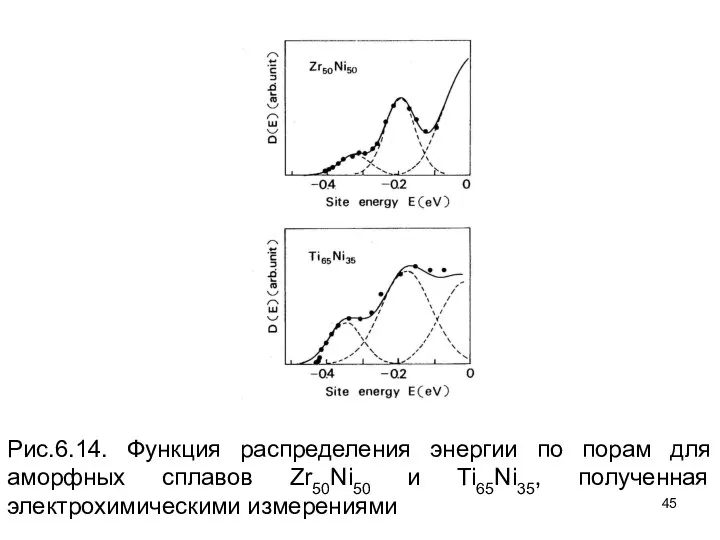
- 45. Рис.6.14. Функция распределения энергии по порам для аморфных сплавов Zr50Ni50 и Ti65Ni35, полученная электрохимическими измерениями
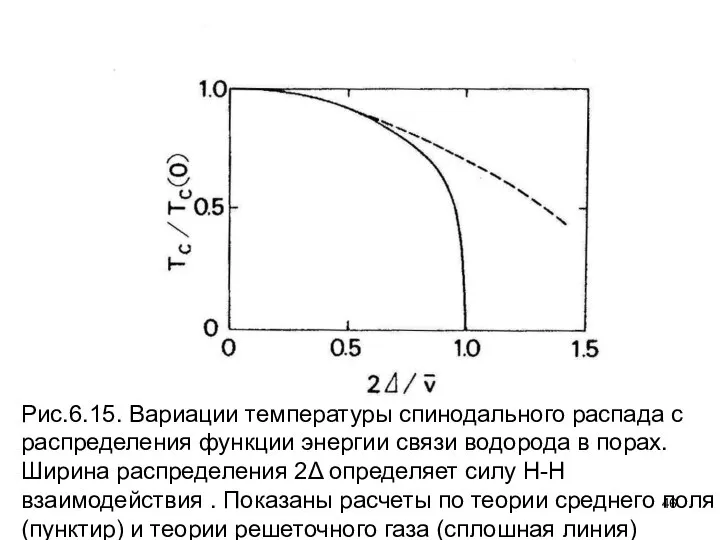
- 46. Рис.6.15. Вариации температуры спинодального распада с распределения функции энергии связи водорода в порах. Ширина распределения 2Δ
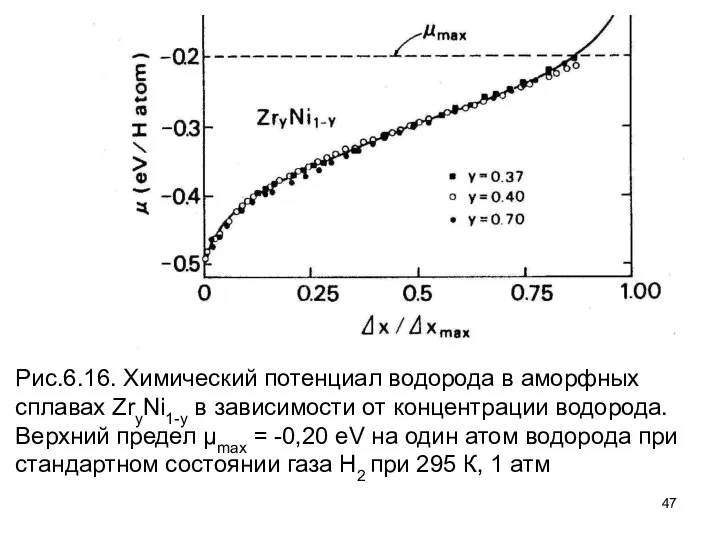
- 47. Рис.6.16. Химический потенциал водорода в аморфных сплавах ZryNi1-y в зависимости от концентрации водорода. Верхний предел μmax
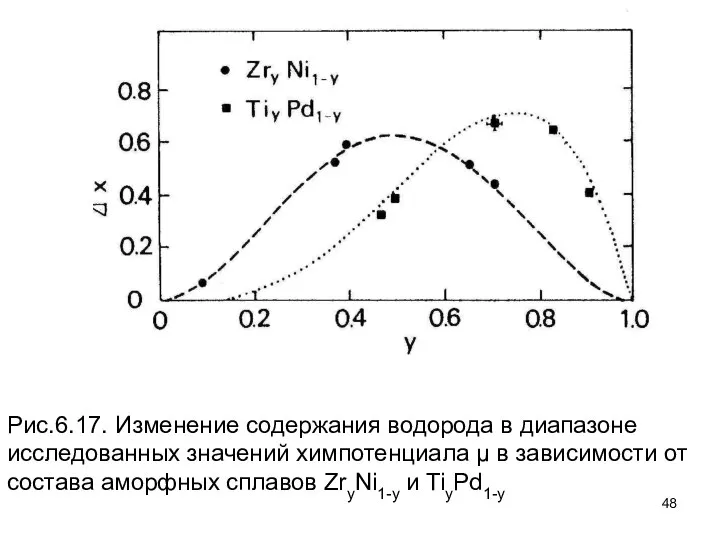
- 48. Рис.6.17. Изменение содержания водорода в диапазоне исследованных значений химпотенциала μ в зависимости от состава аморфных сплавов
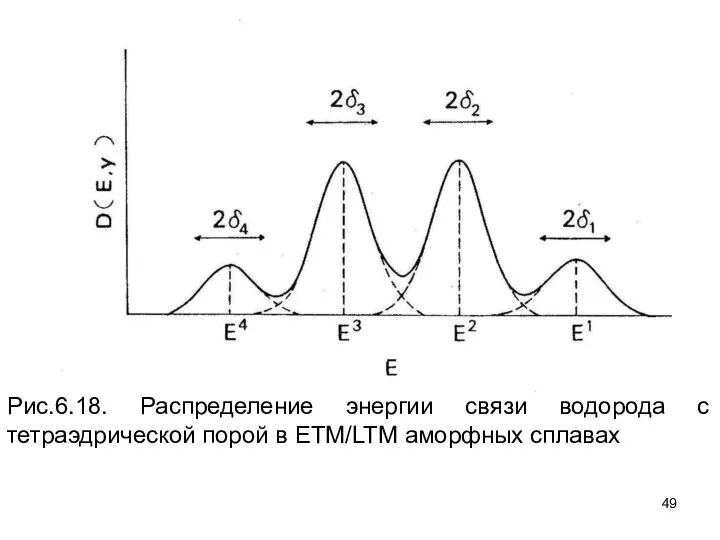
- 49. Рис.6.18. Распределение энергии связи водорода с тетраэдрической порой в ETM/LTM аморфных сплавах
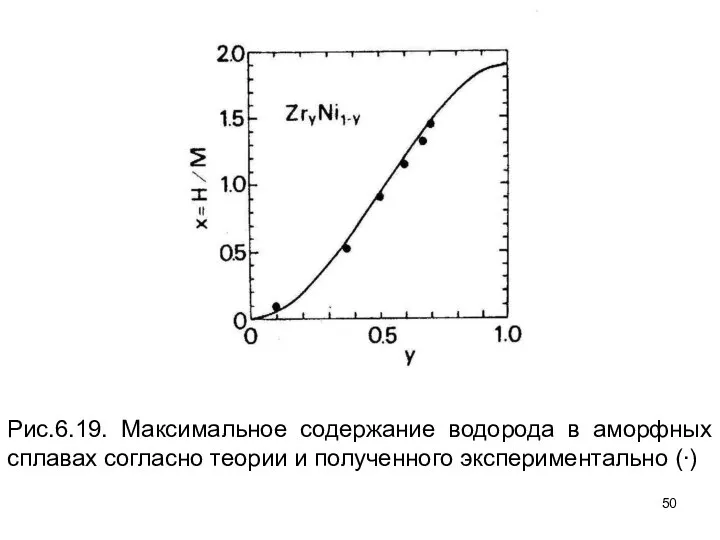
- 50. Рис.6.19. Максимальное содержание водорода в аморфных сплавах согласно теории и полученного экспериментально (∙)
- 51. В 1983 г. Yeh и другие сообщили, что аморфная структура может быть сформирована посредством насыщения кристаллического
- 52. Это явление, называемое вынужденным водородом переход в аморфное состояние (Hydrogen Induced of Amorphous - HIA), если
- 54. Только составы СеМ2 переходят в аморфными в широком диапазоне температур. Во всех этих сплавах переход в
- 55. Термодинамику HIA изучали дифференциальным термографическим анализом в H2 атмосфере, в которой кристаллический GdFe2Hx переходит в аморфное
- 57. Скачать презентацию


































 Нерелятивистская (ньютонова) механика. Кинематика
Нерелятивистская (ньютонова) механика. Кинематика Использование солнечной энергии на Земле
Использование солнечной энергии на Земле УРОК ФИЗИКИ В 10 КЛАССЕ Основные положения МКТ
УРОК ФИЗИКИ В 10 КЛАССЕ Основные положения МКТ 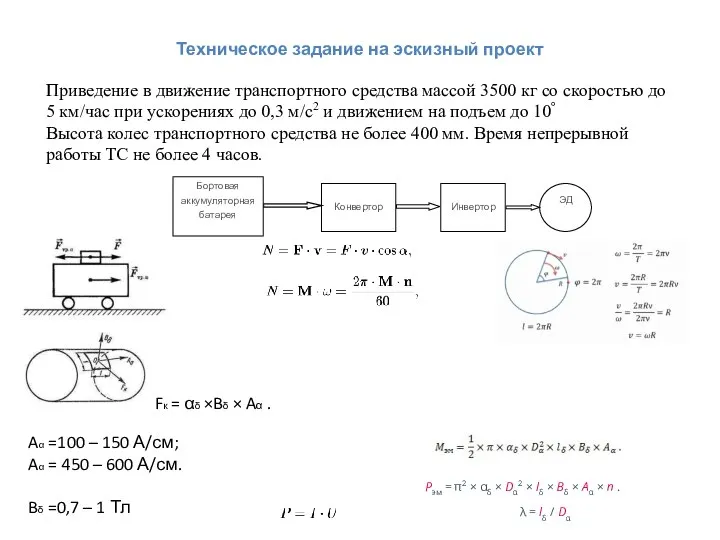 Техническое задание на эскизный проект
Техническое задание на эскизный проект Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій
Активізація пізнавальної діяльності учнів на уроках фізики шляхом використання проблемних ситуацій История паровых машин
История паровых машин Проектирование цифрового устройства управления обогревом помещения с применением микроконтроллера
Проектирование цифрового устройства управления обогревом помещения с применением микроконтроллера Основные положения теории теплопроводности
Основные положения теории теплопроводности Каналы связи по линиям электропередач
Каналы связи по линиям электропередач Твёрдые тела. Кристаллические и аморфные тела.
Твёрдые тела. Кристаллические и аморфные тела.  Технологический процесс получения электроэнергии на станциях разных типов. (Лекция 1)
Технологический процесс получения электроэнергии на станциях разных типов. (Лекция 1) Ток и заряд в магнитном поле
Ток и заряд в магнитном поле Электротехника и электроника. Лекция № 3. Нелинейные электрические цепи постоянного тока
Электротехника и электроника. Лекция № 3. Нелинейные электрические цепи постоянного тока Волновые процессы
Волновые процессы Механическое движение. Виды движения. Скорость. Ускорение. Прямолинейное равномерное и неравномерное движения
Механическое движение. Виды движения. Скорость. Ускорение. Прямолинейное равномерное и неравномерное движения Телескоп из одной линзы
Телескоп из одной линзы Электричество и его роль в развитии человечества
Электричество и его роль в развитии человечества Методы анализа элементного состава материалов
Методы анализа элементного состава материалов Ультразвук в науке и технике. УЗ сварка. УЗ очистка. Применение акустических волн для увеличения нефтедобычи
Ультразвук в науке и технике. УЗ сварка. УЗ очистка. Применение акустических волн для увеличения нефтедобычи Приведение системы сил к заданному центру. Теорема Пуансо
Приведение системы сил к заданному центру. Теорема Пуансо Рубка металла
Рубка металла Физика 9 класс Тема урока: «Механическое движение. Материальная точка. Система отсчета.»
Физика 9 класс Тема урока: «Механическое движение. Материальная точка. Система отсчета.» Оборудование и технология наноматериалов механическим измельчением и механохимическим воздействием
Оборудование и технология наноматериалов механическим измельчением и механохимическим воздействием Theoretical principles of bioenergetics
Theoretical principles of bioenergetics Ускорение свободного падения
Ускорение свободного падения Физические величины
Физические величины Модернизация выжигателя
Модернизация выжигателя Магнит и его свойства
Магнит и его свойства