Содержание
- 2. Основное содержание II начала термодинамики: - это закономерность, позволяющая решать вопросы о возможности протекания процессов, их
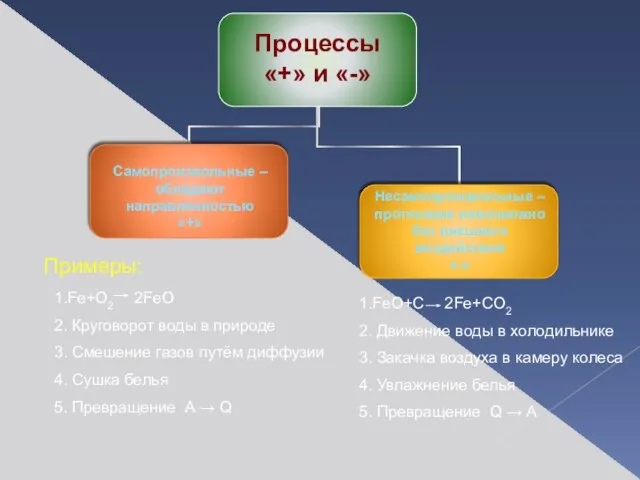
- 3. Примеры: 1.Fe+O2 2FeO 2. Круговорот воды в природе 3. Смешение газов путём диффузии 4. Сушка белья
- 4. Графическое изображение обратимого процесса (кривые прямого и обратного процессов совпадают) Графическое изображение необратимого процесса (кривые прямого
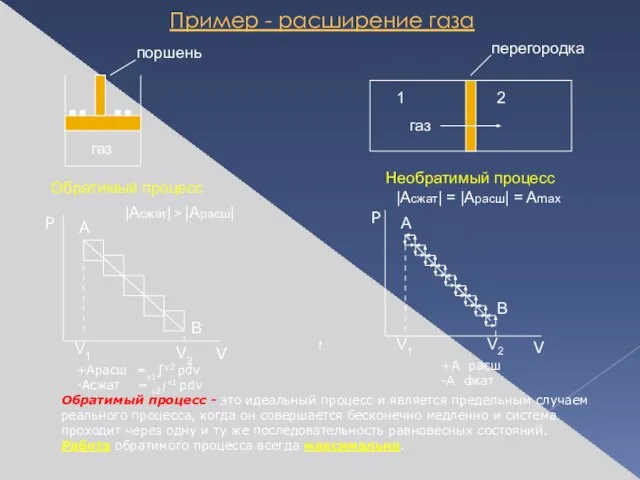
- 5. Пример - расширение газа Обратимый процесс Необратимый процесс |Асжат| > |Арасш| +Арасш =v1∫v2 pdv -Асжат =
- 6. Формулировки II начала термодинамики 1. «Тепло не может переходить от менее нагретого тела к более нагретому.
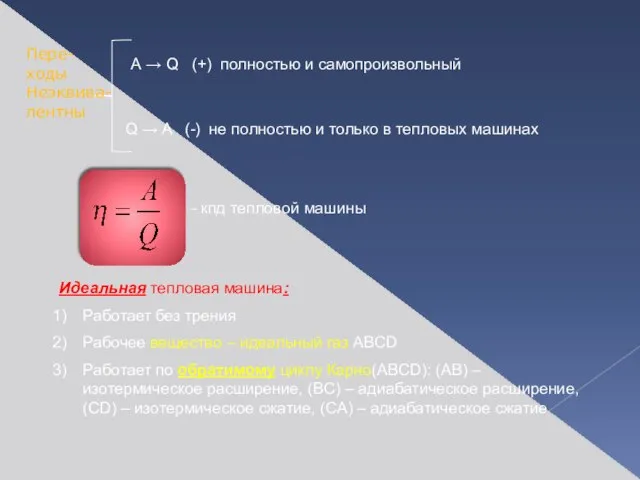
- 7. Идеальная тепловая машина: Работает без трения Рабочее вещество – идеальный газ ABCD Работает по обратимому циклу
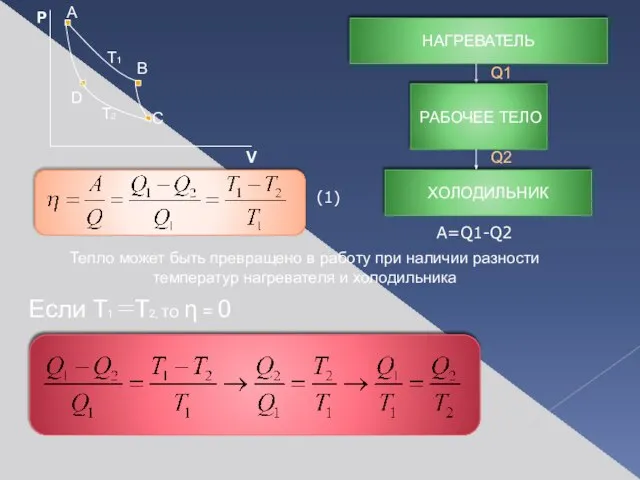
- 8. Тепло может быть превращено в работу при наличии разности температур нагревателя и холодильника Если T1 T2,
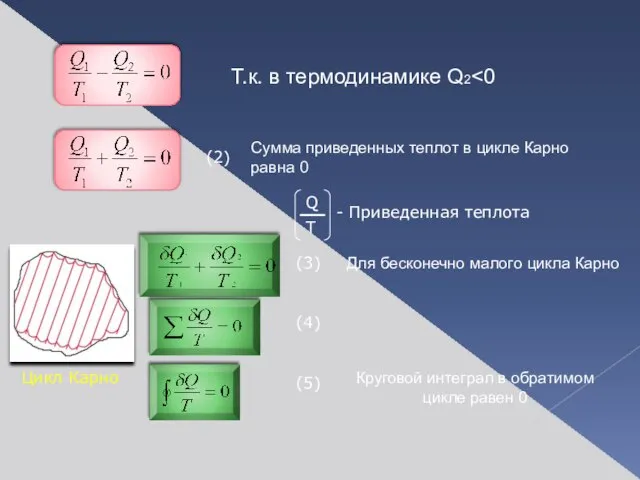
- 9. Т.к. в термодинамике Q2 Сумма приведенных теплот в цикле Карно равна 0 Круговой интеграл в обратимом
- 10. ТЕОРЕМА (в математике): Если интеграл по замкнутому контуру равен нулю, то подинтегральное выражение является полным дифференциалом
- 11. Условия равновесия в изолированных системах 1-2 самопроизвольный процесс 2 состояние равновесия 2-3 несамопроизвольный процесс
- 12. Реальные , в том числе наблюдаемые в природе, самопроизвольные процессы-необратимые, протекающие в направлении увеличения энтропии системы.
- 13. Энтропия и термодинамическая вероятность S – экстенсивный параметр Пример: n=10 книг(4 полки); W1=1260(N-общее число перестановок; Ni=число
- 14. Способы расчета изменения энтропии (для обратимых процессов) 1) Изотермический процесс (Т=const) I начало термодинамики II начало
- 16. Скачать презентацию








 Строение атомов, магнетизм микрочастиц, молекулярные спектры
Строение атомов, магнетизм микрочастиц, молекулярные спектры Презентация по физике "21-22. Двигатель внутреннего сгорания" - скачать бесплатно
Презентация по физике "21-22. Двигатель внутреннего сгорания" - скачать бесплатно Атомдардың рентгендік спектрі. (Лекция14)
Атомдардың рентгендік спектрі. (Лекция14) Презентация по физике "Развитие энергетики республики Башкортостан" - скачать
Презентация по физике "Развитие энергетики республики Башкортостан" - скачать  Законы электродинамики. Их физический смысл
Законы электродинамики. Их физический смысл Импульс.Закон сохранения импульса ФИЗИКА – 9 класс
Импульс.Закон сохранения импульса ФИЗИКА – 9 класс Движение в поле силы тяжести. Свободное падение
Движение в поле силы тяжести. Свободное падение Тематический проект «Виды теплообмена»
Тематический проект «Виды теплообмена»  Никель-кадмиевые аккумуляторные батареи
Никель-кадмиевые аккумуляторные батареи Разумное потребление батареек
Разумное потребление батареек Радиоактивность. Строение атома
Радиоактивность. Строение атома Өткен сабақты игеру барысын тексеру
Өткен сабақты игеру барысын тексеру Аналогии физических свойств сегнетоэлектрических и ферромагнитных кристаллов
Аналогии физических свойств сегнетоэлектрических и ферромагнитных кристаллов Контрольная работа по теме Кинематика
Контрольная работа по теме Кинематика Презентация по физике "Производство передача и использование электроэнергии" - скачать
Презентация по физике "Производство передача и использование электроэнергии" - скачать  Источники звука. Звуковые колебания
Источники звука. Звуковые колебания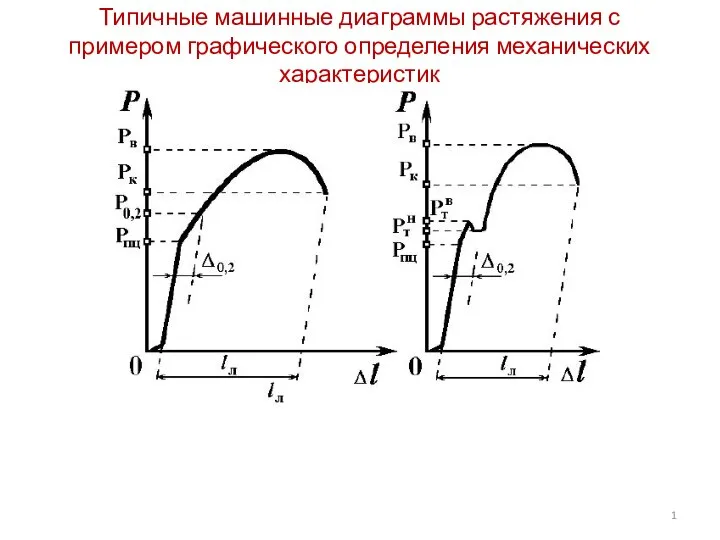 Типичные машинные диаграммы растяжения с примером графического определения механических характеристик
Типичные машинные диаграммы растяжения с примером графического определения механических характеристик Планетарная модель атома. Ядерная модель атома. Квантовые постулаты Бора
Планетарная модель атома. Ядерная модель атома. Квантовые постулаты Бора Оптика. Прохождение света через границу раздела двух сред. (Лекция 3)
Оптика. Прохождение света через границу раздела двух сред. (Лекция 3) Применение в фармацевтическом анализе рефрактометрии, поляриметрии, полярографии
Применение в фармацевтическом анализе рефрактометрии, поляриметрии, полярографии СВОБОДНЫЕ И ВЫНУЖДЕННЫЕ КОЛЕБАНИЯ. УСЛОВИЯ ВОЗНИКНОВЕНИЯ СВОБОДНЫХ КОЛЕБАНИЙ.
СВОБОДНЫЕ И ВЫНУЖДЕННЫЕ КОЛЕБАНИЯ. УСЛОВИЯ ВОЗНИКНОВЕНИЯ СВОБОДНЫХ КОЛЕБАНИЙ. Полевая геофизика. Магниторазведка (лекция 2 )
Полевая геофизика. Магниторазведка (лекция 2 ) Фазированные антенные решетки и их назначение. Задача адаптации в общем виде
Фазированные антенные решетки и их назначение. Задача адаптации в общем виде Основи гемодинаміки
Основи гемодинаміки Ауыстырмалы-төкпелі пункттардағы жүктерді тиеп-түсіру жұмыстарының технологиясы және механикалары
Ауыстырмалы-төкпелі пункттардағы жүктерді тиеп-түсіру жұмыстарының технологиясы және механикалары Презентация по физике "Радиоактивность в физике" - скачать
Презентация по физике "Радиоактивность в физике" - скачать  Електростатичне поле
Електростатичне поле  Проектирование системы обеспечения теплового режима космического полета
Проектирование системы обеспечения теплового режима космического полета