Содержание
- 2. Медико-биологическое значение темы Из остатков аминокислот построены такие важные соединения как белки, которые участвуют практически во
- 3. Некоторые аминокислоты являются лекарственными препаратами. Медико-биологическое значение темы
- 4. Медико-биологическое значение темы
- 5. Пептиды и белки построены из 20 α-аминокислот, информация о положении которых в белковой молекуле записана цифровым
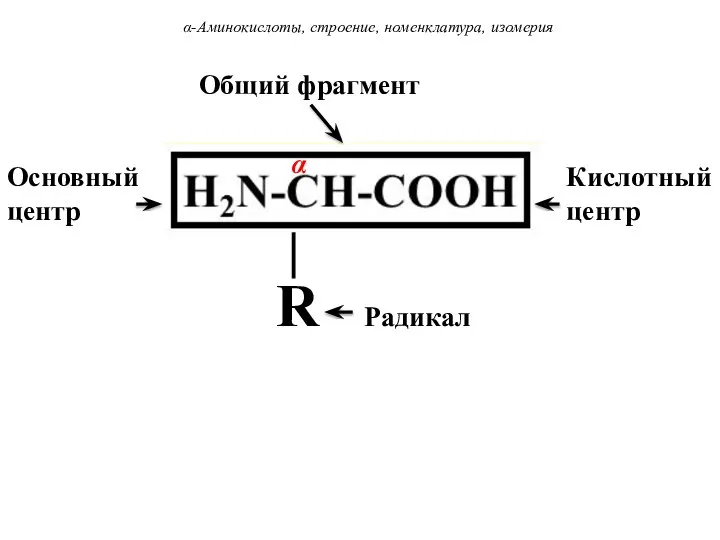
- 6. α-Аминокислоты, строение, номенклатура, изомерия Основный центр Кислотный центр Общий фрагмент ⏐ R Радикал α
- 7. α-Аминокислоты, строение, номенклатура, изомерия I. По строению углеводородного радикала α-аминокислоты делят на 7 групп: I. Моноаминомонокарбоновые
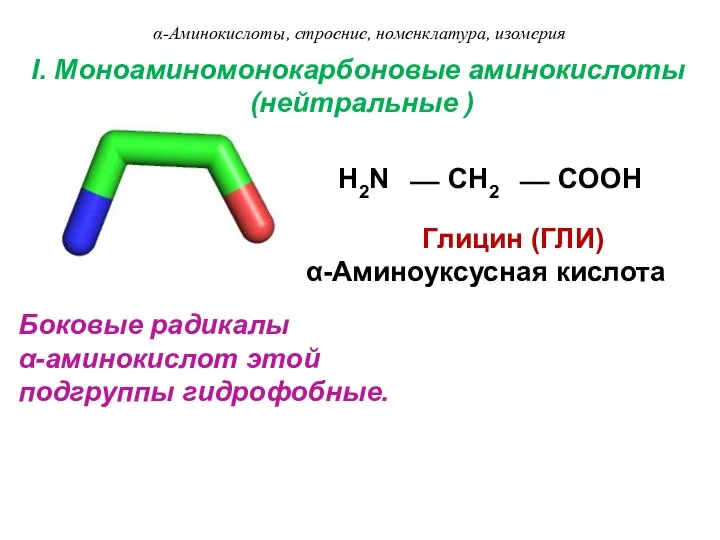
- 8. I. Моноаминомонокарбоновые аминокислоты (нейтральные ) H2N ⎯ CH2 ⎯ COOH Глицин (ГЛИ) α-Аминоуксусная кислота Боковые радикалы
- 9. Моноаминомонокарбоновые аминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH3 Аланин (АЛА) α-Аминопропионовая кислота
- 10. Моноаминомонокарбоновые аминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH ⎯ CH3 ⏐ CH3 Валин (ВАЛ) α-Амино-β-метилмасляная
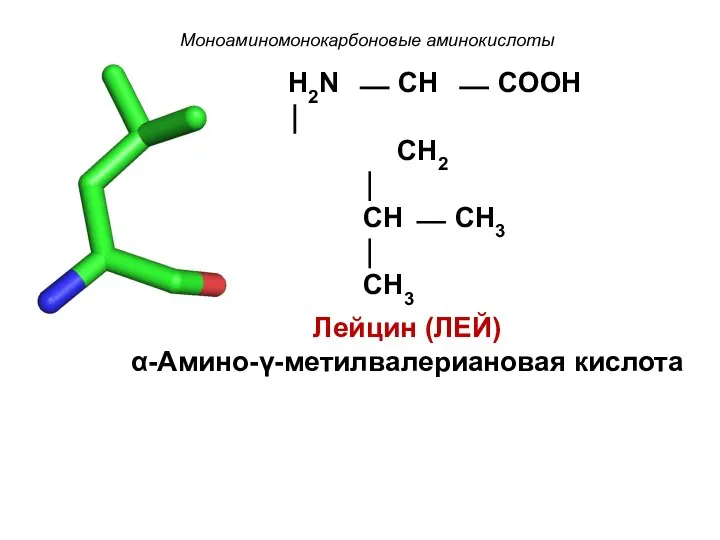
- 11. Моноаминомонокарбоновые аминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ CH ⎯ CH3 ⏐ CH3 Лейцин
- 12. Моноаминомонокарбоновые аминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH ⎯ CH3 ⏐ CH2 ⏐ CH3 Изолейцин
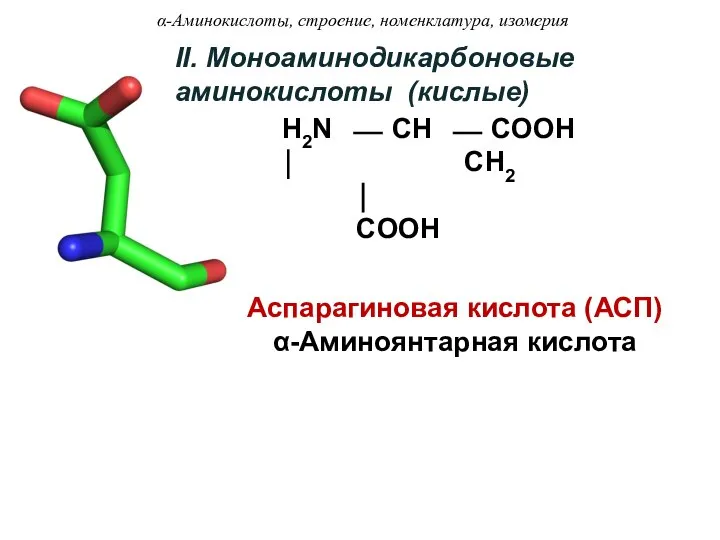
- 13. II. Моноаминодикарбоновые аминокислоты (кислые) H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ COOH Аспарагиновая кислота (АСП)
- 14. Моноаминодикарбоновые аминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ CH2 ⏐ COOH Глутаминовая кислота (ГЛУ)
- 15. Моноаминодикарбоновые аминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ CONH2 Аспарагин (АСН) В состав белков
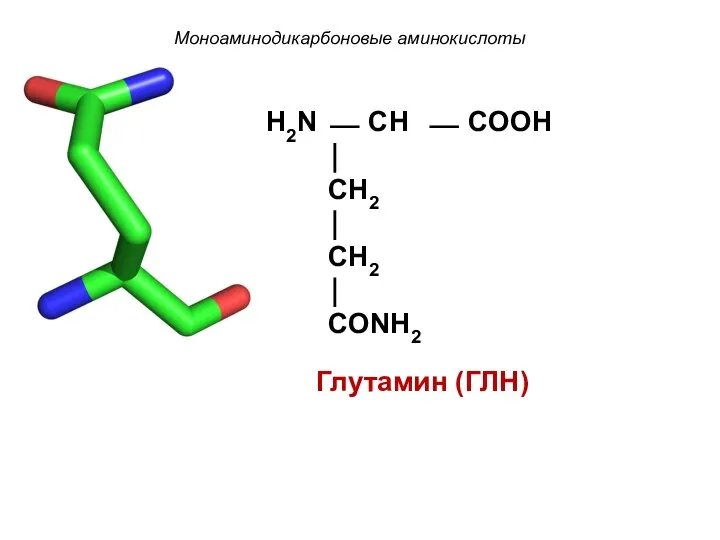
- 16. Моноаминодикарбоновые аминокислоты Глутамин (ГЛН) H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ CH2 ⏐ CONH2
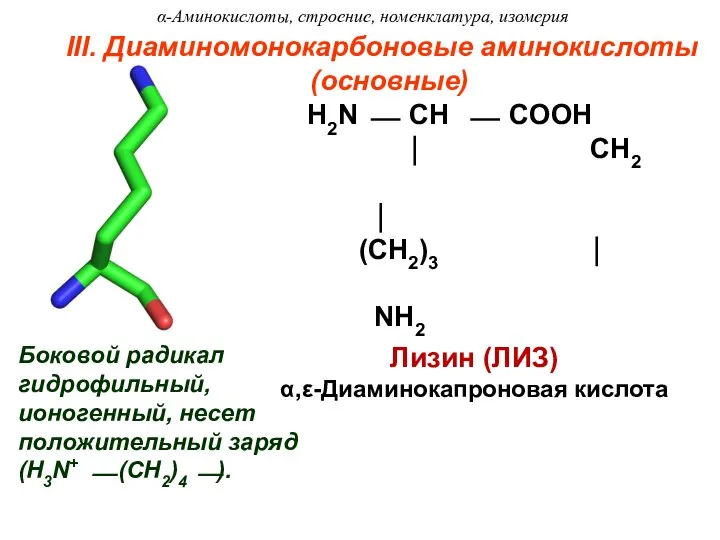
- 17. III. Диаминомонокарбоновые аминокислоты (основные) Лизин (ЛИЗ) α,ε-Диаминокапроновая кислота Боковой радикал гидрофильный, ионогенный, несет положительный заряд (H3N+
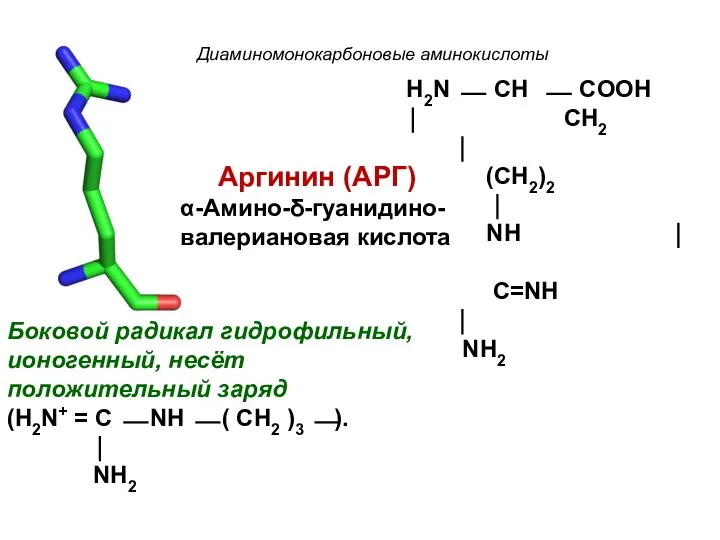
- 18. Диаминомонокарбоновые аминокислоты Аргинин (АРГ) α-Амино-δ-гуанидино- валериановая кислота Боковой радикал гидрофильный, ионогенный, несёт положительный заряд (H2N+ =
- 19. IV. Оксиаминокислоты Серин (СЕР) α-Амино-β-оксипропионовая кислота H2N ⎯ CH ⎯ COOH ⏐ CH2 ⎯ OH α-Аминокислоты,
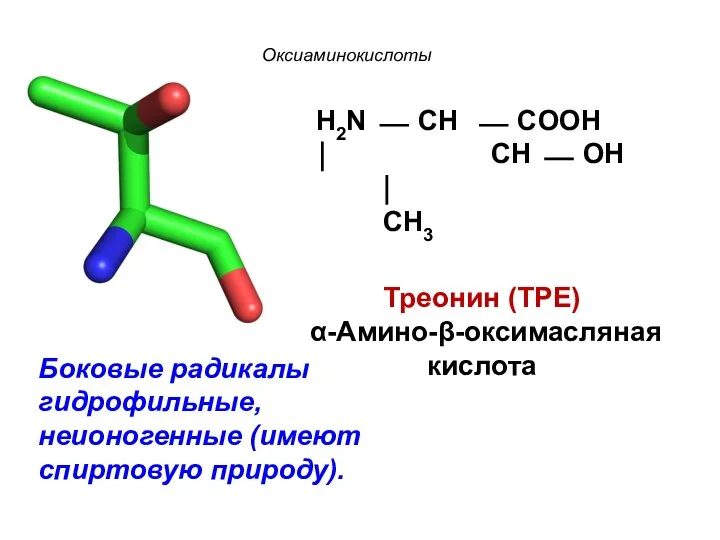
- 20. Оксиаминокислоты H2N ⎯ CH ⎯ COOH ⏐ CH ⎯ OH ⏐ CH3 Треонин (ТРЕ) α-Амино-β-оксимасляная кислота
- 21. V. Серосодержащие аминокислоты Боковой радикал гидрофильный, ионогенный, несёт отрицательный заряд (- S ⎯ CH2 ⎯). H2N
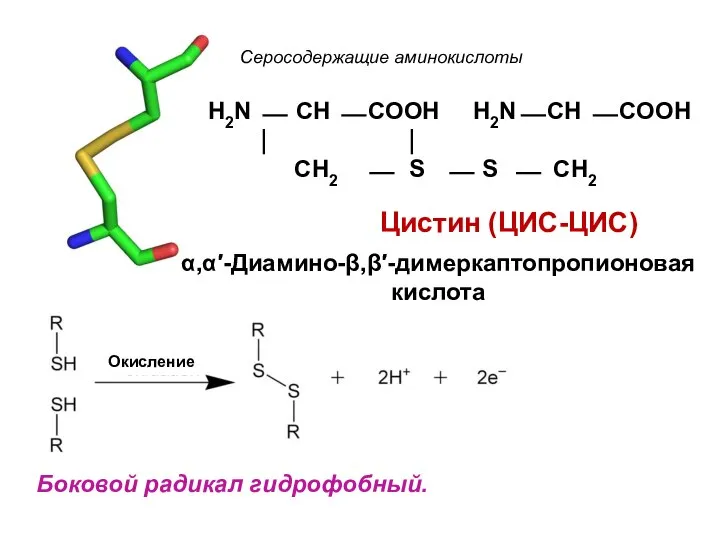
- 22. Окисление Боковой радикал гидрофобный. Серосодержащие аминокислоты Цистин (ЦИС-ЦИС) H2N ⎯ CH ⎯ COOH H2N⎯ CH ⎯
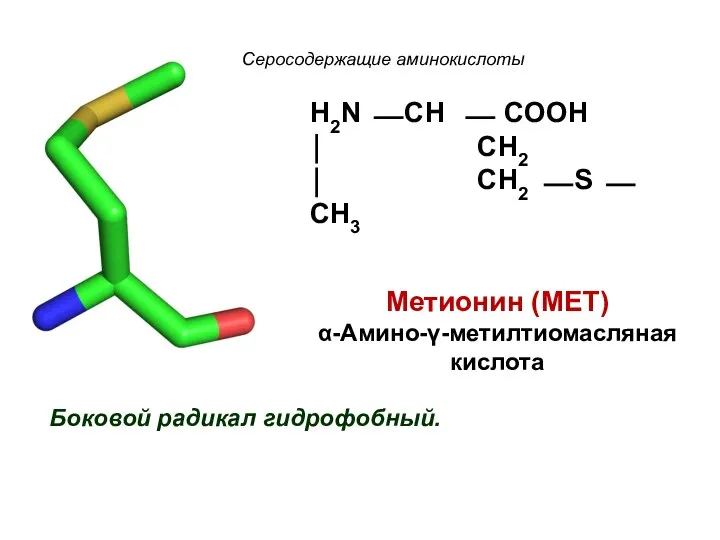
- 23. Серосодержащие аминокислоты Боковой радикал гидрофобный. H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ CH2 ⎯ S
- 24. Боковой радикал гидрофобный. Фенилаланин (Фен) α-Амино-β-фенилпропионовая кислота H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐ VI.
- 25. Ароматические α - аминокислоты Боковой радикал гидрофильный, ионогенный, несёт отрицательный заряд . α-Амино-β-параоксифенилпропионовая кислота H2N ⎯
- 26. Боковой радикал гидрофильный, ионогенный несёт положительный заряд ⏐ H -Амино-β-имидазолил- пропионовая кислота Гистидин (ГИС) H2N ⎯
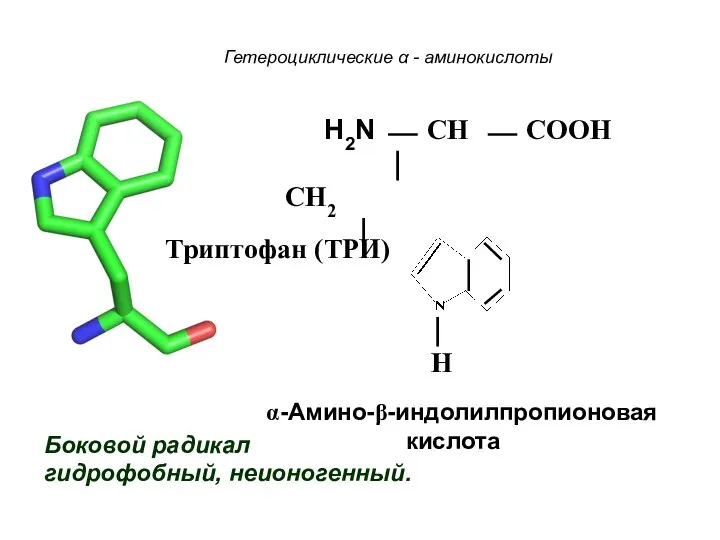
- 27. Гетероциклические α - аминокислоты Боковой радикал гидрофобный, неионогенный. H2N ⎯ CH ⎯ COOH ⏐ CH2 ⏐
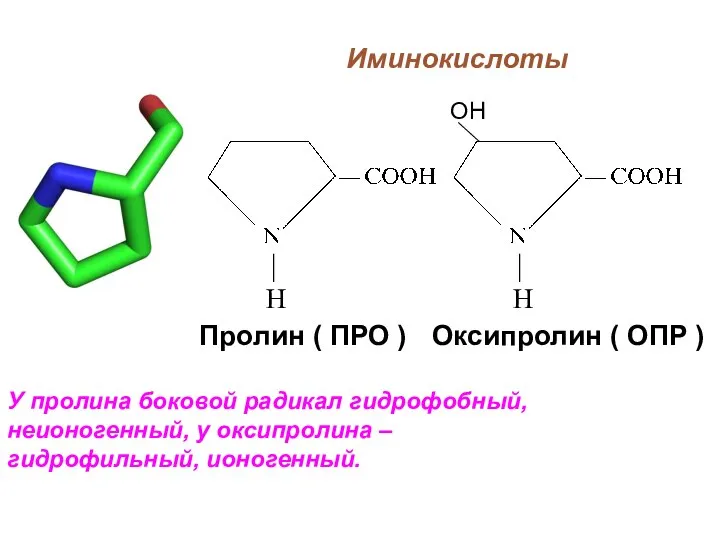
- 28. Иминокислоты У пролина боковой радикал гидрофобный, неионогенный, у оксипролина – гидрофильный, ионогенный. Пролин ( ПРО )
- 29. II. По способности синтезироваться в организме аминокислоты делятся на заменимые и незаменимые. α-Аминокислоты, строение, номенклатура, изомерия
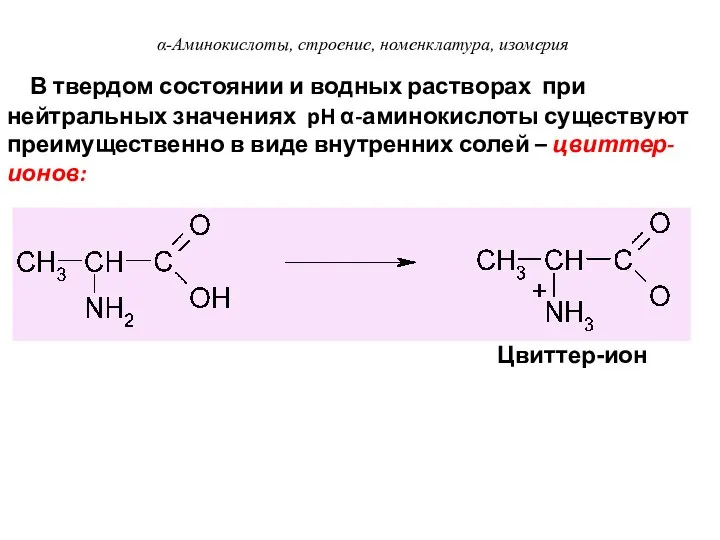
- 30. В твердом состоянии и водных растворах при нейтральных значениях pH α-аминокислоты существуют преимущественно в виде внутренних
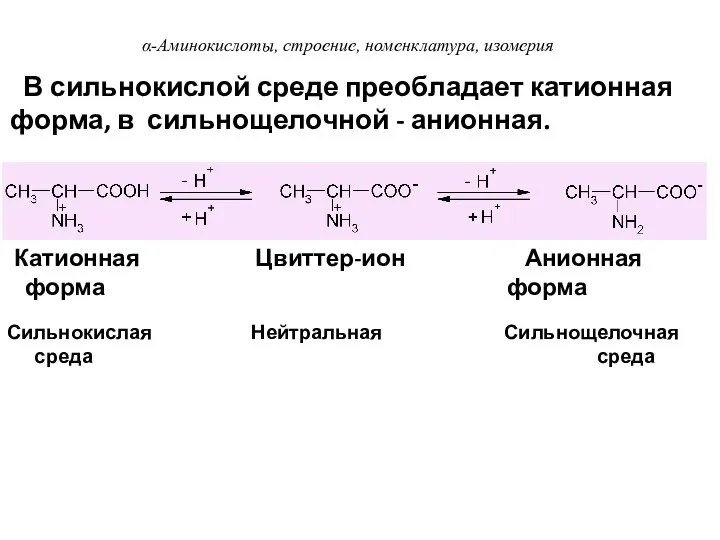
- 31. Сильнокислая Нейтральная Сильнощелочная среда среда В сильнокислой среде преобладает катионная форма, в сильнощелочной - анионная. Катионная
- 32. α-Аминокислоты, строение, номенклатура, изомерия Значение pH, при котором концентрация диполярных ионов максимальна, а минимальные концентрации катионных
- 33. α-Аминокислоты, строение, номенклатура, изомерия Для моноаминомонокарбоновых кислот pI ≈ 5-6, pI моноаминодикарбоновых кислот (Asp, Glu) ≈
- 34. α-Аминокислоты, строение, номенклатура, изомерия На этом основано разделение α-аминокислот методом электрофореза.
- 35. α-Аминокислоты, строение, номенклатура, изомерия In vivo при физиологических значения рН=7,34-7,36 α-аминокислоты и белки находятся в анионной
- 36. Номенклатура Названия α-аминокислот строятся по рациональной и заместительной номенклатуре ИЮПАК, но обычно используются их тривиальные названия:
- 37. Изомерия Структурная изомерия лейцин изолейцин аланин β-аланин
- 38. Стереоизомерия α - Аминокислоты - хиральные соединения, обладающие оптической активностью. Исключение составляет глицин: H2N ⎯ CH2
- 39. Стереоизомерия Относительная конфигурация α-аминокислот определяется по положению –NН2 группы у α-углеродного звена. Расположение аминогруппы слева соответствует
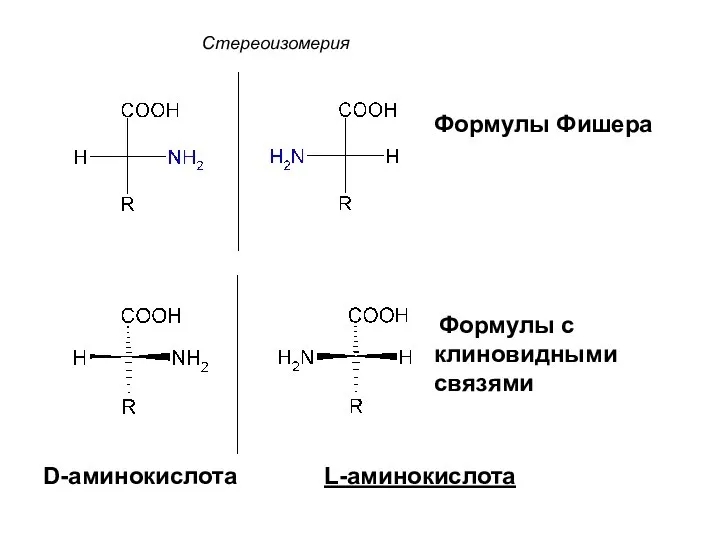
- 40. Стереоизомерия D-аминокислота L-аминокислота Формулы Фишера Формулы с клиновидными связями
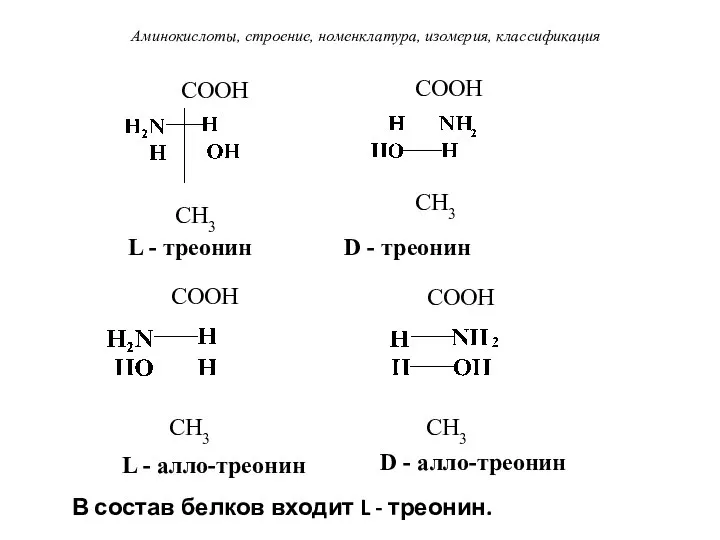
- 41. Аминокислоты, строение, номенклатура, изомерия, классификация CH3 COOH CH3 L - треонин D - треонин COOH COOH
- 42. Физические свойства α-Аминокислоты - кристаллические вещества. Имеют высокие температуры плавления (выше 200° С), нелетучие, растворимые в
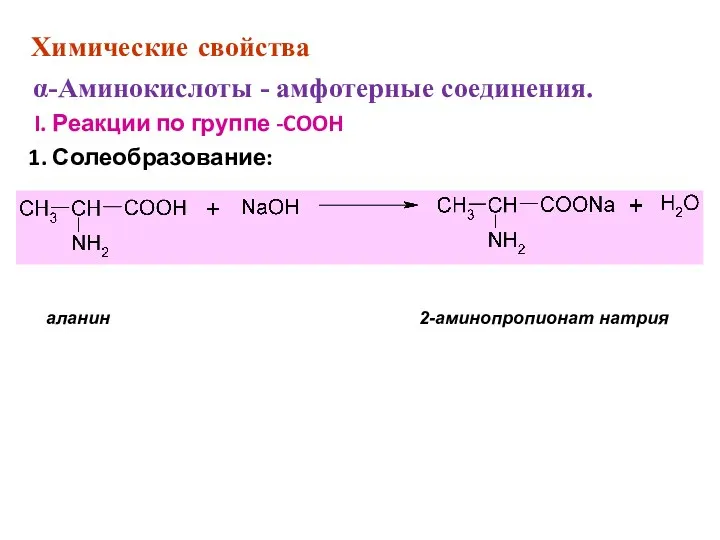
- 43. Химические свойства α-Аминокислоты - амфотерные соединения. I. Реакции по группе -COOH 1. Солеобразование: аланин 2-аминопропионат натрия
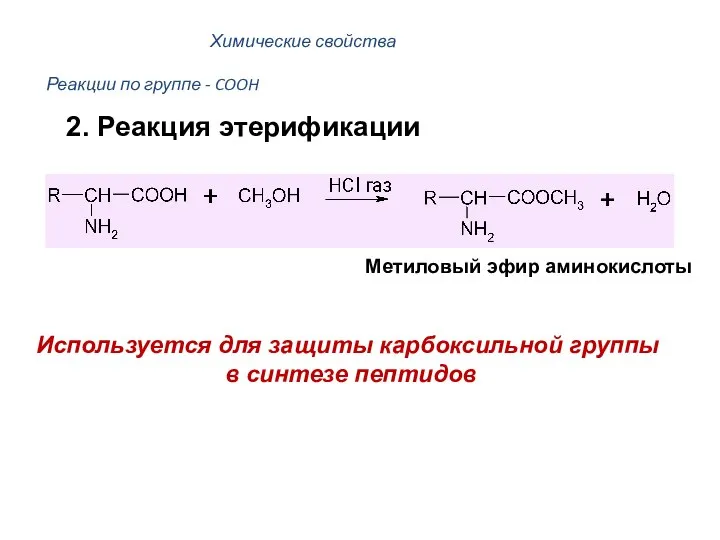
- 44. Реакции по группе - COOH Метиловый эфир аминокислоты Используется для защиты карбоксильной группы в синтезе пептидов
- 45. Химические свойства II. Реакции по группе –NH2: 1. Солеобразование аланин гидрохлорид аланина
- 46. Взаимодействие с Cu(OH)2 Хелатная соль меди Химические свойства Реакции по группе –NH2:
- 47. Реакции по аминогруппе 2.Ацилирование Хлористый ацетил (Ацетилхлорид) N-ацетиламинокислота ацетил Химические свойства
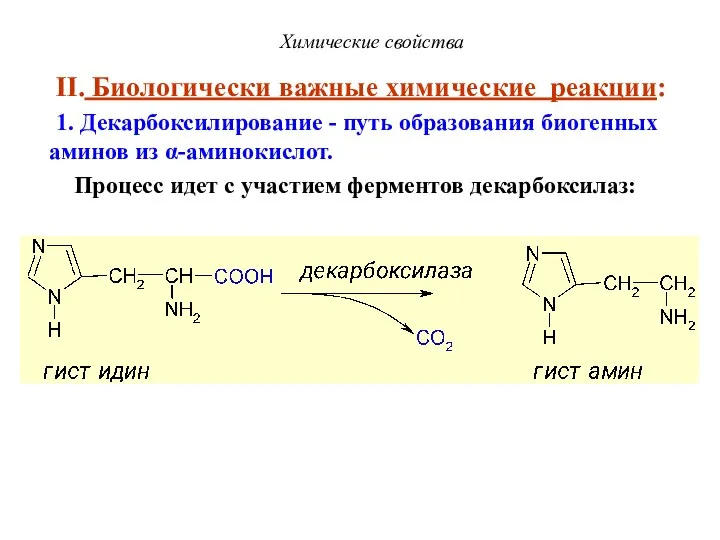
- 48. Химические свойства II. Биологически важные химические реакции: 1. Декарбоксилирование - путь образования биогенных аминов из α-аминокислот.
- 49. Декарбоксилирование Химические свойства
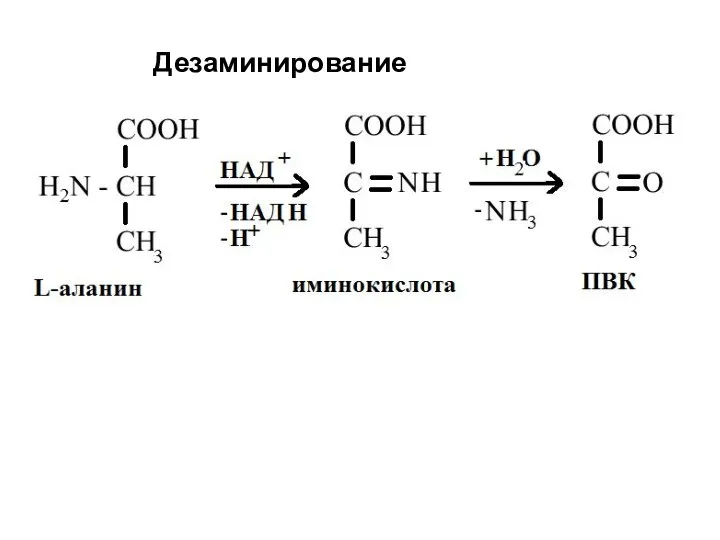
- 50. 2. Дезаминирование - это реакция удаления аминогруппы путем окислительного, восстановительного, гидролитического или внутримолекулярного дезаминирования. В организме
- 51. Окислительное дезаминирование in vivo иминокислота кетокислота Химические свойства На первой стадии процесса происходит дегидрирование α-звена с
- 52. Дезаминирование
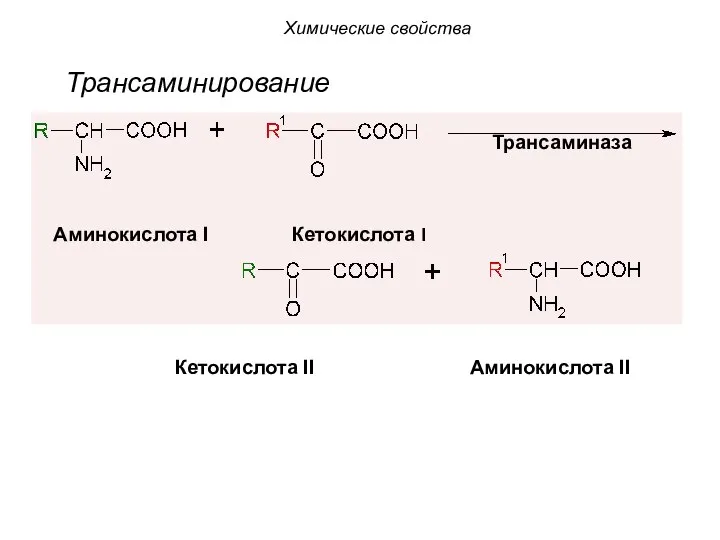
- 53. 3. Трансаминирование (переаминирование) - это путь синтеза необходимых α-аминокислот из α-кетонокислот. При этом донором аминогруппы является
- 54. Трансаминирование Аминокислота I Кетокислота I Кетокислота II Аминокислота II Трансаминаза Химические свойства
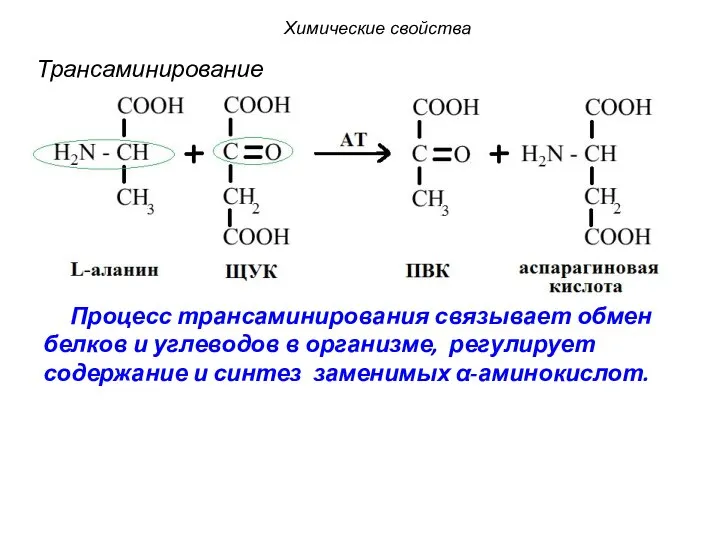
- 55. Процесс трансаминирования связывает обмен белков и углеводов в организме, регулирует содержание и синтез заменимых α-аминокислот. Трансаминирование
- 56. Пептиды и белки Пептиды (греч. πεπτος — питательный) и белки - биополимеры, построенные из α-аминокислот. Пептиды
- 57. Функции белков 1. Ферментативная 2. Структурная 3. Питательная 4. Защитная функция 5. Транспортная 6. Регуляторная 7.
- 58. Классификация пептидов и белков II. По составу белки делят на простые (неконъюгированные) и сложные (конъюгированные). Сложные
- 59. Схема образования пептидов Пептидная связь дипептид Пептиды и белки
- 60. Треонин Фенилаланин Тирозин Треонил-Фенилаланил-Тирозин Образование пептидов
- 61. Пептиды и белки Названия пептидов строятся путём последовательного перечисления аминокислотных остатков, начиная с N-конца, с добавлением
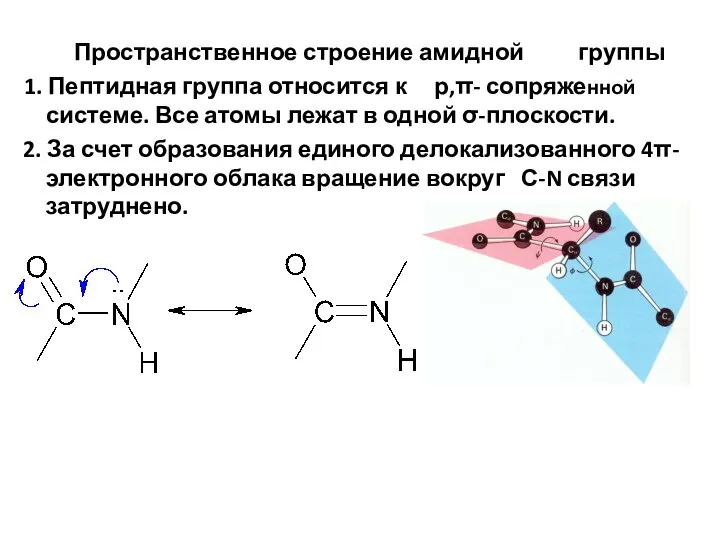
- 62. Пространственное строение амидной группы 1. Пептидная группа относится к р,π- сопряженной системе. Все атомы лежат в
- 63. Глицил-лизил-тирозин Трипептид N-конец С-конец метиновый мостик
- 64. Глутамил-аланил-цистеин Трипептид: Пептиды и белки
- 65. Изоэлектрическая точка белка (pI) Молекула белка имеет электрический заряд. В нейтральной среде заряд белковой молекулы определяется
- 66. Изоэлектрическая точка белка (pI) Схематично диссоциацию (с учетом гидратации) можно представить в виде: COOH COOH COO-
- 67. Изоэлектрическая точка белка Чем больше –COOH, –OH, –SH групп, тем выше отрицательный заряд, и белок будет
- 68. I. Аминокислоты, пептиды и белки являются амфотерными соединениями, содержащими и кислотные группы (–COOH) и оснóвные группы
- 69. Химические свойства II. По месту пептидных связей молекулы белков гидролизуются: а) in vivo с участием ферментов
- 70. Химические свойства пептидов и белков б) Гидролиз in vitro происходит в сильнокислой или сильнощелочной среде и
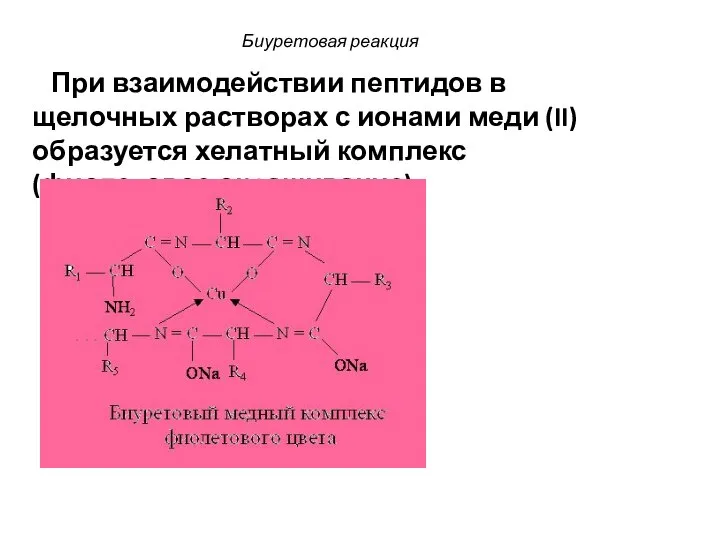
- 71. Биуретовая реакция В реакцию вступают все пептиды и белки, содержащие не менее двух пептидных связей. Реактив
- 72. Биуретовая реакция Биурет образуется из мочевины при медленном нагревании до температуры 150 - 160° С. O
- 73. Биуретовая реакция При взаимодействии пептидов в щелочных растворах с ионами меди (II) образуется хелатный комплекс (фиолетовое
- 74. Нингидринная реакция на α - аминокислоты Реактив - нингидрин. Продукт реакции имеет сине-фиолетовый цвет. Химические свойства
- 75. Ксантопротеиновая реакция Определяет присутствие в белке ароматических и гетероциклических α - аминокислот: триптофана, фенилаланина, тирозина, гистидина.
- 76. Ксантопротеиновая реакция Реактив: конц. HNO3 Образуется нитросоединение, окрашенное в желтый цвет. При добавлении к нему щёлочи
- 77. Реакция Миллона на тирозин Реактив Миллона: раствор HgNO3 и Hg(NO2)2 в разбавленной HNO3, содержащей примесь HNO2.
- 78. Реакция Миллона Реактив Миллона взаимодействует с тирозином с образованием ртутной соли нитропроизводного тирозина, окрашенной в розовато-красный
- 79. Реакция Фоля Это реакция на цистеин и цистин. Химические свойства пептидов и белков
- 80. Реакция Фоля При щелочном гидролизе цистеина или цистина образуется сероводород, который, реагируя со щелочью, дает сульфиды
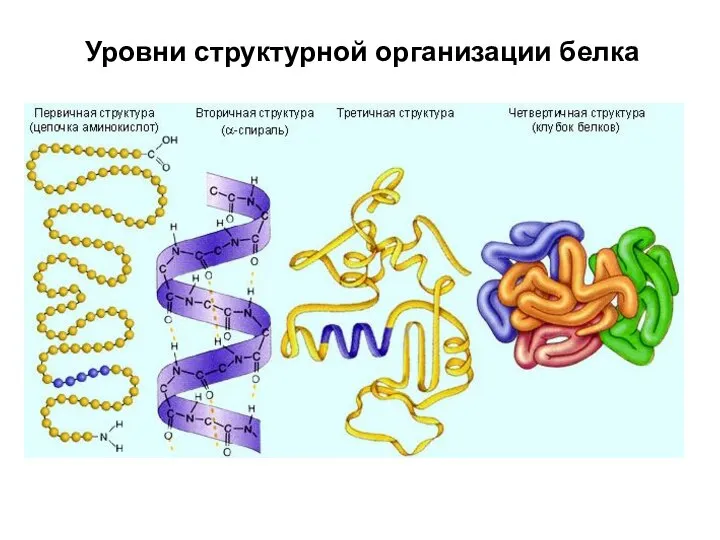
- 81. Уровни структурной организации белка
- 82. Первичная структура NH2-Tyr-Pro-Lys-Gly-Phe-Tyr-Lys-COOH. Первичная структура определяет уровни структурной организации белка. Первичная структура – последовательность аминокислотных остатков
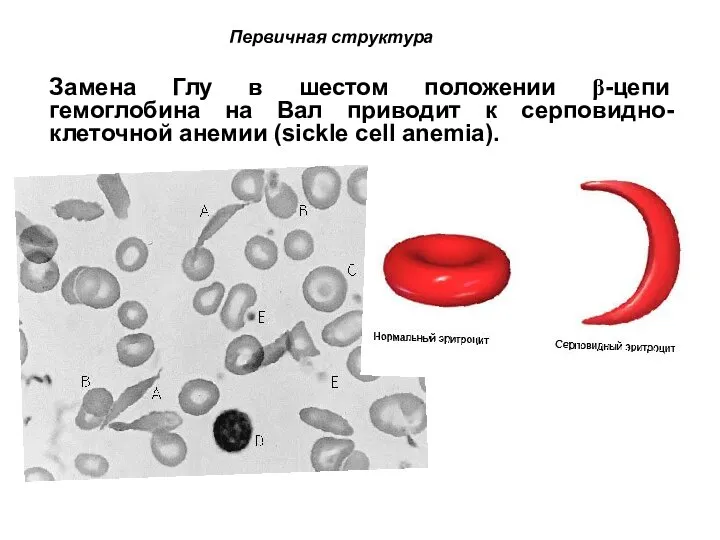
- 83. Замена Глу в шестом положении β-цепи гемоглобина на Вал приводит к серповидно-клеточной анемии (sickle cell anemia).
- 84. 20 аминокислот могут дать примерно 100000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000 белков. Это астрономическое число – число гугол умноженное на число
- 85. Вторичная структура Вторичная структура - локальные высокоупорядоченные конформации белковой цепи – спирали и складчатые слои. Примеры:
- 86. Правые α-спирали в полипептидной цепи стабилизируются водородными связями. Вторичная структура
- 87. Вторичная структура также стабилизуется дисульфидными мостиками по месту цистеиновых остатков. Вторичная структура
- 88. Водородные связи в α-спиралях -Вал-Фен-Тир-Ала-Лей- Первый Второй Третий Четвёртый Остатки АК: α-спираль – 413 спираль: остаток
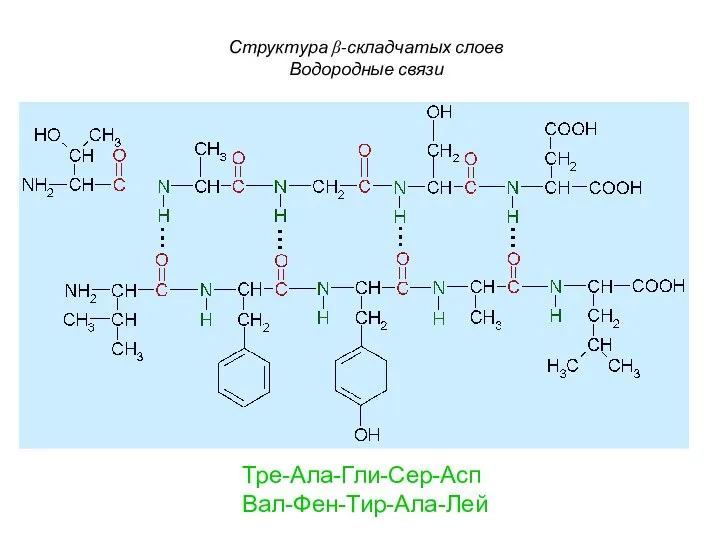
- 89. Структура β-складчатых слоев β-Структура образуется из нескольких полипептидых цепей связанных водородными связями.
- 90. Структура β-складчатых слоев Водородные связи Тре-Ала-Гли-Сер-Асп Вал-Фен-Тир-Ала-Лей
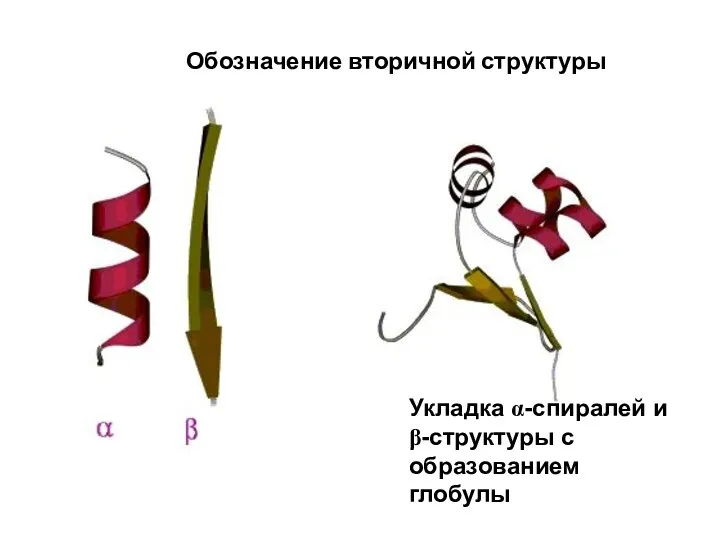
- 91. Обозначение вторичной структуры Укладка α-спиралей и β-структуры с образованием глобулы
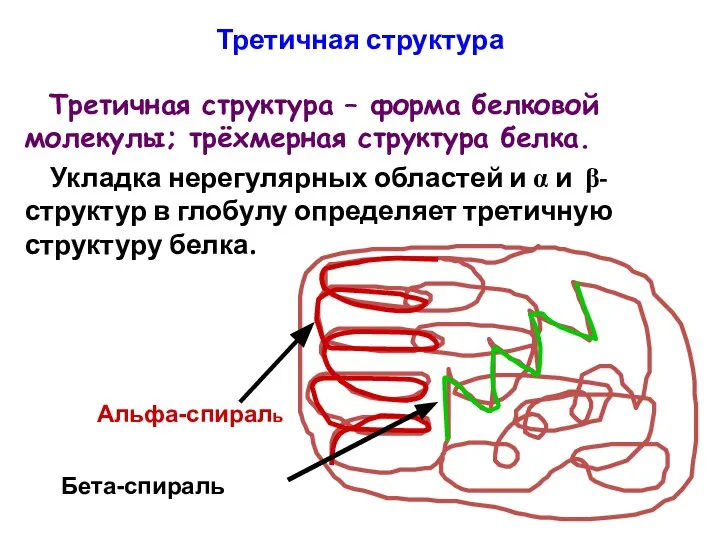
- 92. Третичная структура Третичная структура – форма белковой молекулы; трёхмерная структура белка. Укладка нерегулярных областей и α
- 93. Третичная структура α-Аминокислоты в белковой глобуле взаимодействуют за счёт: Ковалентных связей (дисульфидные –S–S– связи в цистине)
- 94. Уровни структурной организации белка
- 95. Дисульфидные связи в цистине
- 96. Дисульфидные связи Структура лизоцима. Дисульфидные связи показаны пунктиром
- 97. Ионные связи Асп Лиз
- 98. Третичная структура По третичной структуре белки делят на: глобулярные - для них характерна α-спиральная структура (яичный
- 99. Пептиды и белки Глобулярные белки выполняют функции, требующие подвижности и, следовательно, растворимости. Они участвуют в регуляции
- 100. Пептиды и белки Фибриллярные белки нерастворимы, склонны к образованию волокон и потому служат основным строительным материалом
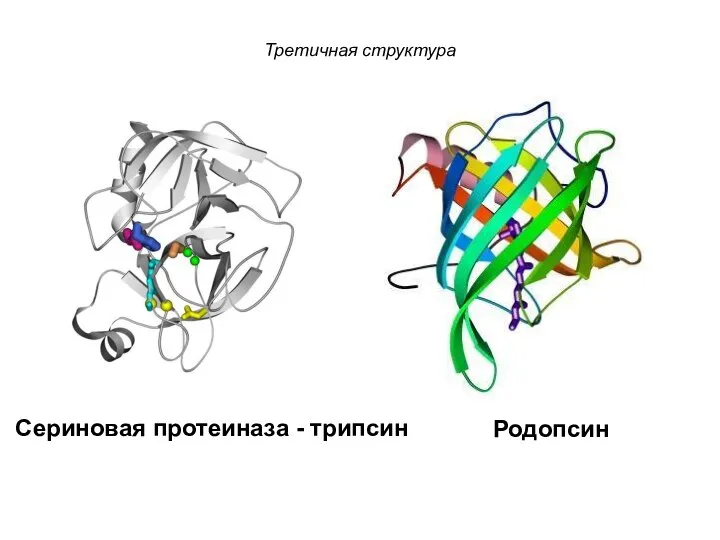
- 101. Третичная структура Сериновая протеиназа - трипсин Родопсин
- 102. Третичная структура Ацилтрансфераза (КФ 2.3) Пиктатлиаза С
- 103. Третичная структура Митохондриальная супероксиддисмутаза (КФ 1.15.1.1)
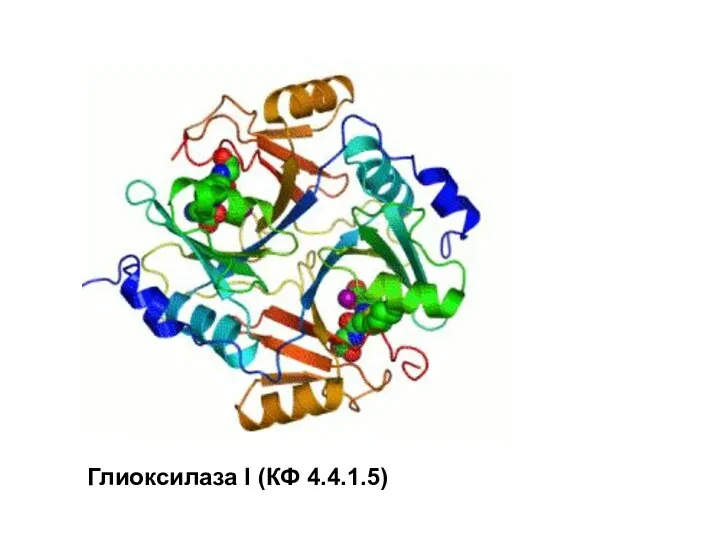
- 104. Figura 4: Cofactores Глиоксилаза I (КФ 4.4.1.5)
- 105. Цитохром C
- 106. Третичная структура α− и β−цепи гемоглобина лошади
- 107. Третичная структура Параллельные β-слои карбоангидразы Антипараллельные β-слои лектина
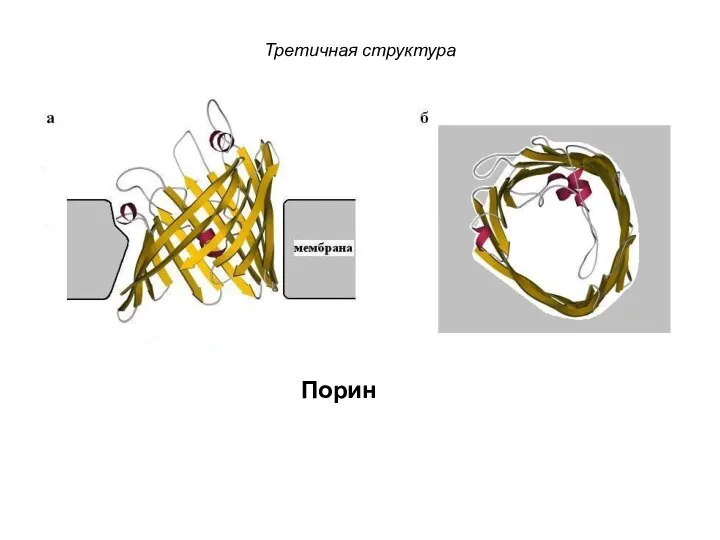
- 108. Третичная структура Порин
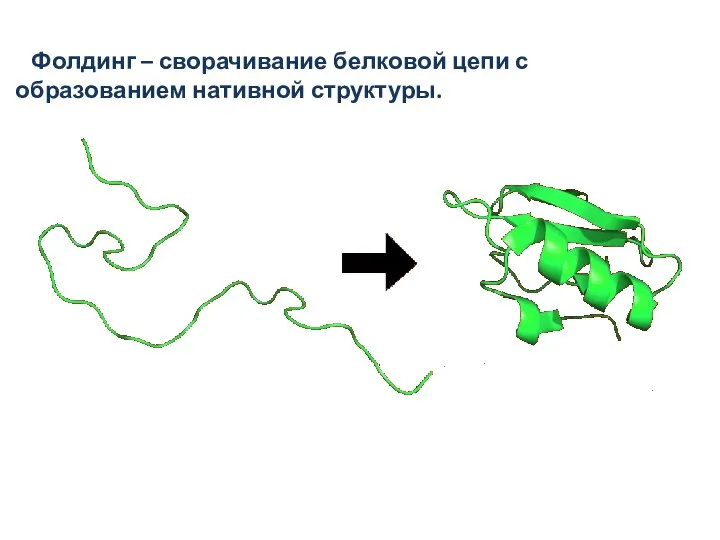
- 109. Фолдинг – сворачивание белковой цепи с образованием нативной структуры.
- 110. Две нативные конформации лимфотактина
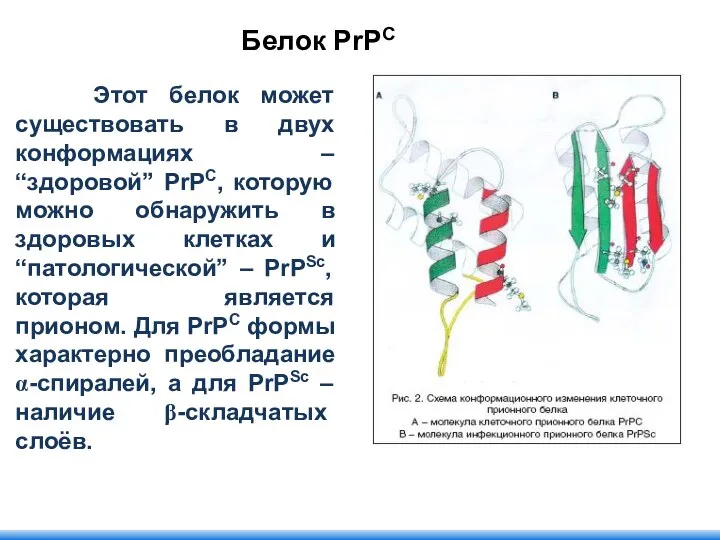
- 111. Этот белок может существовать в двух конформациях – “здоровой” PrPC, которую можно обнаружить в здоровых клетках
- 112. Болезнь Крейтцфельда-Якоба Новый вариант Крейцфельда-Якоба – коровье бешенство Болезнь Герстманна–Штройсслера Летальная семейная инсомния, куру Абориген с
- 113. Домены Домены – глобулярные области в пределах одной белковой молекулы. Домены соединены шарнирным участком. Доменная структура
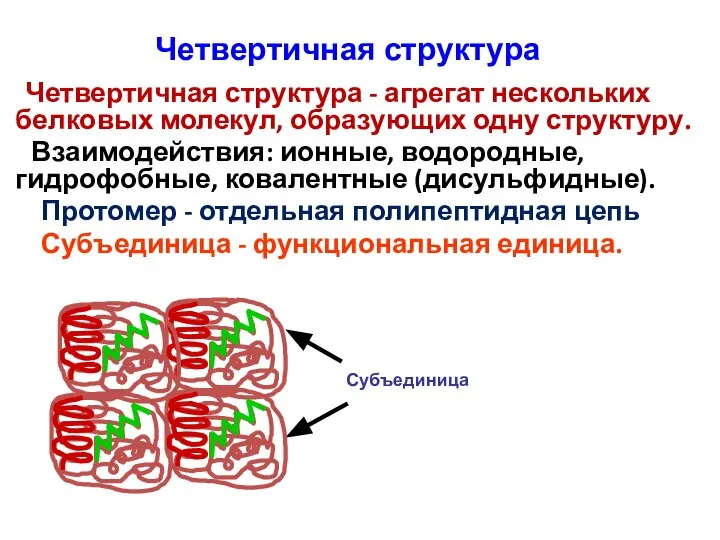
- 114. Четвертичная структура Четвертичная структура - агрегат нескольких белковых молекул, образующих одну структуру. Взаимодействия: ионные, водородные, гидрофобные,
- 115. Молекула гемоглобина состоит из 4-х субъединиц, каждая из которых включает в себя активный центр – гем.
- 116. Дисульфидные связи Дисульфидные связи в иммуноглобулине G
- 117. Четвертичная структура Лактатдегидрогеназа (КФ 1.1.1.27) Фермент состоит из полипептидных цепей двух типов — М (от англ.
- 118. Четвертичная структура Пример четвертичной структуры - вирус табачной мозаики: 2130 одинаковых молекул белка расположены вокруг РНК
- 119. Вопросы для самоконтроля Приведите классификацию α-аминокислот в зависимости от характера радикала. Охарактеризуйте химические свойства α-аминокислот. Перечислите
- 121. Скачать презентацию


















































































 Вирощування кристалів в додомашніх умовах
Вирощування кристалів в додомашніх умовах Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине
Практическая работа. Решение экспериментальных задач по теме «Подгруппа кислорода» Цель: используя знания о свойствах соедине Определение валентности элементов
Определение валентности элементов V група періодичної системи Менделєєва
V група періодичної системи Менделєєва Процессы в растворах: электролитическая диссоциация (ЭД)
Процессы в растворах: электролитическая диссоциация (ЭД) Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады)
Решение задач по химии (ОГЭ, ЕГЭ, Олимпиады) Альдегидтер және кетондар
Альдегидтер және кетондар Кристаллические решетки
Кристаллические решетки Получение и установление состава кристаллогидрата фосфата цинка
Получение и установление состава кристаллогидрата фосфата цинка Взаимодействие элементов-неметаллов между собой. 8 класс
Взаимодействие элементов-неметаллов между собой. 8 класс Теоретические основы органической химии
Теоретические основы органической химии Железо и его соединения.
Железо и его соединения. Beryllium. The physical properties of beryllium
Beryllium. The physical properties of beryllium Физический процесс и химическая реакция.
Физический процесс и химическая реакция. Общая и неорганическая химия
Общая и неорганическая химия Химические свойства алканов
Химические свойства алканов Расчёт равновесного состава
Расчёт равновесного состава Викторина. Дмитрий Иванович Менделеев
Викторина. Дмитрий Иванович Менделеев Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары
Металдар мен бейметалдардың табиғатта таралуы. ҚР-дағы кен орындары Уран. Получение урана
Уран. Получение урана Значение основных химических элементов в жизни человека
Значение основных химических элементов в жизни человека Сведения о воде
Сведения о воде Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs
Речь без пословицы - всё равно что еда без соли Речь без пословицы - всё равно что еда без соли · Пуд соли съешь, прежде чем познаешь человека · &nbs Буровые технологические жидкости для бурения и крепления горизонтальных скважин
Буровые технологические жидкости для бурения и крепления горизонтальных скважин Имеет ли вода форму
Имеет ли вода форму Методы хроматографии. Ионообменная хроматография
Методы хроматографии. Ионообменная хроматография Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Кислород. Получение кислорода и его физические свойства
Кислород. Получение кислорода и его физические свойства