Содержание
- 2. Распространенность 6я группа главная подгруппа содержит элементы: О S Se Te На долю кислорода приходится около
- 3. Химические свойства кислорода О – второй по электроотрицательности элемент. С большинством металлов О реагирует при комнатной
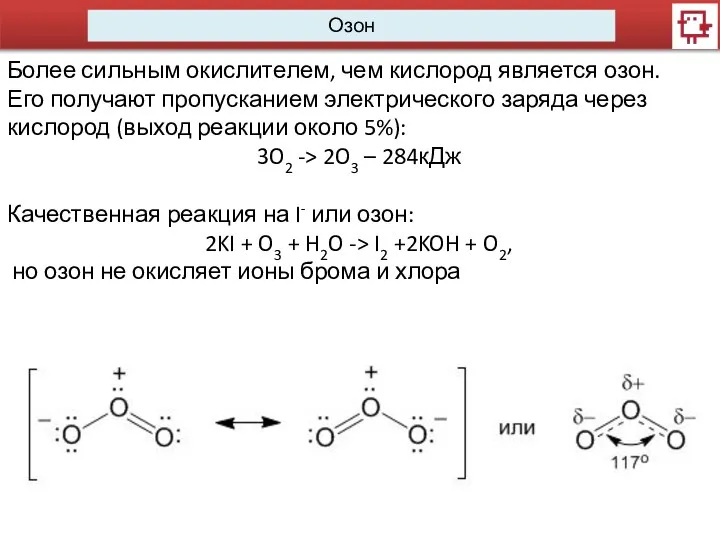
- 4. Озон Более сильным окислителем, чем кислород является озон. Его получают пропусканием электрического заряда через кислород (выход
- 5. Получение В промышленности получают: Фракционной перегонкой жидкого воздуха (разность температур конденсации) Электролизом воды В лаборатории: 2KMnO4
- 6. Сера При комнатной температуре сера реагирует со фтором, хлором и концентрированными кислотами-окислителями (HNO3, H2SO4): S +
- 7. Сероводород Сероводород – бесцветный и очень токсичный газ с запахом тухлых яиц. Получение в лаборатории: FeS
- 8. Сернистый газ. Сернистая кислота SO2 + H2O H2SO3 Сернистый газ можно получить при взаимодействии: Me +
- 10. Скачать презентацию






 Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3
Каталитическое жидкофазное окисление глюкозы в глюконовую кислоту в присутствии катализаторов Pd-Sn/Al2O3 Связь ЭДС с составом фаз. Вывод из межфазных равновесий
Связь ЭДС с составом фаз. Вывод из межфазных равновесий Углеводы. Сукралоза
Углеводы. Сукралоза Оксиды азота
Оксиды азота Предмет химии. Основные задачи курса
Предмет химии. Основные задачи курса Способы определения УЭС пластовой воды
Способы определения УЭС пластовой воды Требования, предъявляемые к дизельным топливам
Требования, предъявляемые к дизельным топливам Марганец и его свойства
Марганец и его свойства Реакции ионного обмена. Теория химического строения органических соединений. 9 класс
Реакции ионного обмена. Теория химического строения органических соединений. 9 класс Презентация по Химии "Первичная переработка нефти" - скачать смотреть бесплатно
Презентация по Химии "Первичная переработка нефти" - скачать смотреть бесплатно лекарства Урок-защита проектов Разработала учитель химии МОУ «Гимназия №1» г. Саратова Шишкина И.Ю.
лекарства Урок-защита проектов Разработала учитель химии МОУ «Гимназия №1» г. Саратова Шишкина И.Ю.  Титан. Металл XXI века
Титан. Металл XXI века Фосфор, его физические и химические свойства
Фосфор, его физические и химические свойства Acizii nucleici
Acizii nucleici Буферные системы. Классификация буферных растворов
Буферные системы. Классификация буферных растворов Процессы горения. Способы сжигания топлива. Горелочные устройства
Процессы горения. Способы сжигания топлива. Горелочные устройства Предельные углеводороды. Алканы
Предельные углеводороды. Алканы Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія
Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія  Эволюция понятия “валентность”
Эволюция понятия “валентность” Химия. Химиялық термодинамика
Химия. Химиялық термодинамика Биотрансформация ядов
Биотрансформация ядов Роль хімічних знань у пізнанні природи
Роль хімічних знань у пізнанні природи Дисперсные системы. Авторы презентации: ученицы 11А класса МБОУ СОШ № 131 г.Новосибирска Галактионова Анастасия и Краскова Е
Дисперсные системы. Авторы презентации: ученицы 11А класса МБОУ СОШ № 131 г.Новосибирска Галактионова Анастасия и Краскова Е Аллотропные модификации углерода
Аллотропные модификации углерода Углеводородное сырье: способы переработки
Углеводородное сырье: способы переработки Задачи по химии
Задачи по химии Поверхностное натяжение
Поверхностное натяжение Серебра нитрат и другие препараты серебра. Ртути окись желтая
Серебра нитрат и другие препараты серебра. Ртути окись желтая