Содержание
- 2. 1. В главных подгруппах периодической системы химических элементов с увеличением заряда ядер не изменяется Радиус атома;
- 3. 2. Наиболее выраженные неметаллические свойства среди элементов 2- го периода периодической системы Бор; Углерод; Азот; Кислород.
- 4. 3. В периодах периодической системы химических элементов с увеличением заряда ядер не изменяется Масса атома; Число
- 5. 4. Наиболее сильно выраженные металлические свойства среди элементов 2-го периода периодической системы проявляет Бор; Бериллий; Углерод;
- 6. 5. Наиболее выражены металлические свойства у Кремния; Натрия; Алюминия; Магния.
- 7. 6. Ряд чисел 2,8,5 соответствует распределению электронов по энергетическим уровням атома Алюминия; Азота; Фосфора; Хлора.
- 8. 7. Электронная формула внешнего энергетического уровня 2s22p4 соответствует атому Серы; Углерода; Кремния; Кислорода.
- 9. 8. Четыре электрона на внешнем энергетическом уровне имеет атом Гелия; Бериллия; Углерода; Кислорода.
- 10. 9. Электронная формула атома углерода 1s22s22p6; 1s22s22p4; 1s22s2; 1s22s22p2.
- 11. 10. Химический знак элемента, электронная формула атома которого 1s22s22p63s23p4, O; S; Cl; F.
- 12. Ты ответил правильно Молодец!!!
- 13. Правильно. Ты сегодня на высоте
- 14. Это верный ответ. Умничка
- 15. Ты ответил на вопрос! Молодец!!!
- 16. Неправильно Попробуй еще раз
- 17. Правильно. У фосфора всего 15 электронов.
- 18. Правильно. Электронная формула атома кислорода: 1s22s22p4
- 19. Правильно. Атом углерода на внешнем энергетическом уровне имеет 4 электрона
- 20. Правильно. Электронная формула атома углерода 1s22s22p2.
- 21. Правильно. Электронная формула серы 1s22s22p63s23p4
- 22. Правильно. Среди предложенных элементов у натрия наименьшее количество электронов на внешнем энергетическом уровне
- 24. Скачать презентацию





















 Кислотно-основное титрование. 4 лекция. Часть 2
Кислотно-основное титрование. 4 лекция. Часть 2 Дослідження складу засобів гігієни та їх вплив на здоров’я людини Підготував : Учень 11 класу СШІТ № 2 Циб Владислав
Дослідження складу засобів гігієни та їх вплив на здоров’я людини Підготував : Учень 11 класу СШІТ № 2 Циб Владислав  Закон сохранения массы веществ
Закон сохранения массы веществ ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО
ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО Взаимодействие в двухкомпонентных системах. Примитивные виды взаимодействия: без промежуточных фаз
Взаимодействие в двухкомпонентных системах. Примитивные виды взаимодействия: без промежуточных фаз Электрохимические процессы и явления
Электрохимические процессы и явления Диазины. Характеристика диазинов. (Лекция 8)
Диазины. Характеристика диазинов. (Лекция 8) Полиэтилен, свойства и применение
Полиэтилен, свойства и применение Когда его называли гением, он морщился: "Какой там гений. Трудился всю жизнь, вот и стал гением". Когда в 26 лет писал курс "
Когда его называли гением, он морщился: "Какой там гений. Трудился всю жизнь, вот и стал гением". Когда в 26 лет писал курс " Термодинамика. 2 закон термодинамики. Энтропия
Термодинамика. 2 закон термодинамики. Энтропия Сероводород. Физические и химические свойства
Сероводород. Физические и химические свойства Химики на службе у дорог
Химики на службе у дорог Общие сведения о месторождениях полезных ископаемых
Общие сведения о месторождениях полезных ископаемых ПОЛИЭТИЛЕН
ПОЛИЭТИЛЕН  Презентация Предельные углеводороды
Презентация Предельные углеводороды  Силоксановый каучук
Силоксановый каучук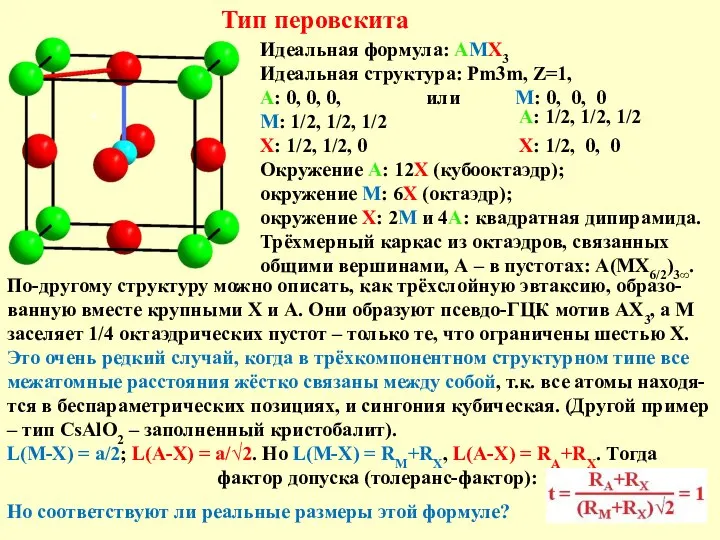 Тип перовскита
Тип перовскита Природный и синтетический каучуки. Резина
Природный и синтетический каучуки. Резина Газообразное состояние вещества Шаманина Наталья Сергеевна учитель химии, экологии и географии БОУ г. Омска «Средняя общеобраз
Газообразное состояние вещества Шаманина Наталья Сергеевна учитель химии, экологии и географии БОУ г. Омска «Средняя общеобраз Относительная атомная и молекулярная массы
Относительная атомная и молекулярная массы Темір. Жалпы сипаттама. Периодтық жүйедегі орны және атом құрылысы
Темір. Жалпы сипаттама. Периодтық жүйедегі орны және атом құрылысы Спирты. Понятие о спиртах
Спирты. Понятие о спиртах Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины
Предельные углеводороды. Насыщенные алифатические углеводороды. Алканы или Парафины Химиялық реакция жылдамдығы
Химиялық реакция жылдамдығы Презентация по Химии "Рисуем овощи и фрукты" - скачать смотреть бесплатно
Презентация по Химии "Рисуем овощи и фрукты" - скачать смотреть бесплатно Презентация по Химии "Презентация Йод" - скачать смотреть
Презентация по Химии "Презентация Йод" - скачать смотреть  Изотопы. Химические и физические свойства
Изотопы. Химические и физические свойства Токсикология и анализ спиртов
Токсикология и анализ спиртов