Содержание
- 2. Caracteristica generală, proprietăți fizice și chimice ale substanțelor pe clase: 1.Acizi; 2. Baze; 3.Oxizi; 4.Săruri. Chestionar
- 3. Identificarea proprietăților fizice și chimice ale acizilor, bazelor, oxizilor și sărurilor; Caracterizarea tipurilor de reacții chimice
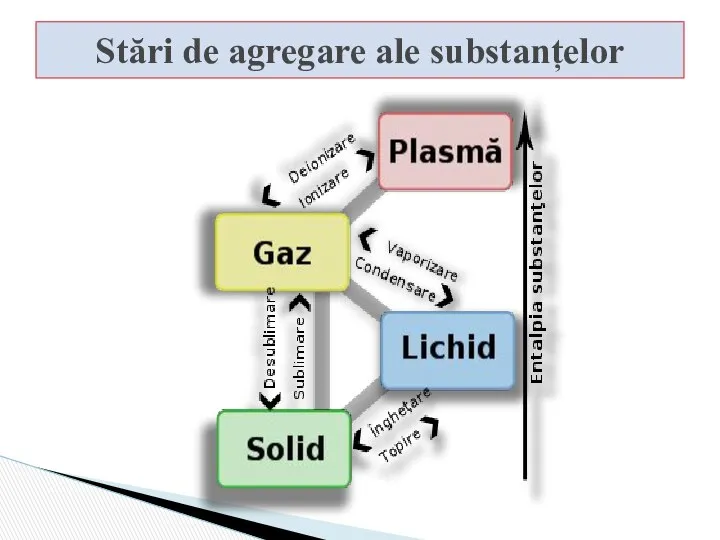
- 4. Stări de agregare ale substanțelor
- 5. Proprietăţi generale Acizii au gust acru, sunt caustici(ard); înroşesc turnesolul, respectiv metiloranjul; descompun piatra de var
- 6. CLASIFICAREA ACIZILOR ȘI BAZELOR Acizii: - compoziţia lor (hidracizi, conțin H și nemetal: HCl, HBr, HI)
- 7. Indicatorii acido – bazici sunt substanţe organice care îşi schimbă structura şi în consecinţă, culoarea, în
- 9. PROPRIETATILE FIZICE ALE ACIZILOR Acizii sunt substante - gazoase: HCl, H2S - lichide: HNO3, H2SO4 -
- 10. PROPRIETATILE CHIMICE ALE ACIZILOR Acțiunea asupra indicatorilor Soluția de turnesol – roșie Soluția de fenolftaleină- incoloră
- 11. Reactia acizilor cu oxizii bazici=sare+H2O 2HCl+CaO CaCl2+H2O H2SO4+CuO CuSO4+H2O Reactia de neutralizare = sare +H2O HCl
- 12. IMPORTANTA SI UTILIZARILE ACIZILOR Acizii se folosesc în laborator – reactivi : obținerea sărurilor, H2, neutralizarea
- 13. Baze Formula generală a bazelor este: M(OH)n. în care M este atomul metalului, iar n reprezintă
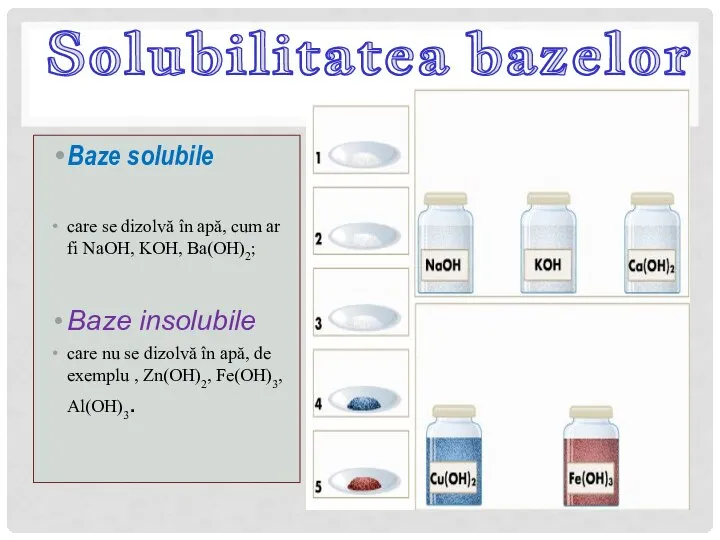
- 14. Baze solubile care se dizolvă în apă, cum ar fi NaOH, KOH, Ba(OH)2; Baze insolubile care
- 15. PROPRIETĂȚI FIZICE • hidroxizii alcalini sunt substanţe solide, albe, opace, higroscopice, bine solubile în apă. •
- 16. PROPRIETĂȚI CHIMICE Unii hidroxizi (de Zn, Al, Sn, Pb) au caracter amfoter , adica reactioneaza cu
- 17. Reactia de neutralizare Toate bazele reactioneaza cu acizii, formand saruri si apa. NaOH + HCl =
- 18. OXIZII Oxizii - sunt compuşi binari ai oxigenului cu alte elemente, metale sau nemetale. Se cunosc
- 19. Proprietăţi fizice la temperatura obişnuită, majoritatea oxizilor sunt substanţe solide sau gazoase; • oxizii metalelor pot
- 20. METODE DE OBTINERE Reacţii de combinare a)Reacţia metalelor cu oxigenul 4Na + O2 => 2Na2O b)Reacţia
- 21. REACŢII DE DESCOMPUNERE CaCO3 ? CaO + CO2 MgCO3 ? MgO + CO2 CuCO3 ? CuO
- 22. PROPRIETĂȚI CHIMICE A)Reacţii cu substanţe simple: Oxizii superiori pot fi obţinuţi prin reacţia oxizilor inferiori cu
- 23. REACŢII CU SUBSTANŢE COMPUSE a)Reacţionează cu apa oxid metalic + apa => baza CaO + H2O
- 24. REACŢIA BAZELOR CU OXIZI ACIZI oxid acid+ bază => sare + apă CO2 + Ca(OH)2 =>CaCO3+
- 25. IMPORTANŢĂ ŞI UTILIZĂRI: materii prime: Al2O3 (bauxita), FeO, Fe2O3; materiale de construcţii: CaO, SiO2; obţinerea acizilor:
- 26. CARACTERISTICILE UNOR OXIZI CO Nu întreține arderea, dar arde cu flacară albastră si formează CO2.Este gaz
- 27. SĂRURILE Sărurile sunt combinaţii cu structură ionică, în general, formate prin neutralizarea unui acid cu o
- 28. Săruri normale (neutre) NaCl — clorură de sodiu CaCO3 — carbonat de calciu CuSO4 —sulfat de
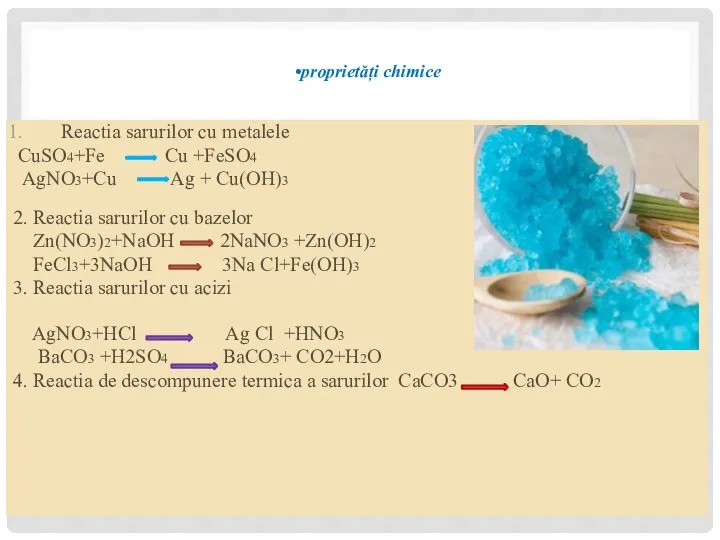
- 29. proprietăți chimice Reactia sarurilor cu metalele CuSO4+Fe Cu +FeSO4 AgNO3+Cu Ag + Cu(OH)3 2. Reactia sarurilor
- 30. Utilizări Materiale de construcție Fabricarea hârtiei Rafinarea cuprului Fabricarea sapunurilor Fabricarea îngrășămintelor Fabricarea sticlei SĂRURI Producerea
- 32. Скачать презентацию


























 Твёрдые жиры
Твёрдые жиры Спирты. Состав и строение спиртов
Спирты. Состав и строение спиртов Презентация по Химии "Задания на соответствие" - скачать смотреть
Презентация по Химии "Задания на соответствие" - скачать смотреть  Model chemistry
Model chemistry Тұздар гидролизі
Тұздар гидролизі Полимеры. Степень полимеризации
Полимеры. Степень полимеризации Углеводороды. Алкены
Углеводороды. Алкены Виды присадок к моторным топливам. Керосин
Виды присадок к моторным топливам. Керосин Р-элементы III группы
Р-элементы III группы Phase formation rules for high entropy alloys
Phase formation rules for high entropy alloys Кислоты и соли. (8 класс)
Кислоты и соли. (8 класс) Визначення якості мила за його лужністю
Визначення якості мила за його лужністю Консистентные смазки для легковых автомобилей
Консистентные смазки для легковых автомобилей Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Vodík
Vodík Көміртегінің мөлшері бойынша легірленген болаттың классификациясы
Көміртегінің мөлшері бойынша легірленген болаттың классификациясы Разработка реактора для отопления домов путем извлечения водорода из воды
Разработка реактора для отопления домов путем извлечения водорода из воды Турнир юных химиков
Турнир юных химиков Жоғары температурағы асқын өткізгіштер
Жоғары температурағы асқын өткізгіштер Группа редкоземельных элементов
Группа редкоземельных элементов Материалы с особыми тепловыми свойствами
Материалы с особыми тепловыми свойствами Рафинирование металлических расплавов
Рафинирование металлических расплавов Физическая и коллоидная химия
Физическая и коллоидная химия Кислотность и основность рганических соединений. Инфракрасная спектроскопия
Кислотность и основность рганических соединений. Инфракрасная спектроскопия Проверка знаний по теме «Белки, состав, структура, функции» (работа на 10-12 минут)
Проверка знаний по теме «Белки, состав, структура, функции» (работа на 10-12 минут) Химиялық реакцияның жылдамдығы. Катализ
Химиялық реакцияның жылдамдығы. Катализ Хімічні добавки. Е-числа Підготувала Учениця 11-А класу Макарівського НВК Заріцька Вікторія Вчитель:Гребенюк Олександра Іва
Хімічні добавки. Е-числа Підготувала Учениця 11-А класу Макарівського НВК Заріцька Вікторія Вчитель:Гребенюк Олександра Іва Адсорбция. Адсорбциондық тепе-теңдік
Адсорбция. Адсорбциондық тепе-теңдік