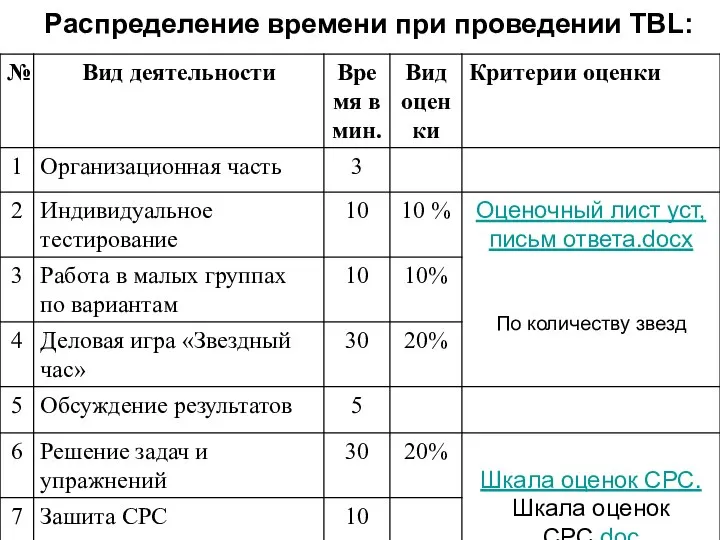
Слайд 10

В заключении – рефлексивный тест.
Рефле́ксия (от позднелат. reflexio — обращение назад) —
обращение субъекта — обращение назад) — обращение субъекта на себя самого, свою личность (ценности, интересы, мотивы, эмоции — обращение назад) — обращение субъекта на себя самого, свою личность (ценности, интересы, мотивы, эмоции, поступки), на свое знание — обращение назад) — обращение субъекта на себя самого, свою личность (ценности, интересы, мотивы, эмоции, поступки), на свое знание или на свое собственное состояние.
Узнал(а) много нового.
Мне это пригодится в жизни.
Было над чем подумать.
На возникшие вопросы я получил(а) ответ.
Поработал(а) добросовестно, цель достигнута.
На доске два рисунка с рожицами (с улыбкой и без).
Предлагается прикрепить магнитные фигурки к тому рисунку, который отражает Ваше отношение к проведенному занятию.

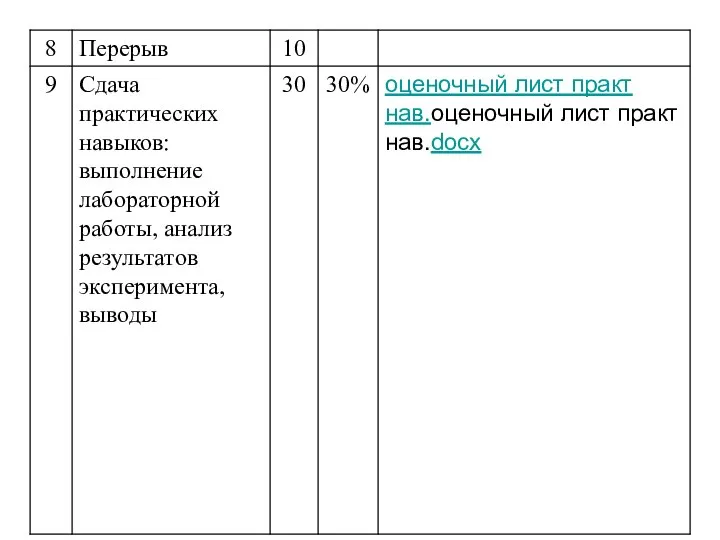
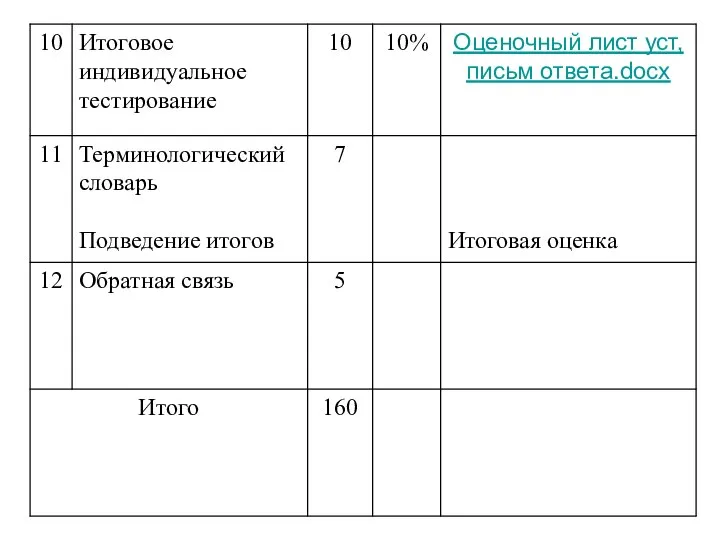











 Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы
Аттестационная работа. Выращивание кристаллов. Выявить условия, позволяющие из раствора медного купороса выращивать кристаллы Ցեմենտի արտադրություն
Ցեմենտի արտադրություն Ученые – химики в годы Великой Отечественной войны
Ученые – химики в годы Великой Отечественной войны Кремний и его соединения
Кремний и его соединения Аллотропия. Аллотропные модификации
Аллотропия. Аллотропные модификации ЗОЛОТОЙ ВЕК ГОЛЛАНДСКОЙ ЖИВОПИСИ
ЗОЛОТОЙ ВЕК ГОЛЛАНДСКОЙ ЖИВОПИСИ  Кристаллдық және аморфтық күй
Кристаллдық және аморфтық күй Углерод. Металлы. 9 класс
Углерод. Металлы. 9 класс А.Д. Сахаров – выдающийся ученый и правозащитник современности МБОУ «Гимназия № 13», 9 «Б» класс. Выполнил: Артёмов Александр. На
А.Д. Сахаров – выдающийся ученый и правозащитник современности МБОУ «Гимназия № 13», 9 «Б» класс. Выполнил: Артёмов Александр. На Аналитическая химия. Качественный анализ
Аналитическая химия. Качественный анализ Окислительно-восстановительные реакции. Электролиз
Окислительно-восстановительные реакции. Электролиз Токсичность. Параметры токсичности
Токсичность. Параметры токсичности Электронное строение атома
Электронное строение атома Разработка технологии получения наноструктурированных катализаторов для гидрирования
Разработка технологии получения наноструктурированных катализаторов для гидрирования Синтетические моющие средства
Синтетические моющие средства Металловедение. Основные типы диаграмм состояния двойных сплавов. (Лекция 4)
Металловедение. Основные типы диаграмм состояния двойных сплавов. (Лекция 4) Строение и функции отдельных коферментов
Строение и функции отдельных коферментов Сравнительная характеристика бензольного кольца и олимпийских колец
Сравнительная характеристика бензольного кольца и олимпийских колец Щелочноземельные металлы
Щелочноземельные металлы Галогены: Хлор, бром, иод
Галогены: Хлор, бром, иод Путешествие по континенту Химия. Познавательная игра по химии, 8 класс
Путешествие по континенту Химия. Познавательная игра по химии, 8 класс Эластомеры (резины)
Эластомеры (резины) Презентация по Химии "«Щелочные металлы»" - скачать смотреть
Презентация по Химии "«Щелочные металлы»" - скачать смотреть  Химиялық элемент алюминий
Химиялық элемент алюминий Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль
Строение атома. Атомные орбитали. Типы связей. Основные органогенные элементы, их роль Аминокислоты и белки
Аминокислоты и белки λ-MnO2 as material with pseudocapacitive properties
λ-MnO2 as material with pseudocapacitive properties Галогены - друзья или враги?
Галогены - друзья или враги?