Содержание
- 2. Cодержание : 1.Введение 2.Определение аминокислот 3.Изомерия аминокислот 4.Фические свойства аминокислот 5.Метод получения аминокислот 6.Химические свойства аминокислот
- 3. 1.Введение На уроках химии мы изучили тему «Аминокислоты и белки .» В этом презентационном проекте я
- 4. 2.Определение аминокислот Аминокислоты -органические соединения, в состав которых входят две функциональные группы : карбоксильная –СООН и
- 5. 3.Изомерия аминокислот Структурная изомерия связана с особенностями строения углеродного скелета и взаимным расположением функциональных групп. Рис.1
- 6. Аминокислоты –бесцветные кристаллические вещества, плавящиеся с разложением при температуре выше 200°С .Они растворимы в воде и
- 7. 5.Метод получения аминокислот Под действием ферментов , а также водных растворов , кислот и щелочей происходит
- 8. 6. Химические свойства аминокислот Все аминокислоты — амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные
- 9. 6.1. Кислотные и основные свойства Как основания , они взаимодействуют с кислотами , образуя соли. Как
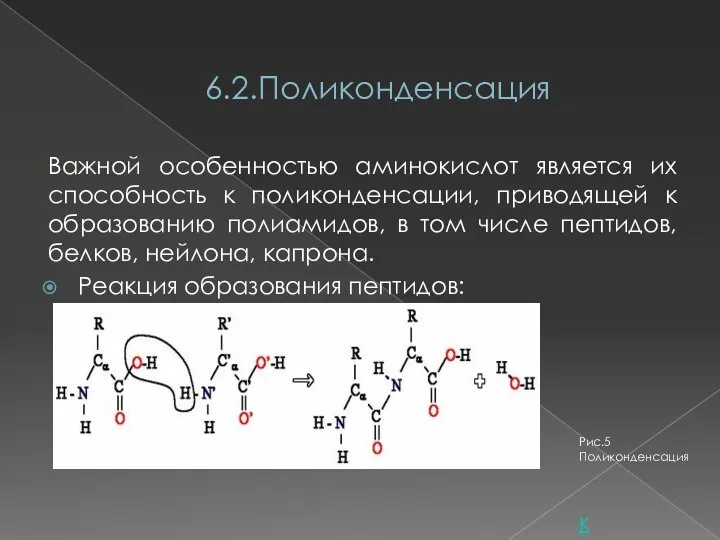
- 10. 6.2.Поликонденсация Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе
- 11. 7.Применение аминокислот Аминокислоты входят в состав спортивного питания и комбикорма. Также аминокислоты применяют в качестве лекарственных
- 12. 8.Определение белков Белки -высокомолекулярное органическое соединение, представляющее собой полимер, который построен из остатков аминокислот, соединенных между
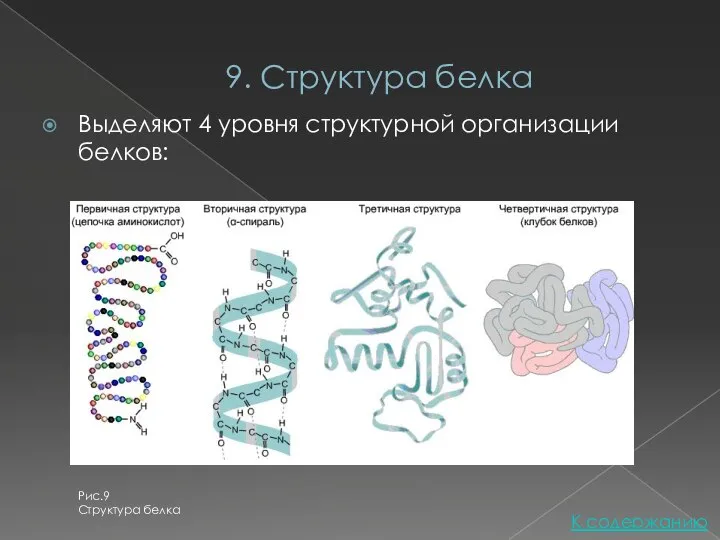
- 13. 9. Структура белка Выделяют 4 уровня структурной организации белков: К содержанию Рис.9 Структура белка
- 14. 10.Физические свойства белков Физические свойства белка определяются строением, поэтому белки делят на глобулярные (растворимые в воде)
- 15. 11. Химические свойства белков При нагревании белки способны к денатурации (разрушение вторичной и третичной структуры белка)
- 16. 11.1 Качественные реакции на белки Биуретовая реакция. При действии на белки свежеполученного осадка гидроксида меди (II),
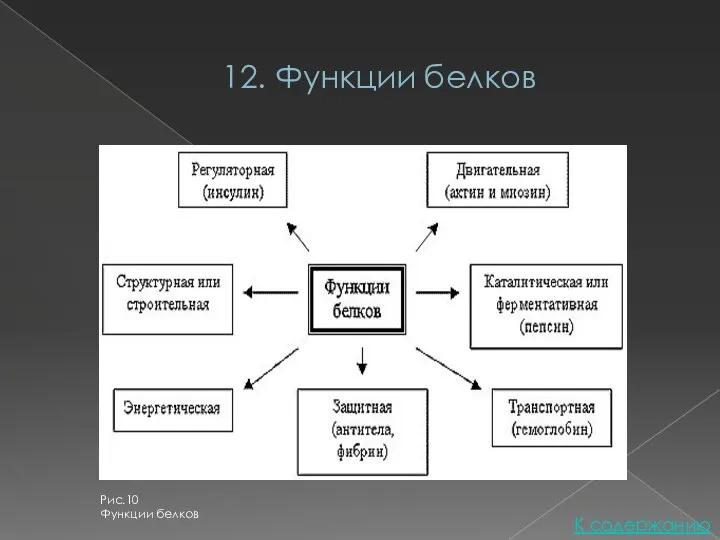
- 17. 12. Функции белков К содержанию Рис.10 Функции белков
- 18. 12.1 Ферментативная функция Большинство химических реакций в организме протекают в присутствии биологических катализаторов – ферментов ,
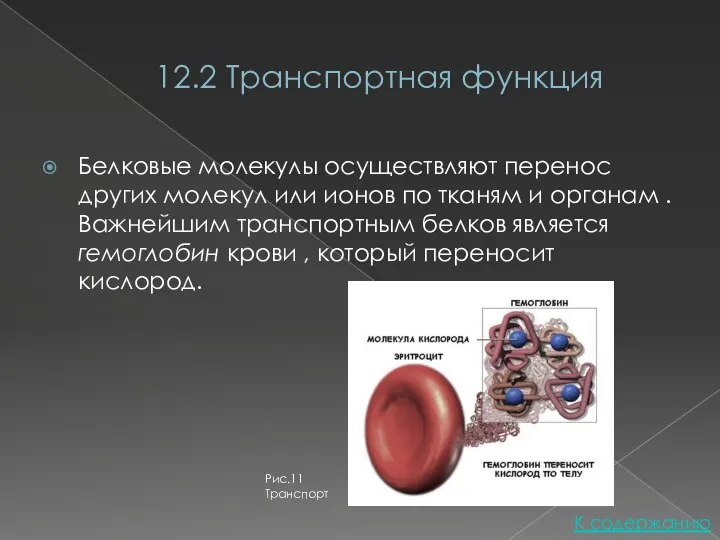
- 19. 12.2 Транспортная функция Белковые молекулы осуществляют перенос других молекул или ионов по тканям и органам .
- 20. 12.3 Структурная функция Белки – это строительный материал почти всех тканей организма : мышечных , опорных
- 21. 12.4 Защитная функция Особые белки – антитела и антитоксины ( белки, которые нейтрализуют яд , образующиеся
- 22. 12.5 Сигнальная функция Белки-рецепторы воспринимают и передают сигналы , поступившие из соседних клеток или окружающей среды
- 23. 12.6 Энергетическая функция Эту функцию в клетках живых организмов выполняют особые белки. Они служат строительным материалом
- 24. 13. Заключение Таким образом , можно сделать следующие выводы : Белки — основа нашей жизни. От
- 26. Скачать презентацию



















 Аминирование диазо
Аминирование диазо Презентация по Химии "Кристаллические решетки" - скачать смотреть
Презентация по Химии "Кристаллические решетки" - скачать смотреть  Масла автомобильные
Масла автомобильные Основания (оснόвные гидроксиды)
Основания (оснόвные гидроксиды) Высокомолекулярные вещества полимеры
Высокомолекулярные вещества полимеры Механизмы трансформации энергии в фотосинтезе
Механизмы трансформации энергии в фотосинтезе Водороды
Водороды Типы химических реакций в органической химии
Типы химических реакций в органической химии Основные законы химии
Основные законы химии Презентация по Химии "Растворимость веществ в воде" - скачать смотреть
Презентация по Химии "Растворимость веществ в воде" - скачать смотреть  Презентация по Химии "Роль металлов в искусстве" - скачать смотреть
Презентация по Химии "Роль металлов в искусстве" - скачать смотреть  Состав и строение металлических кристаллов в титаномагнетитовой руде при медленном росте
Состав и строение металлических кристаллов в титаномагнетитовой руде при медленном росте Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти
Сульфатна кислота. Фізичні та хімічні властивості сульфатної кислоти Функциональные производные с простой связью C-“Э". Галогенпроизводные. (Лекция 5)
Функциональные производные с простой связью C-“Э". Галогенпроизводные. (Лекция 5) Презентация по Химии "Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам курса неорганической химии&qu
Презентация по Химии "Закрепление, совершенствование, обобщение знаний и подготовка к ЕГЭ по темам курса неорганической химии&qu Хром. Строение атома
Хром. Строение атома Петрография магматических пород
Петрография магматических пород Хімія. Каучук
Хімія. Каучук Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть
Презентация по Химии "Д.И. Менделеев – основоположник русской агрохимии" - скачать смотреть  Группа веществ, изолируемых полярными растворителями
Группа веществ, изолируемых полярными растворителями Производственно-торговая компания ООО «СОЖ Синтез-Набережные Челны»
Производственно-торговая компания ООО «СОЖ Синтез-Набережные Челны» Татьяна Леонидовна Быкова, учитель химии, Муниципальное общеобразовательное учреждение «Средняя общеобразовательная школ
Татьяна Леонидовна Быкова, учитель химии, Муниципальное общеобразовательное учреждение «Средняя общеобразовательная школ Волокна Презентація на тему:
Волокна Презентація на тему:  Энергетический обмен в клетке - катаболизм
Энергетический обмен в клетке - катаболизм Олефиновые углеводороды как сырье для органического синтеза. Реакции олефинов. Способы производства олефинов. Лекция 4
Олефиновые углеводороды как сырье для органического синтеза. Реакции олефинов. Способы производства олефинов. Лекция 4 Закон действующих масс и его использование в расчетах. (Лекциии 4-6)
Закон действующих масс и его использование в расчетах. (Лекциии 4-6) Биосинтез углеводов в организме. Метаболизм гексоз. (Лекция 11)
Биосинтез углеводов в организме. Метаболизм гексоз. (Лекция 11) Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия
Целлюлоза Выполнила студентка 11 группы Сыровацкая Лилия