Содержание
- 4. КТ - термодинамическая константа КТ = f (природа вещества, природа растворителя, Т, Р), не зависит от
- 5. Кf - функция активности Кf
- 6. Применение теории сильных электролитов в аналитических расчетах Для раствора, содержащего 0,1 М СаСl2, 0,2 М КСl
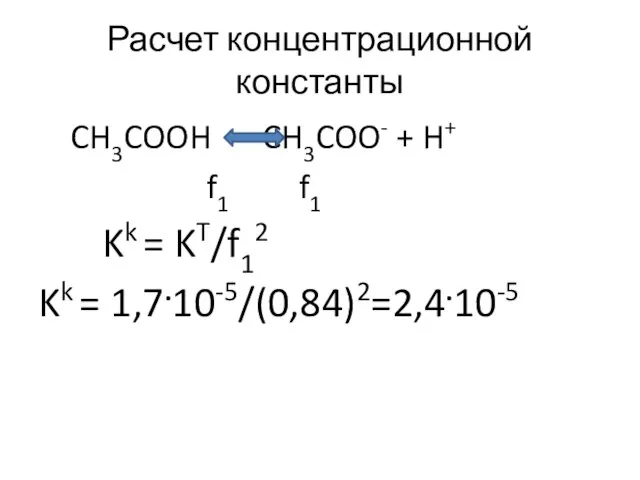
- 7. Расчет концентрационной константы CH3COOH CH3COO- + H+ f1 f1 Kk = KT/f12 Kk = 1,7.10-5/(0,84)2=2,4.10-5
- 8. Константы сильных, слабых, хорошо и малорастворимых электролитов. Показатели констант Константы распада электролита (К и рК): рК
- 9. Константы образования (β и lg β)
- 10. Константы H2O.
- 11. Константы кислот и их показатели (Ка и рКа)
- 12. Константы кислот и их показатели (Ка и рКа) двух- и многопротонные кислоты: H2SO4, H4[Fe(CN)6] и др.
- 13. Кислоты растворимые слабые однопротонные HF, HNO2, HClO, CH3COOH и др. α ≤ 3% HF ⇔ H+
- 15. Если f(H+) и f(F–) = 1, то Как = Кат это возможно в чистых растворах слабых
- 16. По константам и показателям констант производят сравнение силы слабых кислот. Правило: Чем больше значение константы или
- 18. В общем случае: Кок(т) = К1 ⋅ К2 ⋅ К3 ⋅ … Кn рКок(т) = рК1
- 19. Константы оснований и их показатели (Кb и рКb) Основания растворимые сильные однопротонные KOH, NaOH, LiOH, TlOH
- 20. Основания растворимые слабые однопротонные NH3⋅H2O (HOH), CH3NH2⋅H2O, C5H5N⋅H2O или: NH3⋅H2O → [NH3.H]OH→NH4OH [CH3NH2⋅H]+ OH– [C5H5NH]+OH NH3⋅H2O
- 21. Основания растворимые слабые
- 22. Двух- и многопротонные основания малорастворимые основания: Ca(OH)2 – сильное, но только по 1-й ступени слабые: AgOH,
- 23. Константы комплексных ионов Комплексные соединения при диссоциации на внешнюю и внутреннюю сферу относятся к сильным электролитам,
- 24. Кнест., константа устойчивости β К ступенч. и Ко β ступ. и βо Количество ступеней соответствует количеству
- 25. Для ступенчатых констант: β - есть обратная величина той константе нестойкости, которая характеризует данное равновесие и
- 26. Константы малорастворимых электролитов Кислоты: H4SiO4, H2SiO3, HSbO3 Основания: AgOH, Fe(OH)2, Al(OH)3 Соли: AgCl, BaSO4, K2Pb[Cu(NO2)6], K2Na[Co(NO2)6],
- 27. Ksk = [Ca2+] ⋅ [CO32–] (рассчитывают) Кsт = а(Са2+) ⋅ а(СО32–) (в справочнике) Константа растворимости характеризует
- 28. Вывод выражения константы равновесия реакций, протекающих без изменения степени окисления, через константы слабых и малорастворимых электролитов
- 29. Константа равновесия для любых взаимодействий есть отношение произведений констант слабых и малорастворимых электролитов, вступивших в реакцию,
- 30. Константа равновесия и полнота протекания реакции Реакция считается протекающей практически полно, если вступившие в нее вещества
- 31. Если реакция протекает на 99%, то К равновесия (для реакции типа Ар-р + Вр-р ↔ Ср-р
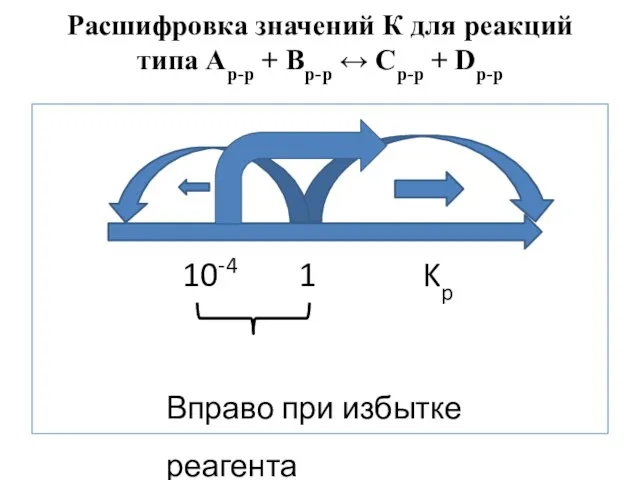
- 32. Расшифровка значений К для реакций типа Ар-р + Вр-р ↔ Ср-р + Dр-р К > 1
- 33. Расшифровка значений К для реакций типа Ар-р + Вр-р ↔ Ср-р + Dр-р 10-4 1 Kp
- 34. Возможности К равновесия реакции Константа равновесия показывает: принципиальную, т.е. термодинамическую возможность протекания реакции, ее направление и
- 35. Пример 1. Hg22+ +2Cl- = Hg2Cl2↓ K = 1/Kso = 1018 Kso Ag+ +Cl- = AgCl↓
- 36. Пример 2. Наиболее вероятна 3 реакция
- 37. Пример 3. 1. CaCO3↓+ 2CH3COOH ↔ Ca(CH3COO)2 + H2CO3 К = 6 ∙ 10–2 (10–4 –
- 38. Необходимый избыток рассчитывают, решая неравенство К > π (функция π) Константа К отвечает за протекание реакции
- 39. Сколько мл концентрированного раствора аммиака потребуется для полного растворения 0,1 г хлорида серебра? Решение: Концентрированный аммиак
- 40. Из выражения для константы равновесия найдем концентрацию аммиаката серебра: обозначим [Ag(NH3)2]+ = х, тогда [Cl-] =
- 41. ТИР (теория ионных равновесий) применительно к типам химических реакций Известны 4 типа химических реакций: - осаждения
- 42. Реакции осаждения Равновесие в системе «осадок – насыщенный р-р малорастворимого сильного электролита» Реакции осаждения – частный
- 43. Способы выражения растворимости г/ на 100 г H2O; г/л раствора; моль/л раствора По величине растворимости вещества
- 44. Взаимосвязь между S и Kso Если растворимость S выражена в моль/л, то она означает концентрацию малорастворимого
- 45. Напишите выражение Kso малорастворимого электролита Mg3(PO4)2 через равновесные концентрации и через растворимость. Рассчитайте Kso Mg3(PO4)2, если
- 46. Расчет растворимости с использованием Kso при I = 0 и I > 0 I = 0
- 47. Рассчитайте растворимость PbBr2 в чистом водном растворе в моль/л и в г/л. M(PbBr2) = 367 г/моль.
- 48. I > 0 в присутствии одноименных ионов ← + Na2SO4 изб. ← + BaCl2 изб. При
- 49. Расчет растворимости в присутствии одноименных ионов Расчет проводят, используя значение Kso, не учитывая коэффициенты активности, т.к.
- 50. Расчет растворимости в присутствии одноименных ионов одноименные ионы – анионы одноименные ионы – катионы
- 51. Общая формула
- 52. Ионное произведение (ИП) и критерии установления возможности образования и выделения в осадок малорастворимых электролитов с учетом
- 53. Выпадет ли осадок при смешении 20 мл 0,005 М раствора хлорида кальция с 30 мл 0,002
- 54. Критерий и расчет практической полноты осаждения Осаждение считается практически полным, когда концентрация ионов малорастворимого электролита, оставшихся
- 55. Формулы расчета полноты осаждения осаждается катион KsoKmAn = [Kn+]mост. ∙ [Am–]nизб осаждается анион KsoKmAn = [Kn+]mизб.
- 56. Расчет полноты осаждения Будет ли достигнута полнота осаждения ионов Pb2+ и Ag+, если к 10 мл
- 57. Факторы, влияющие на полноту осаждения Концентрация осадителя Температура (t) Природа растворителя Сила осадителя как электролита Солевой
- 58. Влияние концентрации осадителя Избыточная концентрация осадителя увеличивает полноту осаждения и является положительным фактором только в том
- 59. Влияние концентрации осадителя Избыточная концентрация осадителя является отрицательным фактором, если избыток осадителя вступает в химическую реакцию
- 60. Влияние температуры (t) При увеличении t увеличивается активность химического взаимодействия, но в то же время увеличивается
- 61. Влияние природы растворителя Растворимость (S) малорастворимых электролитов уменьшается в присутствии органических растворителей, хорошо смешивающихся с водой.
- 62. Влияние силы осадителя как электролита При использовании осадителя входящего в состав более сильного электролита достигается более
- 63. Солевой эффект Солевой эффект – это увеличение растворимости малорастворимого электролита при I > 0 в присутствии
- 64. Расчет концентрации осадителя для начала и практически полного осаждения ионов осаждаемый ион – катион осаждаемый ион
- 65. Для расчета концентрации осадителя для практически полного осаждения необходимо знать Кso малорастворимого электролита и критерий практически
- 66. Дробное осаждение Это определенная последовательность в образовании и выделении в осадок малорастворимых электролитов из одного и
- 67. Пример правила 1 Дан р-р: Cl–, Br– C(Cl–) = C(Br–) +AgNO3 10–6 моль/л ↓ SAgBr ос-к:
- 68. Пример правила 2 Дан р-р: Cl–, Br– и C(Cl–) ≠ C(Br–) С(Cl–) = 1 моль/л; С(Br–)
- 69. Kакой осадок выпадет первым, если к раствору, содержащему 0,1 М KCl и 0,01 М K2CrO4 прибавить
- 70. Какая доля (в %) хлорид-ионов выпадет в осадок до начала осаждения хромат-ионов? Решение: Найдем С(Сl-), оставшуюся
- 71. Совместное осаждение Это одновременное осаждение ионов одним и тем же осадителем из одного и того же
- 72. Совместное осаждение Расчеты для построения графиков осаждения Расчет С(осадителя) для начала и практически полного осаждения каждого
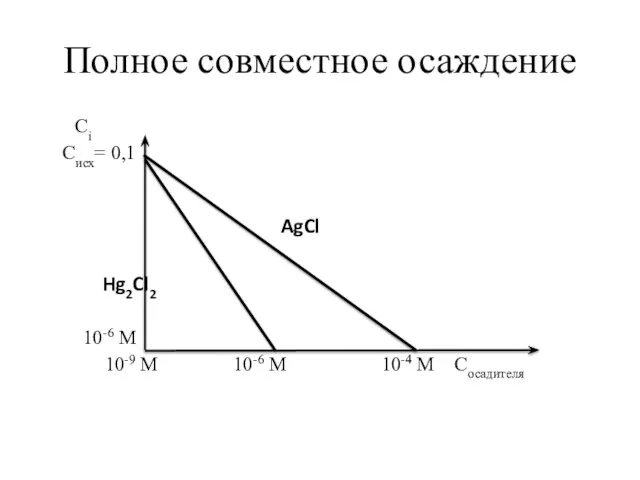
- 73. Полное совместное осаждение
- 74. Полное совместное осаждение Сi Cисх= 0,1 Hg2Cl2 10-6 М 10-9 М 10-6 М 10-4 М Cосадителя
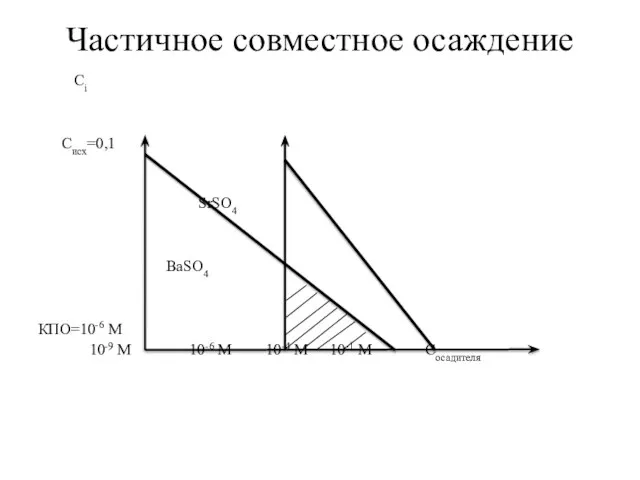
- 75. Частичное совместное осаждение Пример: Происходит ли совместное осаждение Ва2+ и Sr2+ из их 0,1 М растворов
- 76. Частичное совместное осаждение Сi Cисх=0,1 SrSO4 ВаSO4 КПО=10-6 М 10-9 М 10-6 М 10-4 М 10-1
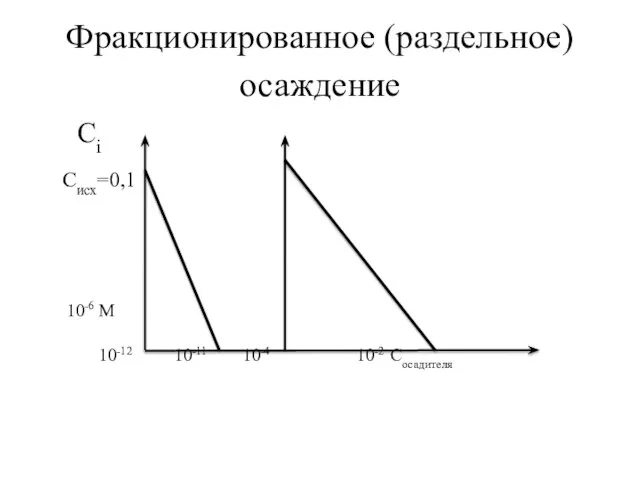
- 77. Фракционированное (раздельное) осаждение
- 78. Фракционированное (раздельное) осаждение Сi Cисх=0,1 10-6 М 10-12 10-11 10-4 10-2 Cосадителя
- 79. Важнейшие осадители Кислоты: HCl, H2SO4, H2S, коричная кислота. Основания: NaOH, KOH, NH3∙H2O, 8-оксихинолин Соли: Na2CO3 (K2CO3),
- 80. Растворение осадков Критерий полноты растворения осадков: 10–2 моль/л. Sм.р. эл-та, содержащего осаждаемый ион, ≥ 10–2 М
- 81. Растворение осадков Растворение осадка происходит при ИП Уменьшение концентрации ионов осадка возможно при: 1. сильном разбавлении;
- 82. Растворение осадков
- 83. Растворение осадков Пример 2. Mg(OH)2 + 2NH4+ = Mg2+ + 2NH3.H2O Кso(Mg(OH)2) = 6,0.10-10 ; Кb(NH3.H2O)
- 84. Растворение осадков Пример 3. CaCO3↓+ 2CH3COOH ↔ Ca(CH3COO)2 + H2O + CO2 ↑ Константа равновесия этой
- 85. Растворение осадков Пример 4. Вопрос: Будут ли полностью растворяться в концентрированном аммиаке AgCl и AgBr? Ответ:
- 86. Растворение осадков Пример 5. 3CuS + 8HNO3 = 3Cu(NO3)2 + 3S + 2NO + 4H2O Окисление
- 87. Перевод одних осадков в другие Необходимость такого перевода возникает при анализе смеси катионов III группы. Для
- 89. Скачать презентацию











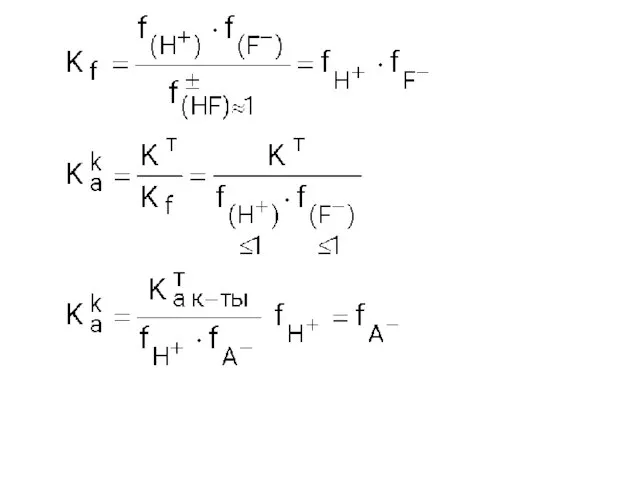












![Ksk = [Ca2+] ⋅ [CO32–] (рассчитывают) Кsт = а(Са2+) ⋅ а(СО32–)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/548770/slide-26.jpg)











![Из выражения для константы равновесия найдем концентрацию аммиаката серебра: обозначим [Ag(NH3)2]+](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/548770/slide-39.jpg)














![Формулы расчета полноты осаждения осаждается катион KsoKmAn = [Kn+]mост. ∙ [Am–]nизб](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/548770/slide-54.jpg)





























 Подготовка к ЕГЭ
Подготовка к ЕГЭ КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ
КУБАНСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ КУБАНСКИЙ МЕДИЦИНСКИЙ ИНСТИТУТ КАФЕДРА ФУНДАМЕНТАЛЬНОЙ И КЛИНИЧЕСКОЙ БИОХИМ Микробиологическая лаборатория и ее задачи. Микроскоп и работа с ним. Морфология шаровидных бактерий
Микробиологическая лаборатория и ее задачи. Микроскоп и работа с ним. Морфология шаровидных бактерий Аминокислоты – структурные единицы белков
Аминокислоты – структурные единицы белков Проект: «Биологическая роль йода, нахождение йода в лекарственных препаратах»
Проект: «Биологическая роль йода, нахождение йода в лекарственных препаратах» Применение карбоновых кислот и сложных эфиров
Применение карбоновых кислот и сложных эфиров Происхождение химических элементов
Происхождение химических элементов Растворы. Способы выражения концентрации растворов
Растворы. Способы выражения концентрации растворов Получение Н2, О2, щелочей
Получение Н2, О2, щелочей Жуғыш заттар және жуғыш әсері. 1 Лекция
Жуғыш заттар және жуғыш әсері. 1 Лекция Закономерности наследования признаков, установленные Г. Менделем
Закономерности наследования признаков, установленные Г. Менделем Органическая химия. (Урок 1-2)
Органическая химия. (Урок 1-2) Алюминий и его соединения
Алюминий и его соединения Двовимірний ямр. Типи двовимірних спектрів
Двовимірний ямр. Типи двовимірних спектрів Периодический закон. Периодическая система элементов. (Лекция 2)
Периодический закон. Периодическая система элементов. (Лекция 2) Общая геология. Породообразующие минералы
Общая геология. Породообразующие минералы ИГРЫ С ПЕРЧАТКАМИ Часто в химических лабораториях игривые экспериментаторы используют не по назначению латексные перчатки. Напр
ИГРЫ С ПЕРЧАТКАМИ Часто в химических лабораториях игривые экспериментаторы используют не по назначению латексные перчатки. Напр Алкены
Алкены Основы химической коррозии
Основы химической коррозии Устойчивость дисперсных систем
Устойчивость дисперсных систем Монокристаллы InSb. Свойства, выращивание, применение
Монокристаллы InSb. Свойства, выращивание, применение Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері
Тіндер-тірі организмнің иерархиялық деңгейінің ұйымдастырудың бір түрі. Олардың құрылымдық принциптері Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень
Основи прийняття рішень, щодо захисту населення під час різних фаз радіаційної аварії. Критерії для прийняття рішень Нефть. Образование нефти
Нефть. Образование нефти Гомологи бензола
Гомологи бензола Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар
Илік заттар. Тітіркендіруші заттар. Қапталғыш заттар, адсорбциялаушы заттар Полиэтилентерефталат. Свойства. Получение
Полиэтилентерефталат. Свойства. Получение Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть
Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть