Содержание
- 2. Цели урока: Изучить строение атома и молекулы азота; Развить исторические познания в области открытия химических элементов;
- 3. История открытия. Даниэль Резерфорд Карл Вильгельм Шееле В 1772 г. английский ученый Д. Резерфорд и шведский
- 4. История открытия. В 1787 г. Антуан Лоран Лавуазье установил наличие в воздухе газа, не поддерживающего дыхания
- 5. История открытия. Жан Антуан Шапталь В 1790 г. Жаном Шапталем было предложено другое латинское название «нитрогениум»,
- 6. Строение атома азота
- 7. молекулярная формула
- 8. Физические свойства азота При нормальных условиях азот это бесцветный газ, не имеет запаха, мало растворим в
- 9. Физические свойства азота При −209,86 °C азот переходит в твердое состояние в виде снегоподобной массы или
- 10. Химические свойства азота При обычных условиях азот малоактивен. Это объясняется прочностью химических связей в его молекуле.
- 11. Химические свойства азота С другими металлами он реагирует лишь при высоких температурах, образуя нитриды: 3Ca +
- 12. Химические свойства азота Образующиеся нитриды полностью гидролизуются при контакте с водой: Сa3N2 + 6H2O → 3Ca(OH)2
- 13. Химические свойства азота С кислородом азот взаимодействует только в электрической дуге (3000-4000° С) (например, при грозовом
- 14. Химические свойства азота При определенных условиях азот реагирует с водородом (температура 300° С, давление 20-30 МПа,
- 15. Получение азота В лабораториях азот можно получать по реакции разложения нитрита аммония: t NH4NO2 → N2↑
- 16. Биологическое значение азота Азот — одно из самых распространенных веществ в биосфере, узкой оболочке Земли, где
- 19. АЗОТ: В атмосфере азота - 4 квадрильона (4·1015) тонн (4 000 000 000 000 000 тонн)
- 20. Незначительная часть этого количества — около 100 миллионов тонн — ежегодно связывается и включается в состав
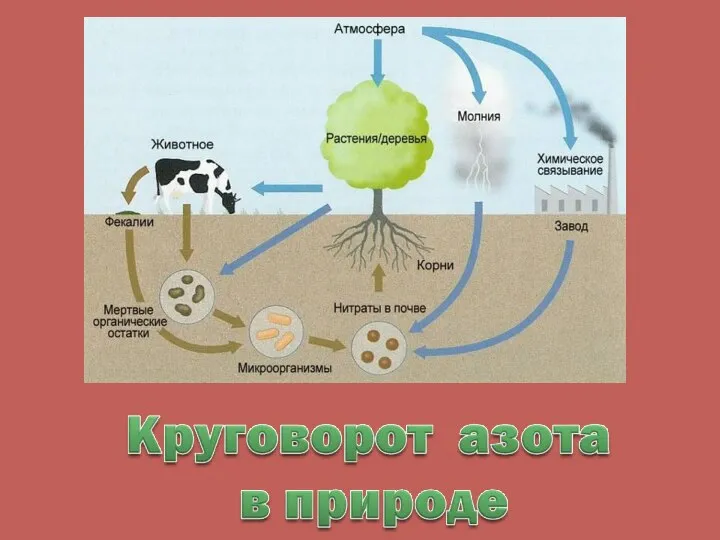
- 21. Главный поставщик связанного азота в природе — бактерии: благодаря им связывается приблизительно от 90 до 140
- 22. На использовании бактерий основан традиционный метод повышения плодородия почвы: на поле сначала выращивают горох или другие
- 23. Некоторое количество азота переводится в связанное состояние во время грозы электрический разряд нагревает атмосферу вокруг себя,
- 24. Таким образом, в результате естественных природных процессов связывается от 100 до 150 миллионов тонн азота год.
- 25. Всякий раз, когда вы совершаете поездку на автомобиле, в биосферу поступает дополнительное количество связанного азота. Примерно
- 26. Но больше всего связанного азота человек производит в виде минеральных удобрений.
- 27. Недостаток азота часто сдерживает рост растений, и фермеры для повышения урожайности покупают искусственно связанный азот в
- 28. Суммировав весь вклад человека в круговорот азота, получаем цифру порядка 140 миллионов тонн в год. Примерно
- 29. Каждая экосистема способна усвоить определенное количество азота, и последствия этого в целом благоприятны — растения станут
- 30. Эвтрофикация (загрязнение водоемов водорослями)—самая неприятная экологическая проблема, связанная с азотом. Азот удобряет озерные водоросли, и они
- 31. N2 Жидкий азот в медицине Синтез аммиака Производство удобрений Синтез азотной кислоты Создание инертной среды
- 32. Домашнее задание Параграф 15, 16, записи в тетради
- 33. Использованные ресурсы https://cdn.turkaramamotoru.com/en/daniel-rutherford-7753.jpg https://cdn.turkaramamotoru.com/ru/sheele-karl-vilgelm-4172.jpg http://img00.deviantart.net/dd6a/i/2013 http://www.traces-ecrites.com/wp-content/uploads/2017/03/Jean-Antoine_Chaptal_1756-1832_comte_de_Chanteloup-768x929.jpg http://monateka.com/images/1321363.jpg https://ds02.infourok.ru/uploads/ex/1071/00009928-f441ad8d/img2.jpg https://ds04.infourok.ru/uploads/ex/0a91/00026808-ba1f3e59/img17.jpg https://avatars.mds.yandex.net/get-pdb/776003/1ec1cee5-9d14-409f-84b1-0107071f2833/s1200?webp=false http://www.uzluga.ru/potrd/1.+Деление+клетки+основа+размножения+и+роста+организмовd/75461_html_m2ede300f.jpg https://bashagroplast.com/img/upload/fea836916a5a4ff0b30ade7328fc1019.jpg http://shing.mobile9.com/download/media/536/voloxlake_tpxjaj7q.jpg https://ds04.infourok.ru/uploads/ex/121e/00024885-8a670226/img19.jpg https://sc02.alicdn.com/kf/HTB1EurjaUR1BeNjy0Fmq6z0wVXaY/Nitrogen-fertilizer-prices-urea.jpg Рудзитис
- 35. Скачать презентацию































 Галогенопроизводные. Растворимость, общие закономерности
Галогенопроизводные. Растворимость, общие закономерности Тренажер Знаки Хэ
Тренажер Знаки Хэ Аминдердің химиялық қасиеттері
Аминдердің химиялық қасиеттері Массовая доля вещества в растворе
Массовая доля вещества в растворе Валентность химических элементов. 1.Валентность водорода равна единице
Валентность химических элементов. 1.Валентность водорода равна единице Некоторые примеры использования Ферментов в промышленности
Некоторые примеры использования Ферментов в промышленности Количество вещества
Количество вещества Понятие о единичных и симметрично-равных направлениях
Понятие о единичных и симметрично-равных направлениях Каменный уголь
Каменный уголь Органическая химия Скорость химических реакций
Органическая химия Скорость химических реакций  Алкены. Химические свойства этилена
Алкены. Химические свойства этилена Свойства катализатора. Промотирование и модифицирование
Свойства катализатора. Промотирование и модифицирование Циклоалканы
Циклоалканы Жидкие кристаллы
Жидкие кристаллы Согласованное и несогласованное действие заместителей в бензольном кольце
Согласованное и несогласованное действие заместителей в бензольном кольце Фосфорное сырье. Применение и обогащение фосфорного сырья
Фосфорное сырье. Применение и обогащение фосфорного сырья Синтез олиголактозаминов – лигандов галектинов
Синтез олиголактозаминов – лигандов галектинов Методология, принципы и методы изучения МПИ
Методология, принципы и методы изучения МПИ Диктант: название алканов
Диктант: название алканов История изучения углеродных нанотрубок и композиционных материалов на основе полиуретанового связующего
История изучения углеродных нанотрубок и композиционных материалов на основе полиуретанового связующего Алкадиены. Состав и строение
Алкадиены. Состав и строение Сульфур. Характеристика елемента та утворених ним сполук, кругообіг елемента в природі
Сульфур. Характеристика елемента та утворених ним сполук, кругообіг елемента в природі Реологические свойства полимерных материалов
Реологические свойства полимерных материалов Сурьма, Sb
Сурьма, Sb G12 - класс антифризов
G12 - класс антифризов Сера, ее физические и химические свойства
Сера, ее физические и химические свойства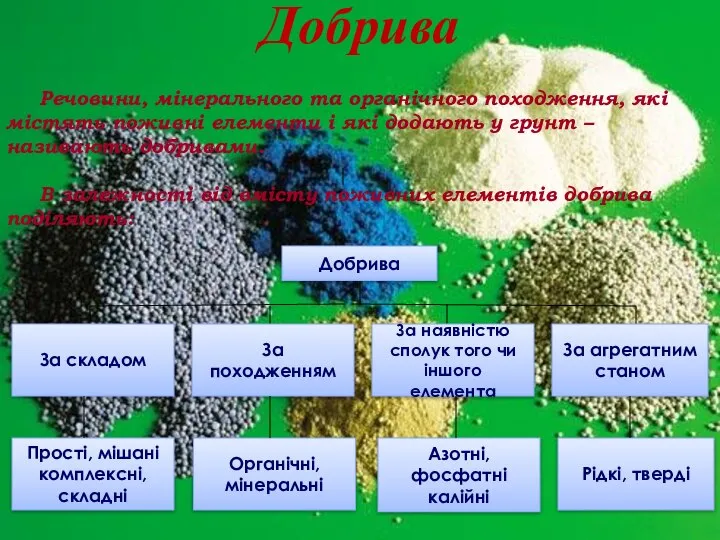 Добрива
Добрива  Пластмасса
Пластмасса