Содержание
- 2. Этилен С2Н4 CnH2n Общая формула класса
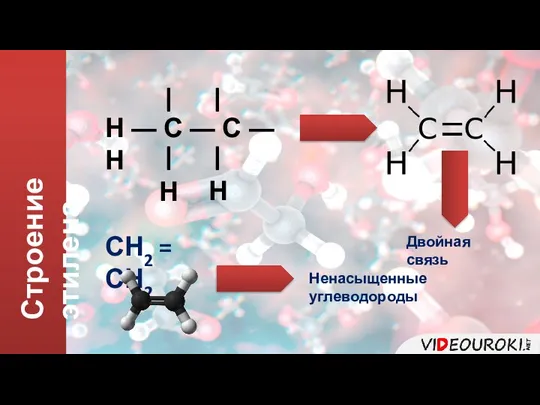
- 3. СН2 = СН2 Строение этилена Н ― С ― С ― Н | | Н Н
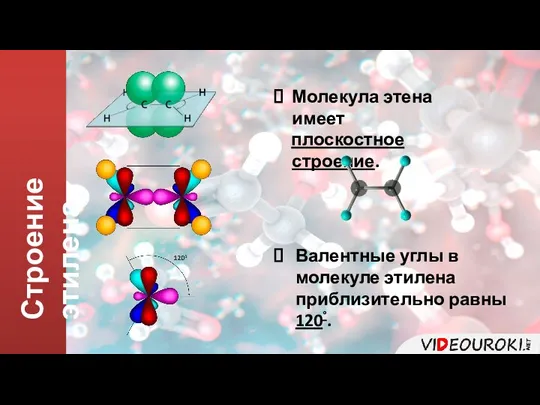
- 4. Строение этилена Молекула этена имеет плоскостное строение. Валентные углы в молекуле этилена приблизительно равны 120°.
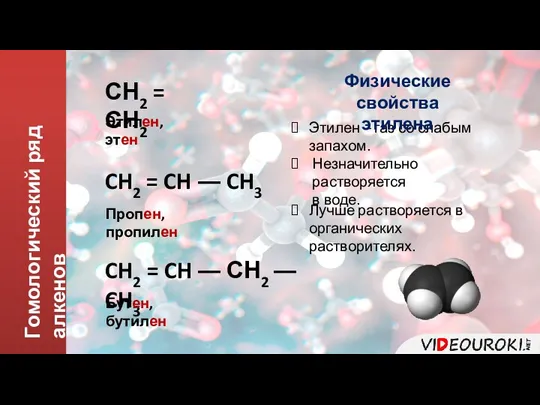
- 5. Гомологический ряд алкенов СН2 = СН2 Этилен, этен CH2 = CH ― CH3 Пропен, пропилен CH2
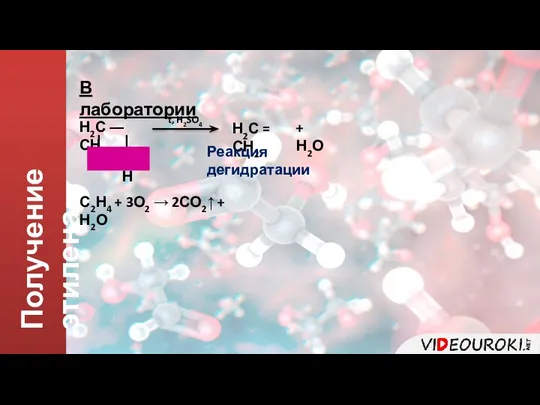
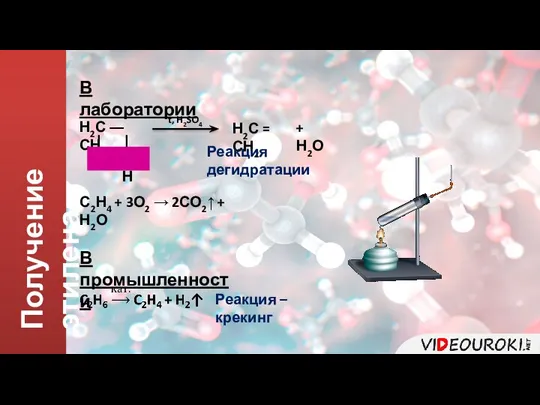
- 6. Получение этилена В лаборатории Н2С ― СН2 | | ОН Н Н2С = СН2 + Н2О
- 7. Получение этилена В лаборатории Н2С ― СН2 | | ОН Н Н2С = СН2 + Н2О
- 8. Получение этилена В лаборатории В промышленности Н2С ― СН2 | | ОН Н Н2С = СН2
- 9. Применение этилена
- 10. Получение полиэтилена Реакции полимеризации – это реакции, в которых происходит соединение молекул исходного вещества в огромную
- 11. Реакции присоединения Реакция гидратации (присоединение воды) этанол Этиловый спирт применяют: как растворитель; для производства каучуков; для
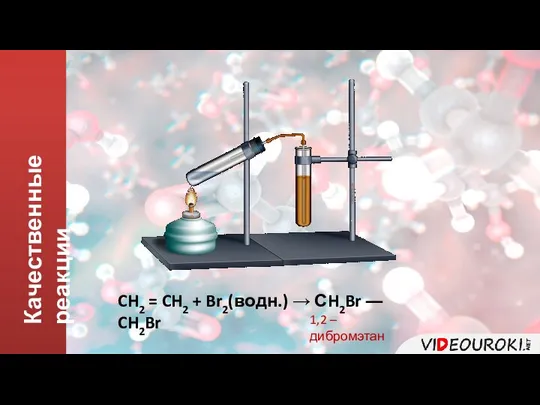
- 12. Качественные реакции CH2 = CH2 + Br2(водн.) → СH2Br ― CH2Br 1,2 – дибромэтан
- 13. Качественные реакции CH2 = CH2 + [O] + H2O → СH2OH ― CH2OH этиленгликоль
- 15. Скачать презентацию





![Качественные реакции CH2 = CH2 + [O] + H2O → СH2OH ― CH2OH этиленгликоль](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1338186/slide-12.jpg)
 Цинк. Нахождение в природе
Цинк. Нахождение в природе Аналитическая химия. Качественный анализ
Аналитическая химия. Качественный анализ Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ
Оксиды углерода (II) и (IV). Качественная реакция на углекислый газ Общая фармакология
Общая фармакология Нуклеиновые кислоты Выполнил : Росовский Алексей
Нуклеиновые кислоты Выполнил : Росовский Алексей Структурные превращения стали 15Х5М при различных режимах термической обработки
Структурные превращения стали 15Х5М при различных режимах термической обработки Живая химия
Живая химия Нанохимия и нанотехнологии. Методы и средства исследования нанообъектов. (Лекция 3)
Нанохимия и нанотехнологии. Методы и средства исследования нанообъектов. (Лекция 3) Оксиды углерода
Оксиды углерода Химия и обмен углеводов. Функции углеводов
Химия и обмен углеводов. Функции углеводов Липатова Яна
Липатова Яна Фотохимический смог
Фотохимический смог Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП
Мельхіор, Нейзильбер, застосування і склад інших сплавів для приборів в ТВКП Амиды кислот. Азо- и диазосоединения
Амиды кислот. Азо- и диазосоединения «Жизнь есть способ существования белковых тел…» (Ф.Энгельс)
«Жизнь есть способ существования белковых тел…» (Ф.Энгельс) Мои первые химические опыты
Мои первые химические опыты Яковлева Татьяна Алексеевна Ярославль, 2009 г.
Яковлева Татьяна Алексеевна Ярославль, 2009 г.  Ионообменная хроматография
Ионообменная хроматография Металлы Общая характеристика
Металлы Общая характеристика Численное моделирование развития возмущений в ударном слое на пластине в потоке смеси колебательно возбужденных газов
Численное моделирование развития возмущений в ударном слое на пластине в потоке смеси колебательно возбужденных газов Презентация по Химии "щелочные метал" - скачать смотреть бесплатно
Презентация по Химии "щелочные метал" - скачать смотреть бесплатно Chemical bonds
Chemical bonds Коллигативные свойства растворов
Коллигативные свойства растворов Аспірин Даниленко, Реутенко 11-А
Аспірин Даниленко, Реутенко 11-А  Химические свойства алкинов
Химические свойства алкинов Девиз урока: «Зажечь, увлечь и подвести»
Девиз урока: «Зажечь, увлечь и подвести»  Презентация по Химии "Галогены и их соединения" - скачать смотреть
Презентация по Химии "Галогены и их соединения" - скачать смотреть  Цемент. (9 класс)
Цемент. (9 класс)