Содержание
- 2. Жоспар Энтропия – процестер тепе- теңдігімен өз- өздігін айқындаушы шама. Термодинамикалық потенциалдар. Тепе- теңдіктің жалпы шарттары.
- 3. Бейорганикалық қосылыстар мен оларды алу реакцияларының термодинамикалық шамаларын есептеу тәсілдері. Химиялық қосылыстардың жылу сыйымдылығын, түзілу және
- 4. Энтропия мәліметтері процестердің бағытталуының бағалау қатынасы үшін қажет. ΔS > 0 өзіндік пайда болу процесс жағдайында.
- 5. Бейорганикалық заттар технологиясындағы газды-сұйықтықты күйлердегі өзгерістер термодинамикасы. Реальді газдар. Реальді газдар мен қоспалардың калыптық теңдеуі. Затттардың
- 6. Төменгі температуралар алу термодинамикасы Төменгі температуралар алу тәсілдерінің құрлымдары. Газдардың изоэнталпиялық ұлғаюы. Дифференциалдық және интегралдық және
- 7. Термодинамикалық потенциалдардың сипаттамалық функциялары Химия-технологиялық процестерді талдау жасауда шешуді қажет ететін ең негізгі мәліметтердің бірі қарастырып
- 8. Жоғарыда келтіргендей олардың арасында процестерге әсер етуші негізгі сыртқы факторларға қатысты қарастырғанда төмендегідей байланыстар бар: U
- 9. Осы теңдеулерден ішкі энергия және энтальпия өзгерістері үшін төмендегідей теңдіктер алынады: ∆U = ∆F + T∆S
- 10. ∆F бос энергиясы T = const, V = const кездегі процестерге тән. Оны Гельмгольц бос энергиясы
- 11. Осыдан төмендегідей қорытындылар жасауға болады: а) ∆F > 0; ∆G > 0 мәндерінде қарастырылып отырған процесс
- 12. Жоғарыда келтірілген термодинамикалық потенциалдар ∆U, ∆H, ∆F, ∆G өзара белгілі бір заңды байланыста. Ол байланыстарды Т,
- 13. Күрделі жүйелердегі химиялық тепе-тендік Химиялық тепе-тендік тұрақтысы. Біртекті және әртекті реакциялардың химиялық тепе-тендік тұрақтысын есептеу тәсілдері.
- 15. Скачать презентацию












 Презентация по Химии "углерод" - скачать смотреть бесплатно
Презентация по Химии "углерод" - скачать смотреть бесплатно Органическая химия. (Урок 1-2)
Органическая химия. (Урок 1-2) Основы безопасности при уничтожении химического оружия
Основы безопасности при уничтожении химического оружия Свойства простых веществ 8 класс
Свойства простых веществ 8 класс Медико-биологическое значение неметаллов. Йод
Медико-биологическое значение неметаллов. Йод Основные понятия и законы химии
Основные понятия и законы химии Эмульсии, микроэмульсии и пены. Производство и применение
Эмульсии, микроэмульсии и пены. Производство и применение Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона
Влияние пластифицирующих добавок на свойства декоративного мелкозернистого бетона Некоторые аспекты физической и коллоидной химии
Некоторые аспекты физической и коллоидной химии Биосинтез липидов
Биосинтез липидов Металлокомплексный катализ. (Лекция 16)
Металлокомплексный катализ. (Лекция 16) Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9
Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9 Амедео Авогадро
Амедео Авогадро Физические явления в химии
Физические явления в химии Каучук Органическая химия 10 класс. Школьная коллекция
Каучук Органическая химия 10 класс. Школьная коллекция Скорость химической реакции
Скорость химической реакции Химический турнир
Химический турнир Процессы нитрозирования и основные реакции диазосоединений
Процессы нитрозирования и основные реакции диазосоединений Калитина Тамара Михайловна учитель экологии, биологии МОУ СОШ №3 и учитель химии МОУ СОШ №2 с.Александров-Гай Саратовской обла
Калитина Тамара Михайловна учитель экологии, биологии МОУ СОШ №3 и учитель химии МОУ СОШ №2 с.Александров-Гай Саратовской обла Классификация углеводов. Глюкоза
Классификация углеводов. Глюкоза Синтез наноматериалов на границах раздела жидкость - жидкость и жидкость - воздух. Метод Ленгмюра - Блоджетт
Синтез наноматериалов на границах раздела жидкость - жидкость и жидкость - воздух. Метод Ленгмюра - Блоджетт Колообіг речовин у природі
Колообіг речовин у природі  ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО
ОЧКАСОВ ЕВГЕНИЙ МИХАЙЛОВИЧ ПРЕПОДАВАТЕЛЬ ХИМИИ И БИОЛОГИИ ГОСУДАРСТВЕННОГО АВТОНОМНОГО ОБРАЗОВАТЕЛЬНОГО УЧРЕЖДЕНИЯ СРЕДНЕГО Нефть и способы её переработки
Нефть и способы её переработки Метод окислительно-восстановительного титрования
Метод окислительно-восстановительного титрования Обмен фосфолипидов и стероидов
Обмен фосфолипидов и стероидов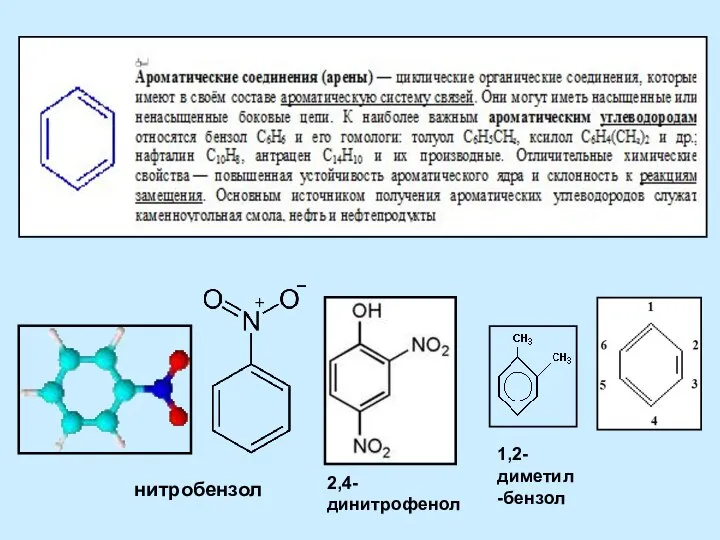 Ароматические соединения (арены)
Ароматические соединения (арены) Максимально очищенные фитопрепараты. Технология и стандартизация
Максимально очищенные фитопрепараты. Технология и стандартизация