Содержание
- 2. В ПСЭ 30 р-элементов, у которых заполняется электронами р-подуровень внешнего электронного уровня. Жизненно необходимы: C, N,
- 3. Углерод Электронная формула: 6С 1s22s22p2→C* 1s22s12p3, с.о.=+4, валентность во всех органических соединениях равна 4.
- 4. Углерод – органоген №1, так как: 1. Атомы углерода способны соединяться друг с другом, образуя цепи,
- 5. 3. Среднее значение электроотрицательности углерода 2,5 позволяет ему образовывать связи и с более и менее электроотрицательными
- 6. Химические превращения углерода и его соединений: C+2H2=CH4 метан 2C+Ca=CaC2 карбид кальция 2C+N2= (CN)2 дициан, летуч, токсичен
- 7. Fe2+ +6HCN= [Fe(CN)6]4-+6H+; гексацианоферрат (II), прочный комплексный ион 2C+O2=2CO угарный газ CO+Cl2=COCl2 фосген, летуч, токсичен C+O2=CO2
- 8. Фотосинтез, происходит в растительных клетках с участием хлорофилла: 6CO2+6H2O=C6H12O6+6O2 глюкоза
- 9. Гидрокарбонатная буферная система организма: CO2+H2O⇔H2CO3⇔H++HCO3 H2CO3+NaOH=NaHCO3+H2O гидрокарбонат натрия. питьевая сода
- 10. H2CO3+2NaOH=Na2CO3+2H2O карбонат натрия Na2CO3+CaCl2=CaCO3↓+2NaCl CaCO3↓+H2O+CO2=Ca(HCO3)2 гидрокарбонат кальция, растворимое соединение
- 11. ω(С) в организме =21%, масса 14кг
- 12. Топография: входит в состав всех клеток и тканей, так как является основой белков, жиров, углеводов, нуклеиновых
- 13. Физиологические функции и токсичность соединений углерода.
- 14. Углекислый газ, СО2 бесцветный газ, тяжелее воздуха, под давлением легко сжижается, может быть получен в твердом
- 15. В ходе метаболизма образуется 13 моль СО2 в сутки в результате окисления белков, жиров, углеводов: Участвует
- 16. 3. Участвует в реакциях карбоксилирования и декарбоксилирования 4. Компонент гидрокарбонатной буферной системы
- 17. 5. В закрытых помещениях при увеличении объемной доли ϕ(СО2) до 10% развивается ацидоз, одышка, так как
- 18. Угарный газ, СО в сутки образуется 10 мл в ходе метаболизма в процессе кроветворения. Продукт неполного
- 19. В окружающей среде источником СО являются выхлопные газы автомобилей, промышленные газовые отходы, табачный дым.
- 20. Токсическое действие СО: 1. Уменьшает кислородную емкость крови, связывая гемоглобин, ⇒прекращается перенос кислорода, наступает асфиксия: HHb
- 21. Главная мишень СО – миоглобин мышц; резко уменьшается содержание О2 в мышцах, нарушается работа мышечного аппарата.
- 22. Нарушает кислотно-щелочное равновесие и электролитный состав биожидкостей в клетках: уровень натрия повышается ↑[Na+], уровень калия понижается
- 23. Причиной отравления угарным газом является курение. Содержание карбонилгемоглобина в крови курильщиков, выкуривающих пачку сигарет в день,
- 24. Причиной более сильного отравления может быть преждевременное закрытие заслонки печи или вдыхание выхлопных газов автомобиля.
- 25. При легких отравлениях (содержание HHbCO в крови 10-15%) наблюдается головная боль, слабость, тошнота.
- 26. При отравлениях средней степени (содержание HHbCO в крови 25-30%) нарушается координация движений, появляется синюшность кожи и
- 27. При тяжелых отравлениях (содержание HHbCO в крови 60% и более) происходит потеря сознания, судороги. Смертельные концентрации
- 28. Лечение при отравлении СО проводят в барокамерах, увеличивая р(О2) до 3 атм. для выведения СО из
- 29. Цианиды (CN-) в организме образуются при окислении аминокислот под действием аминооксидаз. В окружающую среду попадают из
- 30. Токсическое действие цианидов: 1. Ферменты, содержащие железо (каталаза, пероксидаза, цитохромы дыхательной цепи), инактивируются, прекращается перенос электронов
- 31. 2. Главная мишень цианидов – мозг, так как в печени происходит процесс: CN-+S → SCN- роданид,
- 32. Роданистоводородная кислота, HCNS Не токсична, содержится в слюне, обладает бактерицидным действием.
- 33. Лекарственные препараты углерода: 1. С – активированный уголь – адсорбент при метеоризме, пищевых интоксикациях, отравлениях. 2.
- 34. 3. СО2(твердый) – в дерматологии для вымораживания. 4. NaHCO3 – питьевая сода, антацидное: NaHCO3- + H+
- 35. Азот Электронная формула: 7N 1s22s22p3
- 37. Окислительно-восстановительные свойства соединений азота Восстановительные свойства: (с.о.=-3, низшая): NH3+O2→N2+H2O 4NH3+5O2 4NO+6H2O 2NO+O2=2NO2 4NO2+O2+2H2O=4HNO3.
- 38. 2. Окислительно-восстановительная двойственность нитритов (с.о.=+3, промежуточная): восстановительные свойства: KNO2+H2O2=KNO3+H2O; окислительные свойства: 2KNO2+2KI+2H2SO4=I2+2NO+2K2SO4+2H2O.
- 39. 3. Окислительные свойства азотной кислоты (с.о.=+5, высшая). 8HNO3+3Cu→3Cu(NO3)2+2NO+4H2O разб.
- 40. Физиологическая роль и токсичность соединений азота.
- 41. Аммиак, NH3 - метаболический образуется при дезаминировании аминокислот.
- 42. Причины токсического действия: 1. Легко проходит через мембраны, действует на мозг.
- 43. 2. Электронодонор (ЭД), конкурент биогенных лигандов Lб , ингибирует ферменты: NH3+MLб→[MNH3]+Lб Связывание аммиака в нетоксичные соединения:
- 44. Из-за образования Н+ рН уменьшается, для нейтрализации мобилизуется Na+, с ним удаляется определенное количество воды, поэтому
- 45. Оксид азота (IV), NO2 источники в окружающей среде – автотранспорт, металлургия, производство HNO3.
- 46. Токсическое действие NO2: 1. Поражает слизистую носоглотки, открывая путь аллергенам. 2. При взаимодействии NO2 с влажной
- 47. 3. В крови оксид азота (IV) образует нитриты и нитраты, которые в организме восстанавливаются до нитритов.
- 48. 4. В желудочно-кишечном тракте азотистая кислота взаимодействует со вторичными аминами с образованием нитрозаминов, которые являются канцерогенами:
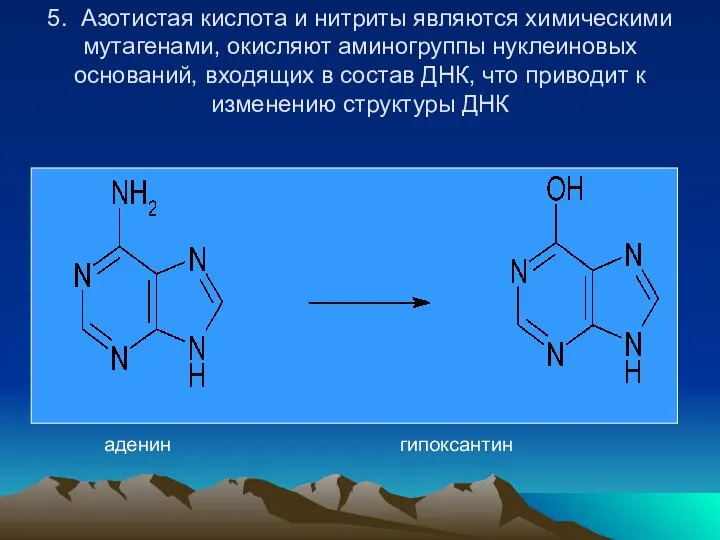
- 49. 5. Азотистая кислота и нитриты являются химическими мутагенами, окисляют аминогруппы нуклеиновых оснований, входящих в состав ДНК,
- 50. 6. NO2 является компонентом фотохимического смога. В настоящее время в связи с увеличением числа транспортных средств
- 51. Для образования смога необходимы следующие условия: - интенсивное солнечное излучение; - наличие в воздухе углеводородов и
- 52. Эти компоненты фотохимического смога образуются при горении бензина в двигателях внутреннего сгорания.
- 53. Фотохимический смог При недостатке кислорода: свет NO2 → NO+O При избытке кислорода: O2+O→O3
- 54. Взаимодействие этих продуктов под действием солнечной радиации приводит к образованию сильно токсичных пероксиацилнитратов (ПАН) RC(O)H+O+NO2→RC(O)O-O-NO2. пары
- 55. ПАН вызывают сильное раздражение слизистых оболочек дыхательных путей и глаз, так как при контакте с водой
- 56. Сохранение смоговой ситуации приводит к повышению заболеваемости и смертности прежде всего детей и пожилых людей. Смог
- 57. Лекарственные препараты: 1. NH4Cl- мочегонное, для коррекции алкалоза (рН 2. N2- жидкий азот, лечение кожных заболеваний.
- 58. 4. NH4OH (10%-й водный раствор)- нашатырный спирт, возбуждающее средство при обмороках. 5. AgNO3 - “ляпис”, прижигающее
- 59. 6. R-O-NO2, R-O-NO - органические и неорганические нитраты и нитриты, например, нитроглицерин, улучшают коронарное кровообращение, для
- 60. Фосфор Электронная формула: 15P 1s22s22p63s23p3,с.о.=-3, 0, +3, +5
- 61. Химические превращения фосфора и его соединений: 3Са+2P=Ca3P2 фосфид кальция Ca3P2+6H2O=3Ca(OH)2+2PH3 фосфин, слабое основание PH3+HI=PH4I
- 62. 2PH3+4O2=P2O5+3H2O 4P+3O2=2P2O3 оксид фосфора (III), кислотный оксид, восстановитель P2O3+3H2O=2H3PO3 фосфористая кислота, слабая кислота
- 63. P2O3+O2=P2O5 оксид фосфора (V), кислотный оксид P2O5+3Н2O=2H3PO4 фосфорная кислота, трехосновная кислота средней силы H3PO4+NaOH=NaH2PO4+H2O дигидрофосфат натрия,
- 64. H3PO4+2NaOH=Na2HPO4+2H2O гидрофосфат натрия, кислая соль H3PO4+3NaOH=Na3PO4+3H2O. фосфат натрия, средняя соль
- 65. ω(Р) в организме = 1%, масса фосфора 650 г.
- 66. Топография: костная и зубная ткань в виде гидроксиапатита Ca5(PO4)3OH и фторапатита Ca5(PO4)3F; в мозге, нервных клетках,
- 67. Биороль фосфора: Влияет на кроветворение. Строительный материал костной и зубной ткани. Влияет на состояние нервной системы:
- 68. 4. Биосинтез идет через обязательную стадию фосфорилирования мономеров. 5. АТФ – аккумулятор и источник энергии в
- 69. Фосфорорганические соединения, содержащие связь С―Р, являются сильными ядами нервно-паралитического действия, входят в состав боевых отравляющих веществ,
- 70. Суточная потребность – 1,3 г фосфора. Фосфор содержится в рыбе, мясе, яйцах, овощах. Дефицит фосфора вызывает
- 71. Лекарственные препараты: АТФ (Na-соль) – при мышечной дистрофии, стенокардии. 2. Ca-глицерофосфат – нормализует функции нервной системы.
- 72. Фитин ( органический препарат фосфора) – стимулирует кроветворение, усиливает рост и развитие костной ткани. H3PO4 –
- 73. Сера Электронная формула: 16S 1s22s22p63s23p4
- 75. Окислительно-восстановительные свойства соединений серы
- 76. Сероводород, с.о.=-2, низшая, восстановитель: 2H2S+O2=2H2O+2S; H2S+I2=2HI+S; 2H2S+3O2=2SO2+2H2O.
- 77. Оксид серы (IV), с.о.=+4, промежуточная, ОВ-двойственность: SO2+Вr2+2H2O=2HВr+H2SO4 –восстановительные свойства; SO2+2H2S=3S+2H2O – окислительные свойства.
- 78. Серная кислота, с.о.=+6, высшая, окислительные свойства: 2H2SO4+C=CO2+2SO2+2H2O 2H2SO4(конц.)+Cu=CuSO4+SO2+2H2O.
- 79. ω(S) в организме = 0,16%, масса 115г, суточная потребность 4-5г.
- 80. Топография: белки (особенно кератин волос и ногтей), костная и нервная ткань, инсулин; сера входит в состав
- 81. Биороль и токсичность соединений серы: 1. Сера в виде SH- групп формирует активный центр ферментов, входит
- 82. 3. RSH в клетках выполняет защитную функцию: водородсульфидные группы связывают активные радикалы при облучении: RS–H +OH
- 83. 5. Оксиды серы токсичны, являются компонентами химического смога, при их участии образуются «кислотные дожди»: SO2+H2O=H2SO3 SO3+H2O=H2SO4
- 84. При выпадении кислотных дождей закисляются почвы ⇒ снижается урожайность; снижается рН воды в природных водоемах⇒ гибнет
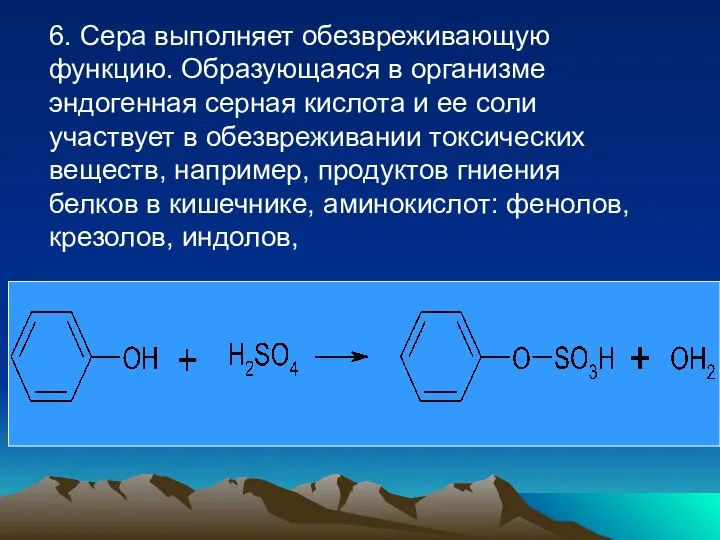
- 85. 6. Сера выполняет обезвреживающую функцию. Образующаяся в организме эндогенная серная кислота и ее соли участвует в
- 86. лекарственных препаратов и продуктов их метаболизма, при этом образуются нетоксичные хорошо растворимые эфиры, которые легко выводятся
- 87. Лекарственные препараты: Na2SO4∙10H2O – слабительное средство; 2. MgSO4∙7H2O – гипотензивное, желчегонное, слабительное; 3. CuSO4∙5H2O, ZnSO4∙7H2O –антисептические.
- 88. 4. ВaSO4 – контрастное вещество при рентгенологии желудка и пищевода; 5. Тиосульфат натрия Na2S2O3 используют для
- 89. как универсальный антидот при отравлении хлором, йодом, цианидами, солями тяжелых металлов: Na2S2O3+Cl2+H2O=2HCl+Na2SO4+S↓, Na2S2O3+I2=2NaI+Na2S4O6, Na2S2O3+KCN=KSCN+Na2SO3, PbCl2+Na2S2O3+H2O=PbS↓+2HCl+Na2SO4.
- 90. Биороль физиологически активных галогенов
- 91. Хлор Электронная формула: 17Cl 1s22s22p63s23p53d0
- 93. ω (Cl) = 0.15%, масса 100 г, макроэлемент, жизненно необходимый внеклеточный элемент.
- 94. Топография: все органы и ткани, биологические жидкости. В организме находится в виде гидратированных ионов Cl– ,
- 95. Биороль Cl-: 1.Активирует ферменты ( пепсин желудочного сока, катализирующий гидролиз белков). 2.Обеспечивает ионные потоки через клеточные
- 96. 3.Поддерживает постоянство осмотического давления. 4.Необходим для выработки соляной кислоты желудочного сока, которая вырабатывается под действием ферментов
- 97. Соляная кислота участвует в процессе переваривания, а также выполняет барьерную функцию: уничтожает болезнетворные бактерии.
- 98. Соединения хлора: Cl2 –тяжелый газ, высокотоксичен (БОВ) , предельно допустимая концентрация хлора в воздухе 0.001 мг/л
- 99. Хлор используется для обеззараживания питьевой воды: Cl2+H2O →HCl+ HClO HClO →HCl+O
- 100. [O] и HClO - сильные окислители, оказывают дезинфицирующее и отбеливающее действие. HClO действует и как окислитель,
- 101. Таким же действием обладает хлорная (белильная) известь – смешанная соль соляной и хлорноватистой кислот, которая образуется
- 102. На влажном воздухе Ca(OСl2) гидролизуется с образованием HClO: Ca(OСl2) +H2O → Ca(OH)Cl + HClO
- 103. Лекарственные препараты: HCl - 8%-ный раствор, при пониженной кислотности желудочного сока; 2. NaCl – физиологический и
- 104. Фтор Электронная формула: 9F 1s22s22p5
- 105. Степень окисления постоянная: -1 ω(F)=10 –5 %, масса 7мг, микроэлемент, примесный элемент.
- 106. Топография: зубная эмаль (99.4%), ногти, костная ткань. В организме находится в виде труднорастворимого неорганического соединения –
- 107. Для поддержания постоянного содержания фтора в организме необходимо обогащение питьевой воды фтором до концентрации 1 мг/л.
- 108. При недостатке фтора (содержание в воде Ca5(PO4)3OH +7H+ → 5Ca2 ++ 3H2PO4–+H2O
- 109. Для предотвращения кариеса используют фторированные зубные пасты, содержащие NaF: Ca5(PO4)3OH + F–→Ca5(PO4)3F+ OH– Происходит восстановление эмали,
- 110. При избытке фтора (содержание в воде >1,2 мг/л )возникает заболевание –флуороз (фтороз), зубная эмаль становится хрупкой,
- 112. Бром Электронная формула: 35Br 3d104s24p54d0
- 113. Степень окисления от–1 до +7. ω(Br)=10 –5 %, масса 7мг, микроэлемент, примесный.
- 114. Топография: гипофиз и другие железы внутренней секреции, в организме находится в виде гидратированных ионов Br –
- 115. Биороль брома: способствует восстановлению равновесия между процессами возбуждения и торможения, усиливает активность коры надпочечников, угнетает функцию
- 116. Лекарственные препараты: NaВr, KВr, NH4Вr при расстройствах высшей нервной деятельности
- 117. Иод Электронная формула внешнего энергетического уровня: 53I 4d105s25p5
- 118. Степень окисления от–1 до +7. ω(I)= 4∙10 –5 %, масса 25мг, микроэлемент, незаменимый.
- 119. Топография: Щитовидная железа, кровь. В щитовидной железе йод находится в связанном виде – в виде гормонов
- 120. В крови содержание йода поддерживается постоянным 10–4- 10–5%. Это йодное зеркало крови.
- 121. Суточная потребность 0,2 мг. Йод содержится в небольшом количестве в морской капусте, хурме, а также в
- 122. Биороль йода: 1.Участвует в синтезе гормонов щитовидной железы тироксина и трийодтиронина. 2.Влияет на синтез и обмен
- 123. При недостатке I– наблюдается пониженная функция щитовидной железы (гипотиреоз), что связано с уменьшением ее способности накапливать
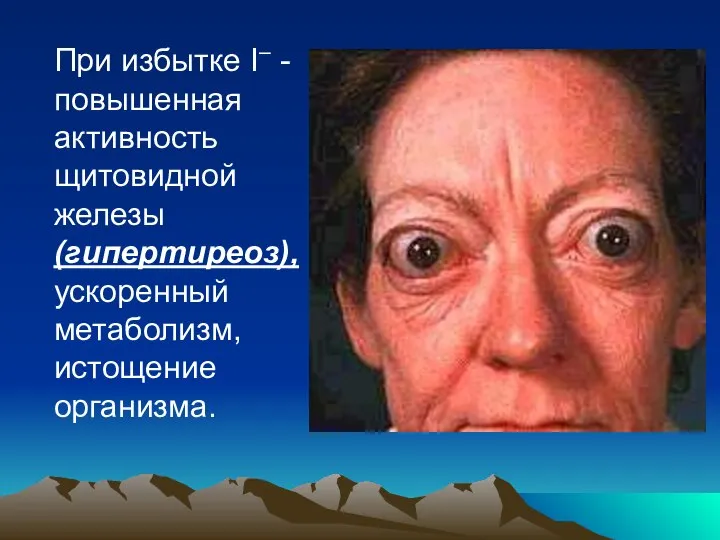
- 126. При избытке I– - повышенная активность щитовидной железы (гипертиреоз), ускоренный метаболизм, истощение организма.
- 127. Лекарственные препараты: I2 – 5-10%-ный раствор, антисептик (окисляет–SH и -NH2 группы белков микробных клеток). 2. KI,
- 129. Скачать презентацию





![Fe2+ +6HCN= [Fe(CN)6]4-+6H+; гексацианоферрат (II), прочный комплексный ион 2C+O2=2CO угарный газ](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396240/slide-6.jpg)



































![2. Электронодонор (ЭД), конкурент биогенных лигандов Lб , ингибирует ферменты: NH3+MLб→[MNH3]+Lб](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396240/slide-42.jpg)






















































![[O] и HClO - сильные окислители, оказывают дезинфицирующее и отбеливающее действие.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1396240/slide-99.jpg)

























 Презентация по химии Биополимеры и их компоненты
Презентация по химии Биополимеры и их компоненты  Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Харчові добавки Е-числа
Харчові добавки Е-числа  Аминокислоты. Белки
Аминокислоты. Белки Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5)
Материаловедение. Влияние нагрева на структуру деформированного металла. (Тема 5) Тірі ағзада жүретін процесстер – физика-химиялық интерпретация
Тірі ағзада жүретін процесстер – физика-химиялық интерпретация Сarbonyl compounds. Carboxylic acids. Lipids
Сarbonyl compounds. Carboxylic acids. Lipids Современные способы защиты ОТТ
Современные способы защиты ОТТ Электроотрицательность (ЭО). Ковалентная связь
Электроотрицательность (ЭО). Ковалентная связь Этил спирті және оның адам ағзасына әсері
Этил спирті және оның адам ағзасына әсері Основные сведения о металлах и сплавах
Основные сведения о металлах и сплавах Мило. Мийні засоби
Мило. Мийні засоби Кристаллография и основы кристаллохимии. Лекция 5
Кристаллография и основы кристаллохимии. Лекция 5 Определение температуры. Абсолютная температура
Определение температуры. Абсолютная температура Повітря. Основні забруднювачі: теплоенергетика, кольорова та чорна металургія, використання фреонів, підприємства будматеріалі
Повітря. Основні забруднювачі: теплоенергетика, кольорова та чорна металургія, використання фреонів, підприємства будматеріалі Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов
Влияние параметров технологического режима на удельную производительность и устойчивую работу реакторов Окислительно-восстановительные реакции
Окислительно-восстановительные реакции В МИРЕ КРИСТАЛЛОВ Выполнила: ученица 4 класса Константинова Мария Научный руководитель: Аникина Валентина Ивановна уч
В МИРЕ КРИСТАЛЛОВ Выполнила: ученица 4 класса Константинова Мария Научный руководитель: Аникина Валентина Ивановна уч Презентация по Химии "Природные источники углеводородов. Нефть и способы ее переработки" - скачать смотреть
Презентация по Химии "Природные источники углеводородов. Нефть и способы ее переработки" - скачать смотреть  Описание и сравнение признаков 2-3 тел и веществ
Описание и сравнение признаков 2-3 тел и веществ Презентация Природные источники углеводородов
Презентация Природные источники углеводородов  Химическая связь
Химическая связь Нафта Походження,переробка, використання
Нафта Походження,переробка, використання  Плотнейшие упаковки одинаковых сфер
Плотнейшие упаковки одинаковых сфер Кислоты
Кислоты Лекарственные препараты
Лекарственные препараты  Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь
Алканы. Состав, строение, свойства и химические превращения. Экологические последствия. Синтезы генетическая связь Нанохимия, как наука
Нанохимия, как наука