Содержание
- 2. СЕРОВОДОРОД Бесцветный газ с запахом «тухлых яиц». Тяжелее воздуха. Ядовит (блокирует металлопротеидные центры ферментов, гемоглобина). Хорошо
- 3. СЕРОВОДОРОД В ПРИРОДЕ Сероводородные ванны Сероводородные минеральные воды Сероводород в районах вулканов Сероводород в Чёрном море
- 5. ХИМИЧЕСКИЕ СВОЙСТВА СЕРОВОДОРОДА Восстановительные (S-2 – минимальная степень окисления) Горение: 2H2S + 3O2 →2SO2+2H2O Неполное окисление:
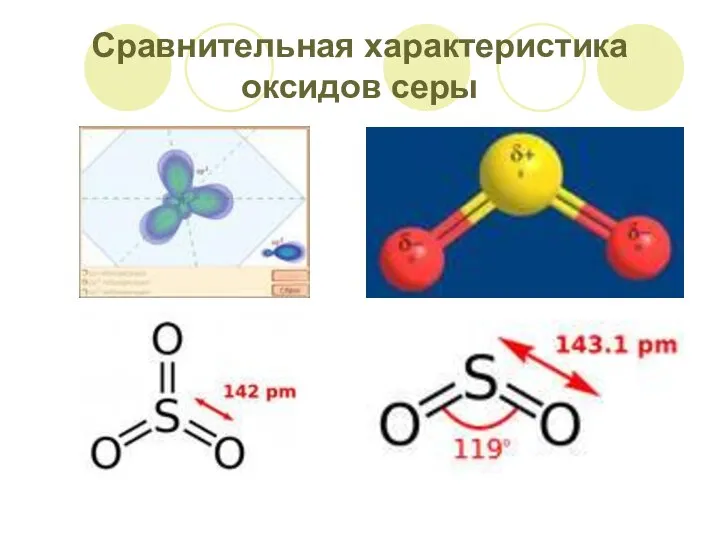
- 6. Сравнительная характеристика оксидов серы
- 7. Сравнительная характеристика оксидов серы SO2 – сернистый газ, сернистый ангидрид Бесцветный газ с удушливым запахом «горелых
- 8. Способы получения оксидов серы SO2 В промышленности – обжиг пирита: 4FeS2 + 11O2 → 2Fe2O3+8SO2 В
- 9. Свойства кислотных оксидов Сернистый ангидрид SO2+NaOH→NaHSO3 SO2+2NaOH→Na2SO3 + H2O SO2 + H2O ↔ H2SO3 SO2 +
- 10. Окислительно-восстановительная активность оксидов серы SO2 – и восстановитель, и окислитель, так как сера в промежуточной степени
- 11. Сернистый газ используется для отбеливания тканей, но его присутствие в атмосфере чрезвычайно опасно для здоровья
- 12. Серная кислота Сернокислотное озеро вулкан Горелый на Камчатке
- 13. Обугливающее действие концентрированной серной кислоты
- 14. Разрушение бумаги под действием серной кислоты
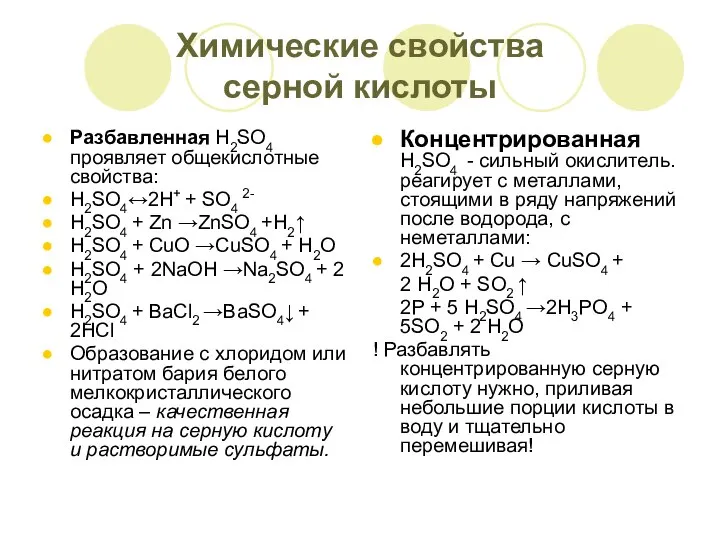
- 15. Химические свойства серной кислоты Разбавленная H2SO4 проявляет общекислотные свойства: H2SO4↔2Н+ + SO4 2- H2SO4 + Zn
- 16. Серная кислота – «хлеб химической промышленности» Сернокислотный завод Цистерны с серной кислотой
- 17. Производство серной кислоты 1-я стадия – обжиг пирита (обжиговая печь) 4FeS2 + 11O2 → 2Fe2O3+8SO2 2-я
- 18. Производство серной кислоты
- 20. Скачать презентацию














 Гликогенді және кетогенді аминқышқылдары. Биологиялық рөлі
Гликогенді және кетогенді аминқышқылдары. Биологиялық рөлі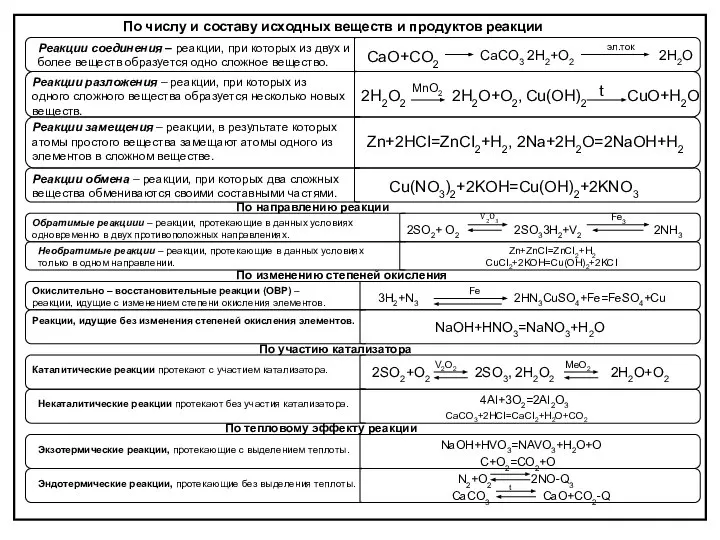 Классификация реакций. Таблица
Классификация реакций. Таблица Ионообменная хроматография
Ионообменная хроматография Муравьиная и уксусная кислоты
Муравьиная и уксусная кислоты galogeny
galogeny Методы выращивания GaAs. Сравнение
Методы выращивания GaAs. Сравнение Растворение. Растворимость веществ в воде
Растворение. Растворимость веществ в воде Сабақтың тақырыбы: донорлыакцепторлы байланыс. Комплексті қосылыстар
Сабақтың тақырыбы: донорлыакцепторлы байланыс. Комплексті қосылыстар Удивительный мир кристаллов
Удивительный мир кристаллов Объединение по интересам “тайны вещества”
Объединение по интересам “тайны вещества” Определение расхода воздуха на горение, количество и температуру продуктов
Определение расхода воздуха на горение, количество и температуру продуктов Карбоновые кислоты
Карбоновые кислоты Гетероорганические углеводороды нефти и асфальто-смолистые вещества
Гетероорганические углеводороды нефти и асфальто-смолистые вещества Натрий. Роль натрия в организме
Натрий. Роль натрия в организме Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола
Синтез 2,4-диметил-3,5-ди(этоксикарбонил)пиррола Принцип Паули. Периодическая система элементов Д.И. Менделеева
Принцип Паули. Периодическая система элементов Д.И. Менделеева Альдегидтер және кетондар
Альдегидтер және кетондар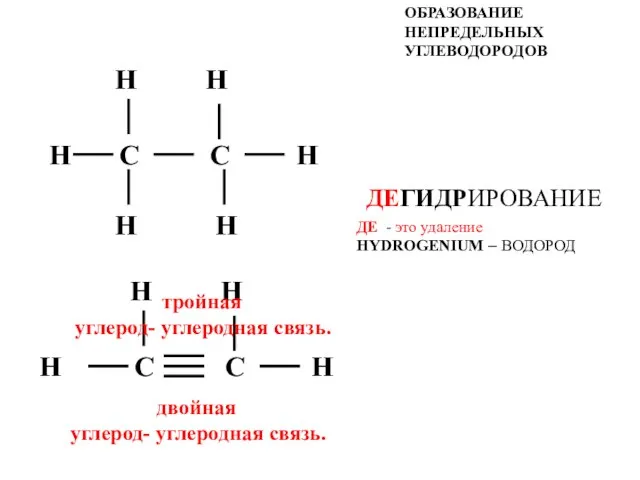 Образование непредельных углеводородов
Образование непредельных углеводородов Химический элемент свинец
Химический элемент свинец Проект на тему «Вуглеводні. Класифікація»
Проект на тему «Вуглеводні. Класифікація»  Презентация по Химии "Драгоценные и поделочные камни - соединения кремния" - скачать смотреть
Презентация по Химии "Драгоценные и поделочные камни - соединения кремния" - скачать смотреть  Вещества. Превращения и свойства веществ
Вещества. Превращения и свойства веществ Взаимодействие солей аммония со щелочами
Взаимодействие солей аммония со щелочами Кремнийдің құрамы, құрылысы және қасиеттері
Кремнийдің құрамы, құрылысы және қасиеттері Реакции ионного обмена
Реакции ионного обмена Исследование минералов в параллельном свете с одним поляризатором
Исследование минералов в параллельном свете с одним поляризатором Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.
Фотометрический анализ III курс, д/о Лекция№1 Преподаватель Ельчищева Ю.Б.  Общая химия. Химическая термодинамика. Первый закон термодинамики. Термохимия
Общая химия. Химическая термодинамика. Первый закон термодинамики. Термохимия