Содержание
- 2. Лекции-9 Семинары-12 Самостоятель-ная работа
- 3. Химическая термодинамика раздел химии, изучающий взаимные превращения энергии, теплоты и работы в термодинамических системах разных типов.
- 4. Лекция 1 Первый закон термодинамики. Термохимия
- 5. П Л А Н 1.1 Основные понятия химической термодинамики 1.2 Первый закон термодинамики 1.3 Термохимия
- 6. 1.1 ЭНЕРГИЯ – способность совершать работу (кДж, ккал) 1 ккал = 4,184 кДж
- 7. Виды энергии Потенциальная -энергия взаимодействия Кинетическая -энергия движения
- 8. По видам совершаемых работ различают: химическую, электрическую, световую,
- 9. По видам совершаемых работ различают: механическую, звуковую, поверхностную, и др. виды энергии
- 10. Работа (А) – это способ превращения одного вида энергии в другой ее вид. Различают: (а) работу
- 11. Важнейшими видами полезной работы в организме являются: 1) механическая работа – выполняется при сокращении мышц;
- 12. 2) осмотическая работа почек и цитоплазматических мембран по переносу веществ против градиента концентраций,
- 13. 3) электрическая работа нервной ткани и мозга по переносу заряженных частиц.
- 14. ТЕПЛОТА (Q) – перенос энергии между двумя телами, имеющими разные температуры.
- 15. ТЕРМОДИНАМИЧЕСКАЯ СИСТЕМА – это тело или группа тел, отделенных от окружающей среды термодинамической оболочкой, которая может
- 17. ОТКРЫТЫЕ СИСТЕМЫ обмениваются с окружающей средой и веществом, и энергией (живая клетка, человек и др. биосистемы);
- 18. За 40 лет человек потребляет ~40 т воды, 12 млн. л кислорода, 10 тысяч плиток шоколада
- 19. ЗАКРЫТЫЕ СИСТЕМЫ обмениваются с окружающей средой только энергией; обмен веществом отсутствует (запаянная ампула)
- 20. ИЗОЛИРОВАННЫЕ СИСТЕМЫ не обмениваются с окружающей средой ни веществом, ни энергией. Они не существуют в природе
- 21. Термодинамическое описание системы включает: набор термодинамических параметров: Т, р, V, ν, m, изменение которых свидетельствует о
- 22. набор термодина-мических функций, описывающих способность системы совершать работу.
- 23. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ Функции Функции состояния процесса Их изменения зависят от начального и конечного состояния системы и
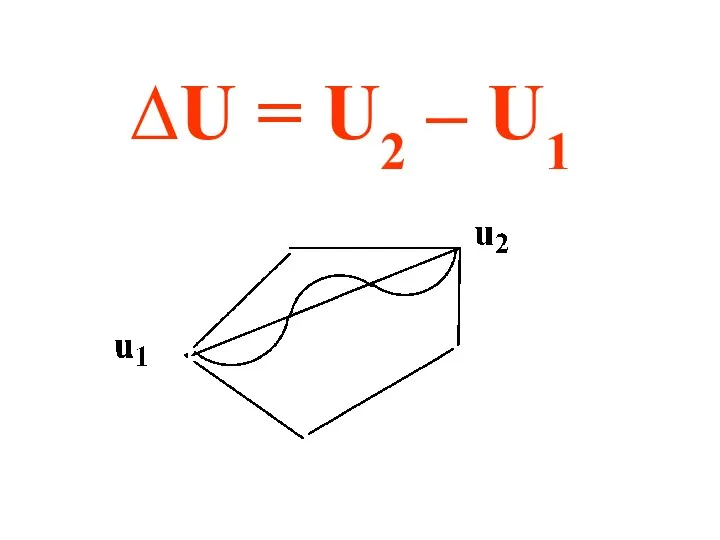
- 24. Примером функции состояния является внутренняя энергия системы (U) – это совокупность потенциальной и кинетической энергии всех
- 25. ∆U = U2 – U1
- 26. 1.2 Первый закон термодинамики является выражением всеобщего закона сохранения энергии: энергия не создается и не разрушается,
- 27. В организме человека превращение одного вида энергии в другой сопровождается совершением работы: Химическая энергия пищи работа
- 28. Химическая энергия работа нервной ткани Электрическая энергия
- 29. Звуковая энергия Электрическая энергия Работа внутреннего уха
- 30. Световая энергия Электрическая энергия Работа сетчатки глаза
- 31. Первый закон термодинамики не имеет доказательств, но является результатом опыта, накопленного человечеством. Ярким доказательством его справедливости
- 32. Вечный двигатель первого рода – это машина, совершающая работу без поглощения энергии из окружающей среды
- 33. Первые проекты вечного двигателя появились в 13 веке В 1775 году Парижская Академия Наук приняла решения
- 34. Вечный двигатель Иоганна Эрнста Элиаса Беслера (1680-1745)
- 36. Математическое выражение первого закона термодинамики для различных типов систем: 1. Внутренняя энергия изолированной системы постоянна: U
- 37. 2. Теплота, подводимая к закрытой системе, расходуется на увеличение ее внутренней энергии и на совершение работы:
- 38. Для изобарного процесса (р = const ), при условии А΄ = 0 Q= ΔU + pΔV
- 39. Соответственно Qр = H2 – H1 = ΔH, где ΔH – тепловой эффект изобарного процесса для
- 40. 3. Внутренняя энергия открытой системы возрастает как при ее нагревании, так и при увеличении количества вещества
- 41. 1.3 Термохимия – раздел химической термодинамики, изучающий тепловые эффекты химических реакций. Тепловые эффекты (теплота) химической реакции
- 42. ΔrH0298 – это стандартная теплота реакции т.е. теплота, измеренная при стандартных условиях: Т = 298 К,
- 43. Уравнения химических реакций, в которых указаны тепловые эффекты и агрегатное состояние веществ называются термохимическими уравнениями.
- 44. N2O4 (ж) → 2 NO2 (г), ΔrH0 = + 58,4 кДж O2(г) + 2H2S (г)→3S (к)
- 45. Герман Гесс (1802 - 1850) Центральным законом термохимии является закон, сформулированный в 1840 г. профессором Санкт-Петербургского
- 46. Тепловой эффект химической реакции, протекающей при постоянном давлении или объеме, зависит от состояния исходных веществ и
- 47. Закон Гесса есть следствие первого закона термодинамики. Поскольку энтальпия является функцией состояния, то ее изменение определяется
- 48. С СО2 СО ΔH = H(CO2) – H(C)
- 49. Следствия из закона Гесса: 1. Расчет теплового эффекта реакции по теплотам образования индивидуальных веществ. ΔfH –
- 50. Стандартные теплоты образования простых веществ в их наиболее устойчивых формах равны нулю.
- 51. Для условной химической реакции: аА + bB → сС + dD ΔrH = c ΔfH(C) +
- 52. 2. Расчет теплового эффекта химической реакции по теплотам сгорания индиви-дуальных веществ. ΔсгН – теплота сгорания –
- 53. Для условной реакции: ΔrH = а ΔcгH(A) + + b ΔcгH(B) – c ΔcгH(C) – -
- 54. Термохимия является основой диетологии, науки о рацио-нальном питании. Приведенные теплоты сгорания (кДж/г или ккал/г) пищевых продуктов
- 55. Калорийность важнейших компонентов пищи Жиры ~ 9 ккал/г Белки ~ 4 ккал/г Углеводы ~ 4 ккал/г
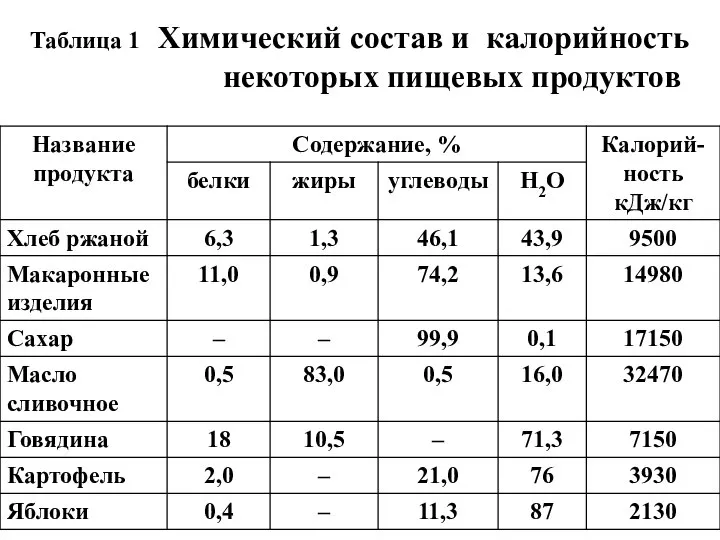
- 56. Таблица 1 Химический состав и калорийность некоторых пищевых продуктов
- 57. Суточная потребность человека в энергии зависит от мышечной нагрузки и составляет: при легкой мышечной работе –
- 58. Энергозатраты организма возрастают при различных заболеваниях. Например, при ревмотоидном артрите энергетическая прибавка на болезнь составляет ~10
- 59. Мозг человека, как во время сна, так и в период напряженной творческой деятельности, стабильно окисляет 5-6г
- 60. Увеличение калорийности пищи при одновременном снижении мышечной активности являются главными причинами ожирения. Ожирение – неинфекционная эпидемия
- 61. По данным ВОЗ в мире зарегистрировано 300 млн. больных ожирением. В развитых странах число страдающих от
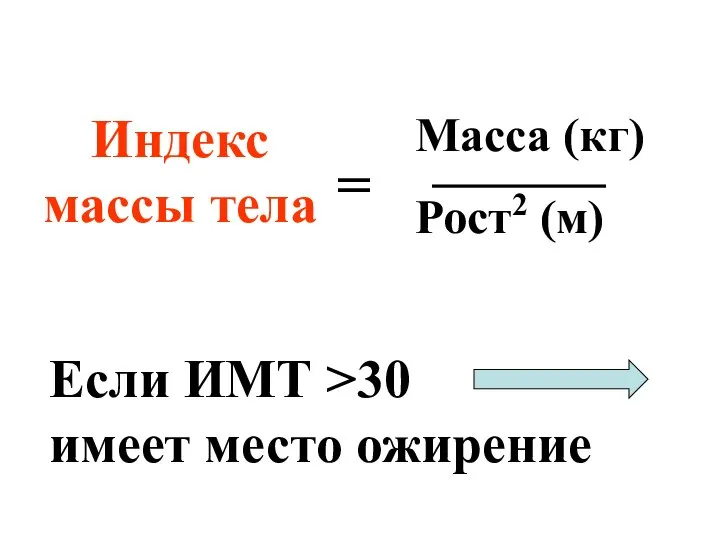
- 64. Индекс массы тела Масса (кг) Рост2 (м) = Если ИМТ >30 имеет место ожирение
- 65. Ожирение повышает риск сердечно-сосудистых заболеваний, диабета и рака.
- 67. Скачать презентацию



























































 Общие электронные конфигурации элементов главных подгрупп
Общие электронные конфигурации элементов главных подгрупп Аминокислоты. Свойства
Аминокислоты. Свойства Классификация металлов в соответствии с ионным потенциалом и параметром мягкости
Классификация металлов в соответствии с ионным потенциалом и параметром мягкости Сульфаниламидные препараты. (Тема 5)
Сульфаниламидные препараты. (Тема 5) Химия. 8 класс. Подготовка к контрольной работе
Химия. 8 класс. Подготовка к контрольной работе Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень
Атомный уровень. Химия простых веществ. Молекулярный уровень. Химия соединений. Живое субклеточный уровень Присадки к маслам
Присадки к маслам Периодический закон и периодическая система Д.И.Менделеева. Лекция 4
Периодический закон и периодическая система Д.И.Менделеева. Лекция 4 Презентация по Химии "Фосфор" - скачать смотреть бесплатно_
Презентация по Химии "Фосфор" - скачать смотреть бесплатно_ Химия в быту
Химия в быту Химия муравьиной кислоты
Химия муравьиной кислоты Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Генетическая связь основных классов неорганических соединений
Генетическая связь основных классов неорганических соединений Подача питательной воды в парогенератор при запроектной аварии
Подача питательной воды в парогенератор при запроектной аварии Именные реакции в органической химии
Именные реакции в органической химии Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно
Презентация по Химии "Оксиды получение, свойства, применение" - скачать смотреть бесплатно Презентация по Химии "Металлическая связь" - скачать смотреть
Презентация по Химии "Металлическая связь" - скачать смотреть  Углеводы. Дисахариды и полисахариды
Углеводы. Дисахариды и полисахариды Окислительно-восстановительные реакции . Алканолы
Окислительно-восстановительные реакции . Алканолы Тяжёлая вода
Тяжёлая вода Нитраты и нитриты. Азотные удобрения
Нитраты и нитриты. Азотные удобрения ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»
ПРЕЗЕНТАЦИЯ «Химия и повседневная жизнь человека»  Применение неметаллов
Применение неметаллов Бензойная кислота
Бензойная кислота Окислительно- восстановительные процессы
Окислительно- восстановительные процессы Выполнила: Смирнова Маргарита Ученица: 9-а класса
Выполнила: Смирнова Маргарита Ученица: 9-а класса Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..
Тест 1.Тип кристаллической решетки у белого фосфора…. а) молекулярный б) атомный в) ионный а) молекулярный Р4 2. У фосфора…..  Лекция 1. Топливо. Горение топлива
Лекция 1. Топливо. Горение топлива