Содержание
- 2. МККОС. Л.К. № 9. Попова Людмила Федоровна ЛИТЕРАТУРА
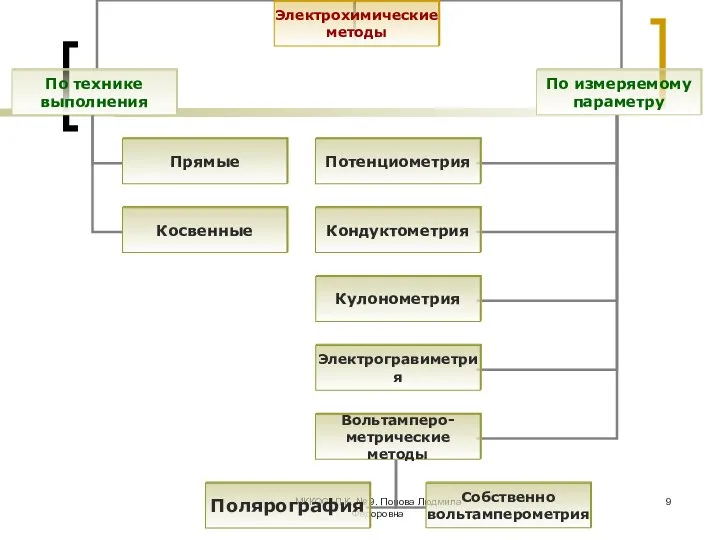
- 3. МККОС. Л.К. № 9. Попова Людмила Федоровна Теоретические основы электрохимических методов Электрохимические методы основаны на изучении
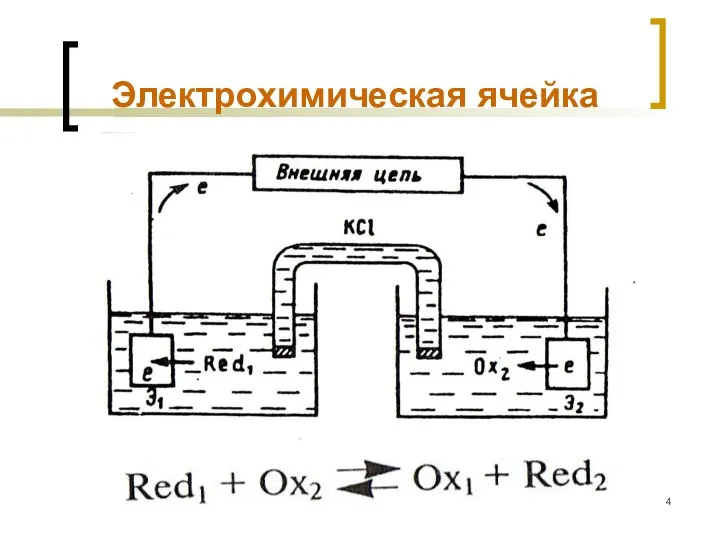
- 4. МККОС. Л.К. № 9. Попова Людмила Федоровна Электрохимическая ячейка
- 5. МККОС. Л.К. № 9. Попова Людмила Федоровна Электроды, используемые в электрохимии Электроды первого рода (обратимые относительно
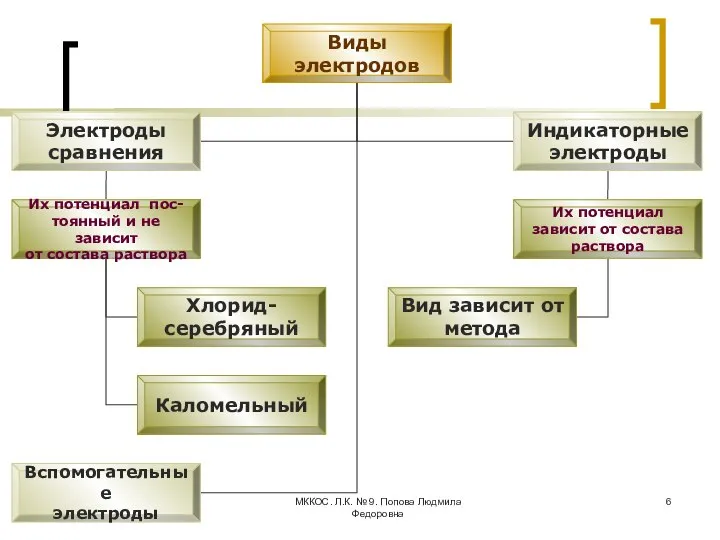
- 6. МККОС. Л.К. № 9. Попова Людмила Федоровна
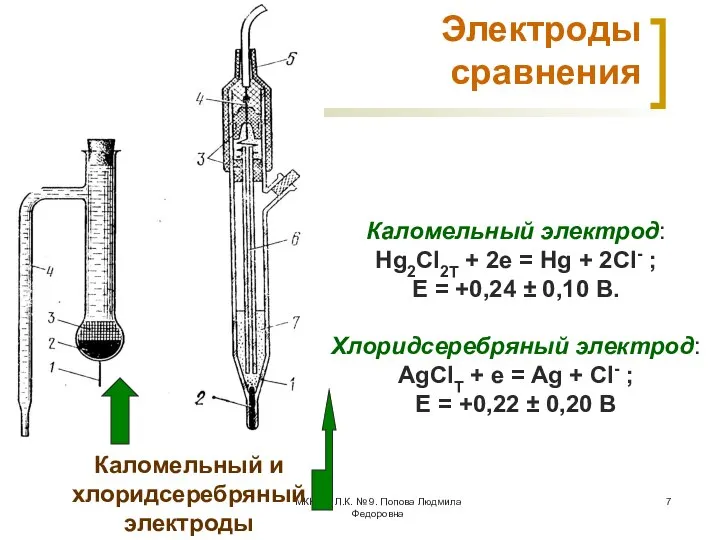
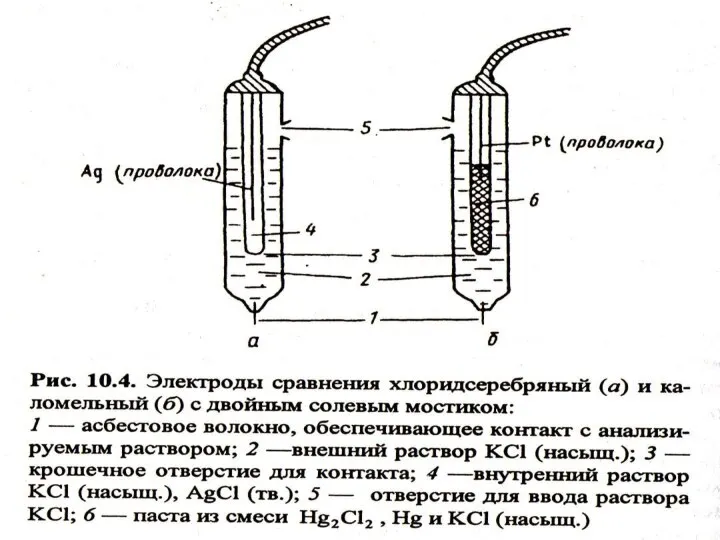
- 7. МККОС. Л.К. № 9. Попова Людмила Федоровна Электроды сравнения Каломельный и хлоридсеребряный электроды Каломельный электрод: Hg2Cl2Т
- 8. МККОС. Л.К. № 9. Попова Людмила Федоровна
- 9. МККОС. Л.К. № 9. Попова Людмила Федоровна
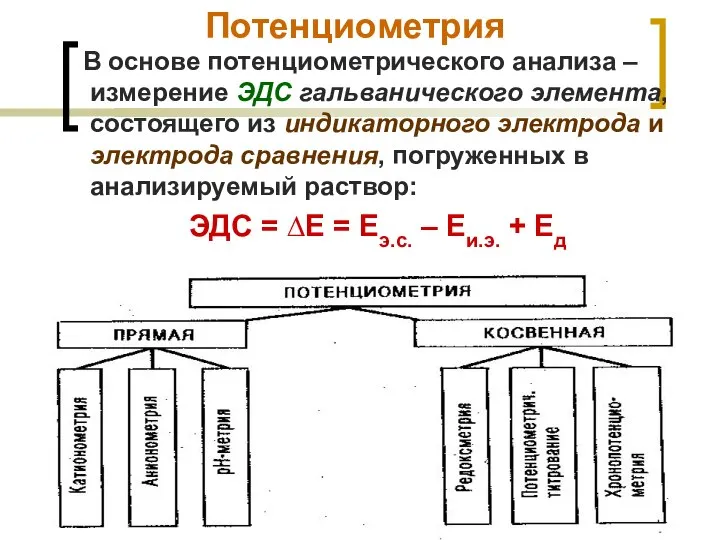
- 10. МККОС. Л.К. № 9. Попова Людмила Федоровна Потенциометрия В основе потенциометрического анализа – измерение ЭДС гальванического
- 11. МККОС. Л.К. № 9. Попова Людмила Федоровна В основе потенциометрических измерений лежит зависимость равновесного потенциала индикаторного
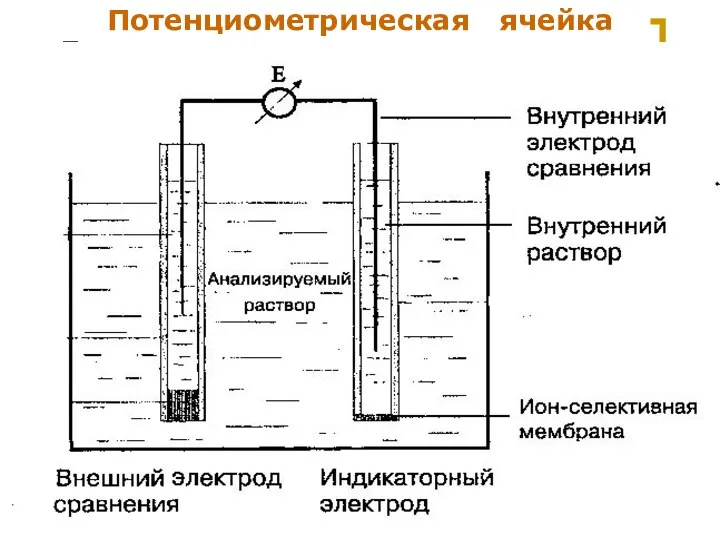
- 12. МККОС. Л.К. № 9. Попова Людмила Федоровна Потенциометрическая ячейка
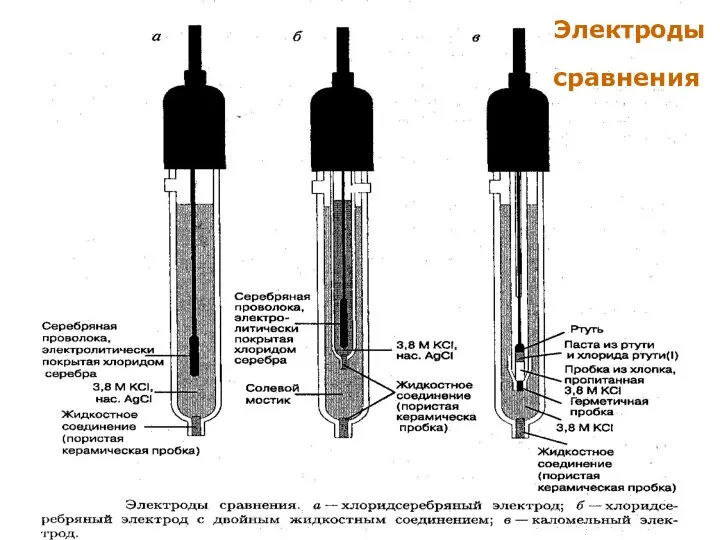
- 13. МККОС. Л.К. № 9. Попова Людмила Федоровна Электроды сравнения
- 14. МККОС. Л.К. № 9. Попова Людмила Федоровна Индикаторные электроды Металлические: Активные (первого рода); Инертные (третьего рода).
- 15. МККОС. Л.К. № 9. Попова Людмила Федоровна Металлические электроды Активные МЭ изготавливают из металлов (Ag, Pb,
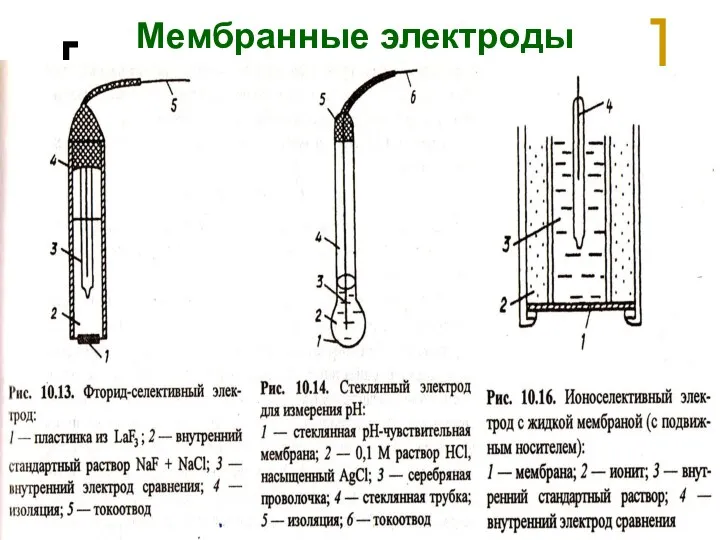
- 16. МККОС. Л.К. № 9. Попова Людмила Федоровна Мембранные электроды
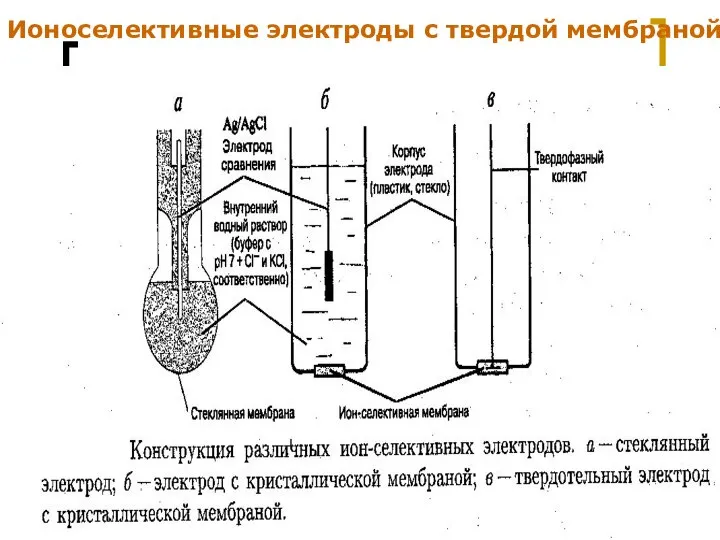
- 17. МККОС. Л.К. № 9. Попова Людмила Федоровна Ионоселективные электроды с твердой мембраной
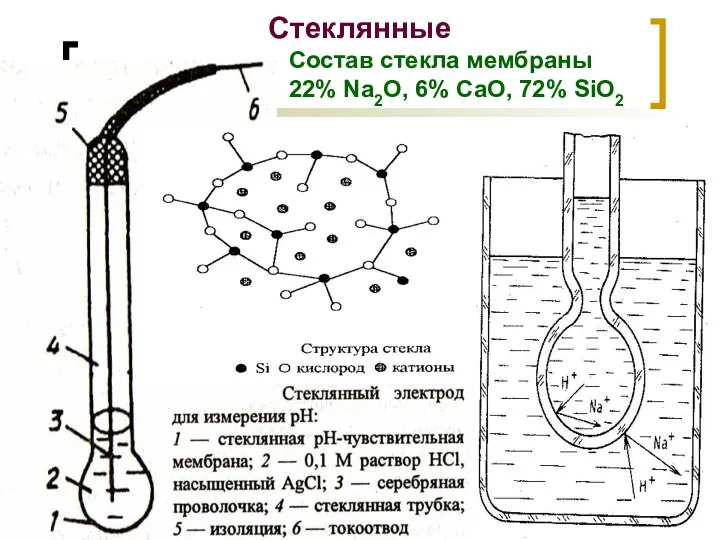
- 18. МККОС. Л.К. № 9. Попова Людмила Федоровна Стеклянные Состав стекла мембраны 22% Na2O, 6% CaO, 72%
- 19. МККОС. Л.К. № 9. Попова Людмила Федоровна Кристаллические Монокристаллические Таблетированные
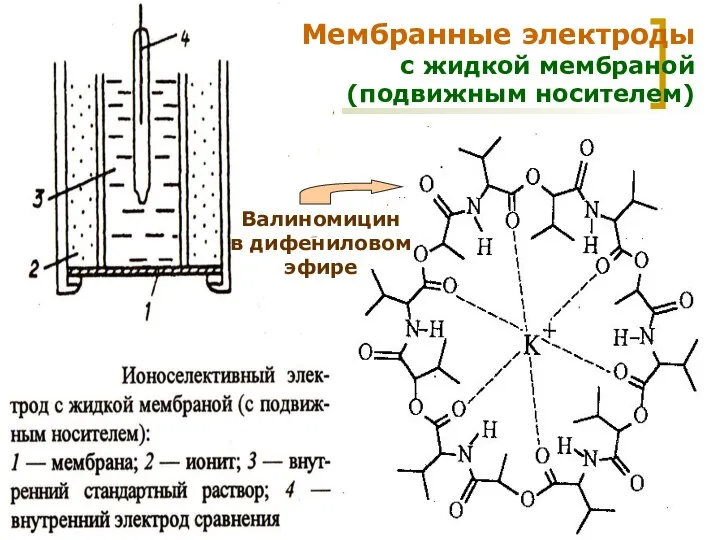
- 20. МККОС. Л.К. № 9. Попова Людмила Федоровна Мембранные электроды с жидкой мембраной (подвижным носителем) Валиномицин в
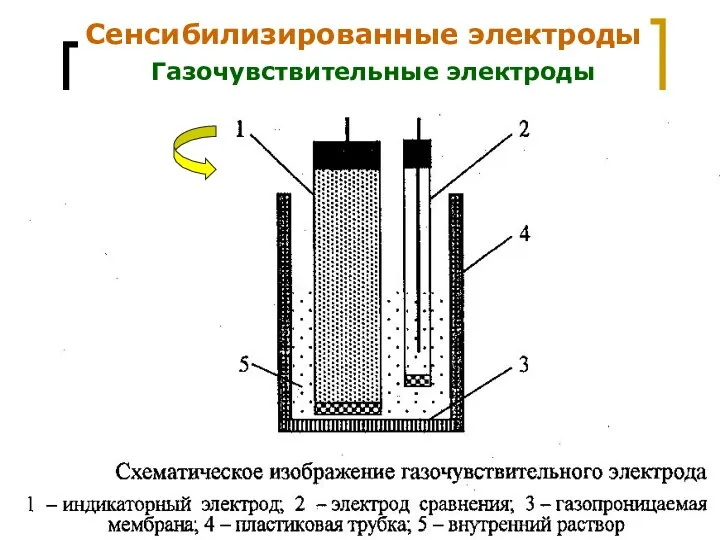
- 21. МККОС. Л.К. № 9. Попова Людмила Федоровна Сенсибилизированные электроды Газочувствительные электроды
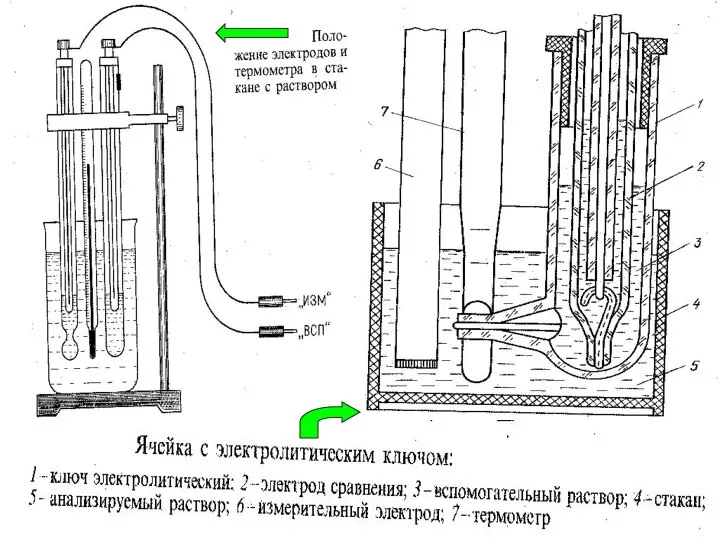
- 22. МККОС. Л.К. № 9. Попова Людмила Федоровна Оборудование для потенциометрии
- 23. МККОС. Л.К. № 9. Попова Людмила Федоровна
- 24. МККОС. Л.К. № 9. Попова Людмила Федоровна Прямая потенциометрия В основе метода – зависимость равновесного потенциала
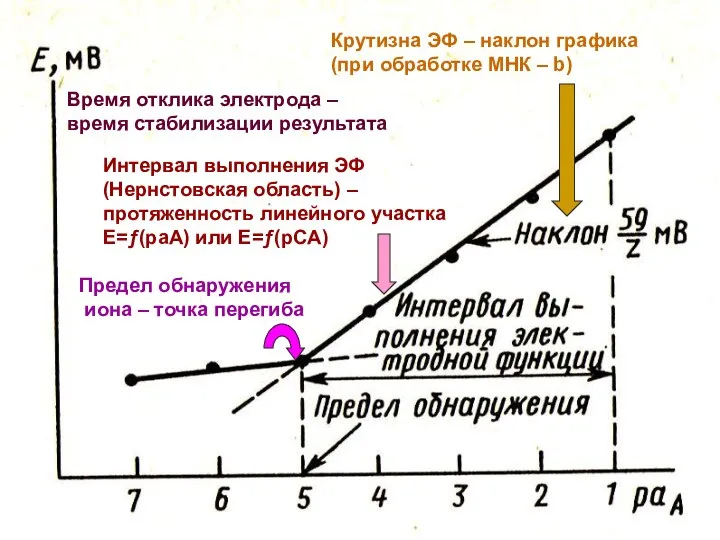
- 25. МККОС. Л.К. № 9. Попова Людмила Федоровна Ионометрия Построить калибровочный график и по нему определить основные
- 26. МККОС. Л.К. № 9. Попова Людмила Федоровна Крутизна ЭФ – наклон графика (при обработке МНК –
- 27. МККОС. Л.К. № 9. Попова Людмила Федоровна Способы определения концентрации Способ калибровочного графика
- 28. МККОС. Л.К. № 9. Попова Людмила Федоровна Способ добавок с учетом разбавления ; без учета разбавления
- 29. МККОС. Л.К. № 9. Попова Людмила Федоровна Потенциометрическое титрование Сущность метода – измерение потенциала индикаторного электрода
- 30. МККОС. Л.К. № 9. Попова Людмила Федоровна
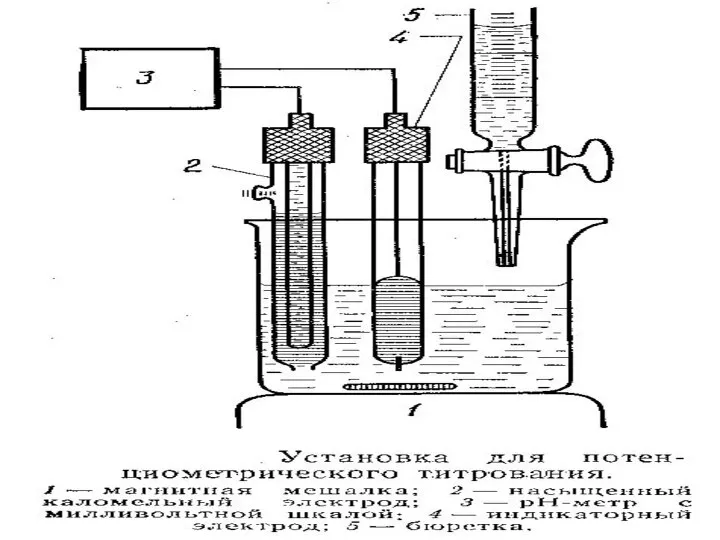
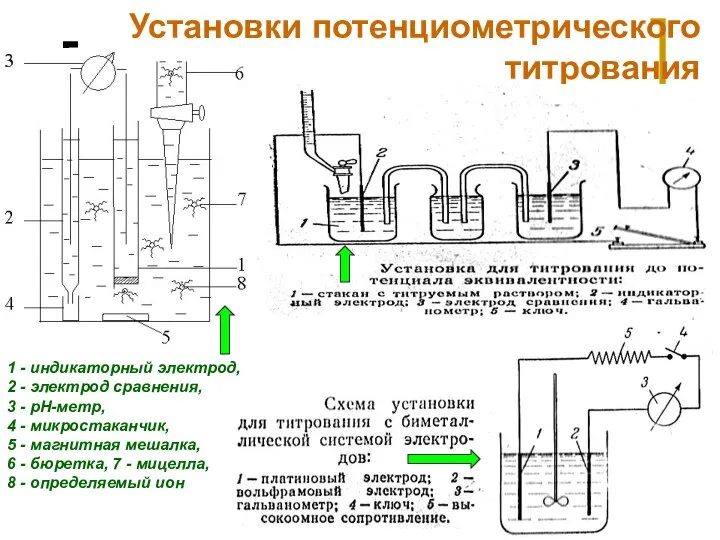
- 31. МККОС. Л.К. № 9. Попова Людмила Федоровна Установки потенциометрического титрования 1 - индикаторный электрод, 2 -
- 32. МККОС. Л.К. № 9. Попова Людмила Федоровна Автотитраторы (современные установки)
- 33. МККОС. Л.К. № 9. Попова Людмила Федоровна
- 34. МККОС. Л.К. № 9. Попова Людмила Федоровна Способы определения КТТ Расчетный способ N – число капель;
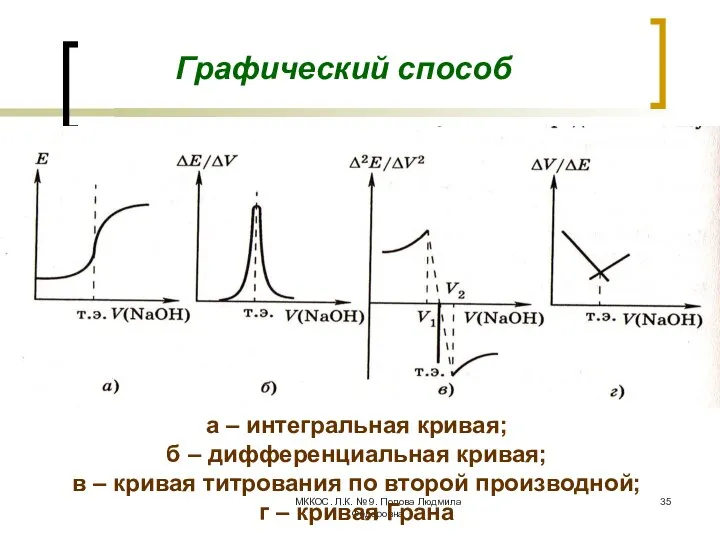
- 35. МККОС. Л.К. № 9. Попова Людмила Федоровна Графический способ а – интегральная кривая; б – дифференциальная
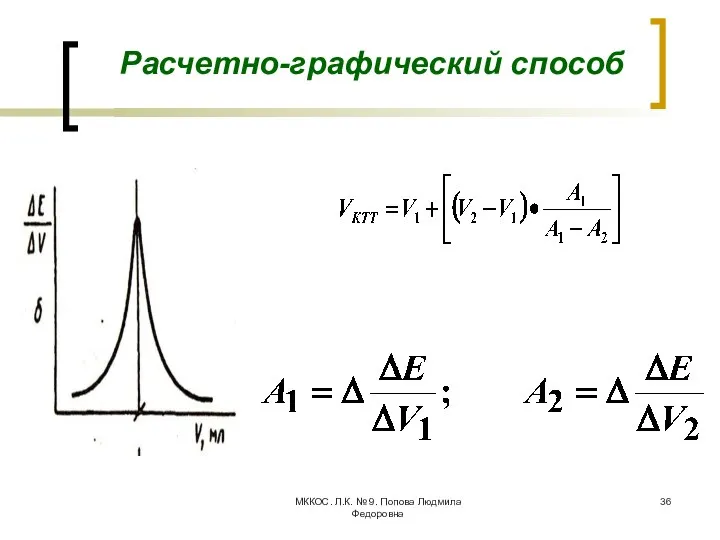
- 36. МККОС. Л.К. № 9. Попова Людмила Федоровна Расчетно-графический способ
- 37. МККОС. Л.К. № 9. Попова Людмила Федоровна Виды потенциометрического титрования Кислотно-основное (рН-селективный электрод). Комплексонометрическое (Ме-селективные электроды
- 38. МККОС. Л.К. № 9. Попова Людмила Федоровна Кондуктометрия Основана на измерении удельной электропроводности анализируемого раствора. Электрическая
- 39. МККОС. Л.К. № 9. Попова Людмила Федоровна Теоретические основы метода Электрическая проводимость – W – величина
- 40. МККОС. Л.К. № 9. Попова Людмила Федоровна Удельная электропроводность æ (См/см или Ом-1•см-1) равна электрической проводимости
- 41. МККОС. Л.К. № 9. Попова Людмила Федоровна
- 42. МККОС. Л.К. № 9. Попова Людмила Федоровна Эквивалентная ионная электропроводность (подвижность) λ (См•см2/моль-экв) – это проводимость
- 43. МККОС. Л.К. № 9. Попова Людмила Федоровна В соответствии с законом независимого движения ионов Кольрауша эквивалентная
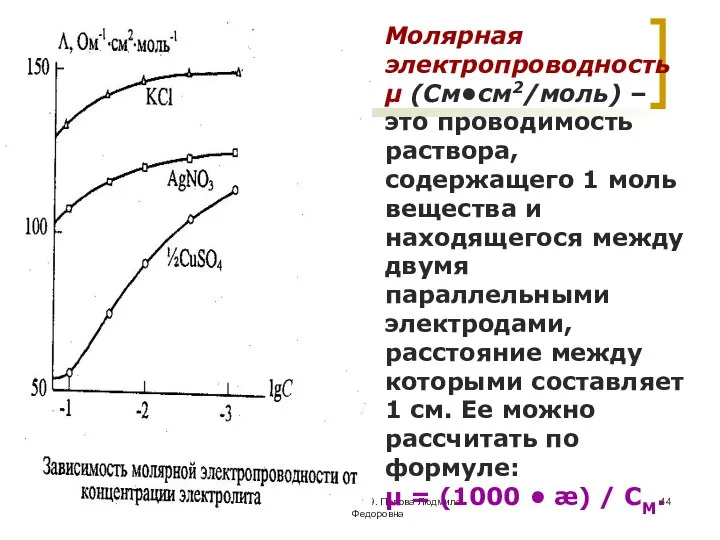
- 44. МККОС. Л.К. № 9. Попова Людмила Федоровна Молярная электропроводность μ (См•см2/моль) – это проводимость раствора, содержащего
- 45. МККОС. Л.К. № 9. Попова Людмила Федоровна
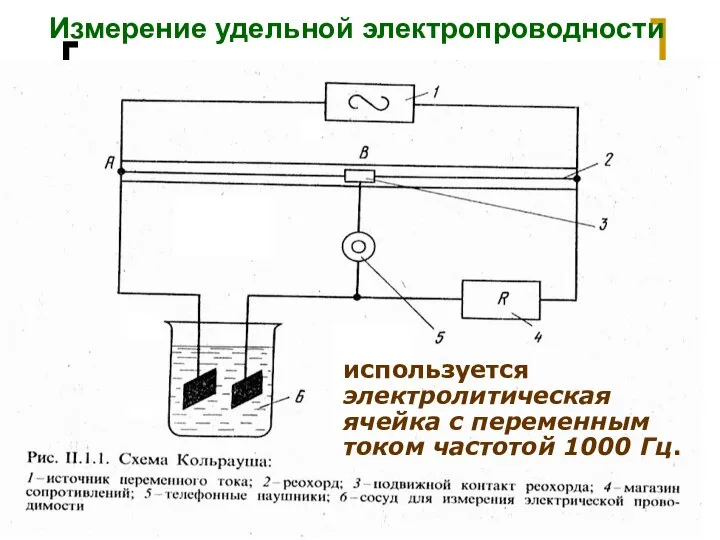
- 46. МККОС. Л.К. № 9. Попова Людмила Федоровна Измерение удельной электропроводности используется электролитическая ячейка с переменным током
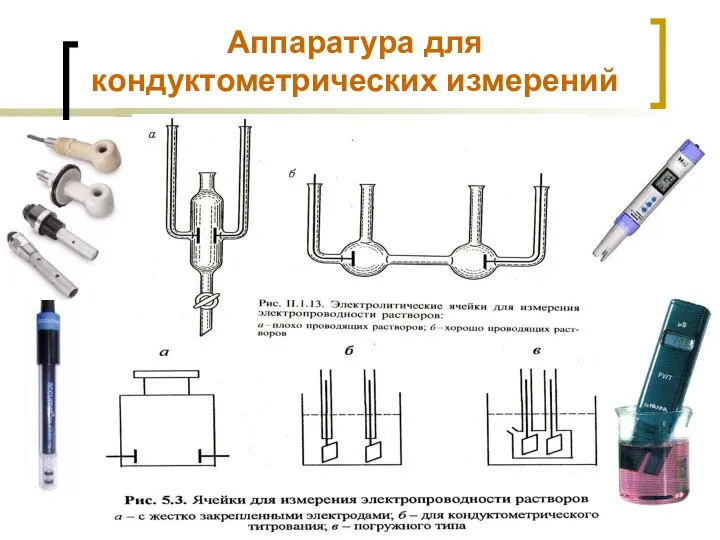
- 47. МККОС. Л.К. № 9. Попова Людмила Федоровна Аппаратура для кондуктометрических измерений
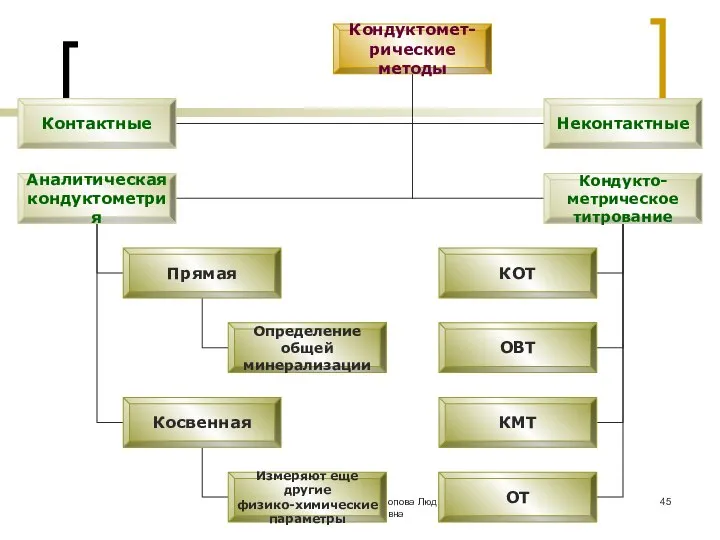
- 48. МККОС. Л.К. № 9. Попова Людмила Федоровна Аналитическая кондуктометрия
- 49. МККОС. Л.К. № 9. Попова Людмила Федоровна Кондуктометрически можно определять: физико-химические свойства и характеристики веществ, например:
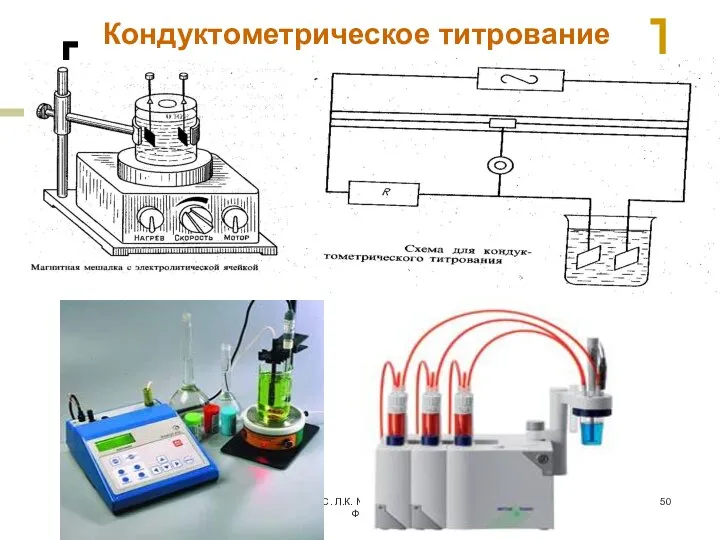
- 50. МККОС. Л.К. № 9. Попова Людмила Федоровна Кондуктометрическое титрование
- 52. Скачать презентацию

























 Chemistry
Chemistry Получение кормовой добавки на основе выжимок томатов и рисовой мучки
Получение кормовой добавки на основе выжимок томатов и рисовой мучки Липиды. Общая характеристика липидов
Липиды. Общая характеристика липидов Органическая химия- химия соединений углерода
Органическая химия- химия соединений углерода Презентация по Химии "Гетероциклические соединения" - скачать смотреть
Презентация по Химии "Гетероциклические соединения" - скачать смотреть  Воздух. Постоянные компоненты воздуха
Воздух. Постоянные компоненты воздуха Безопасное использование атразина, как гербицида в сельском хозяйстве
Безопасное использование атразина, как гербицида в сельском хозяйстве Решение расчётных задач
Решение расчётных задач Виды присадок к моторным топливам. Присадки к дизельному топливу
Виды присадок к моторным топливам. Присадки к дизельному топливу Композитные материалы
Композитные материалы Элементы теории горения
Элементы теории горения Презентация к открытому уроку Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.
Презентация к открытому уроку Учитель химии МОУ «Гимназия №1» г. Саратов Шишкина И.Ю.  Оксид азота(2) NO
Оксид азота(2) NO Введение в минералогию. Лекция 1
Введение в минералогию. Лекция 1 Основания, кислоты, соли Комбинированный урок химии в 8 классе
Основания, кислоты, соли Комбинированный урок химии в 8 классе Тяжелые металлы. Опасность токсичных металлов для организма
Тяжелые металлы. Опасность токсичных металлов для организма Көміртек жене оның қосылыстары
Көміртек жене оның қосылыстары Алканы. Пропан - С3Н8
Алканы. Пропан - С3Н8 Положение металлов в ПСХЭ Д.И. Менделеева. Общие физические свойства металлов
Положение металлов в ПСХЭ Д.И. Менделеева. Общие физические свойства металлов Кислоты
Кислоты Типы химических реакций в органической химии. Типы реакций в органике
Типы химических реакций в органической химии. Типы реакций в органике Презентация по Химии "Химические свойства металлов. Электрохимический ряд напряжения металлов. 11-й класс" - скачать смотреть
Презентация по Химии "Химические свойства металлов. Электрохимический ряд напряжения металлов. 11-й класс" - скачать смотреть  Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2)
Основи процесів горіння. Полум’я. Процеси, що відбуваються у полум’ї. (Розділ 1.1.2) Пластмаси.Синтетичні каучуки.Гума виконала учениця 11-Ф класу Бабич Роксолана
Пластмаси.Синтетичні каучуки.Гума виконала учениця 11-Ф класу Бабич Роксолана  G11. Химический состав
G11. Химический состав Презентация по Химии "ПОЛУЧЕНИЕ И СВОЙСТВА СТАБИЛЬНЫХ ИЗОТОПОВ КРЕМНИЯ ВЫСОКОЙ ХИМИЧЕСКОЙ И ИЗОТОПНОЙ ЧИСТОТЫ" - скачать смо
Презентация по Химии "ПОЛУЧЕНИЕ И СВОЙСТВА СТАБИЛЬНЫХ ИЗОТОПОВ КРЕМНИЯ ВЫСОКОЙ ХИМИЧЕСКОЙ И ИЗОТОПНОЙ ЧИСТОТЫ" - скачать смо МЕТАЛЛЫ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д.И. МЕНДЕЛЕЕВА Петреня Игорь Михайлович, учитель химии и биологии госуд
МЕТАЛЛЫ В ПЕРИОДИЧЕСКОЙ СИСТЕМЕ ХИМИЧЕСКИХ ЭЛЕМЕНТОВ Д.И. МЕНДЕЛЕЕВА Петреня Игорь Михайлович, учитель химии и биологии госуд Биополимеры. Классификация полисахаридов (гликаны)
Биополимеры. Классификация полисахаридов (гликаны)