Содержание
- 2. Классификация полисахаридов (гликаны). (по составу) гомополисахариды гетерополисахариды (состоят из одинаковых моноструктурных единиц) (крахмал, гликоген, целлюлоза, хитин)
- 3. Образуется в результате фотосинтеза в растениях и накапливается в клубнях, семенах, корнях Крахмал: Мм – 106
- 4. В горячей воде набухает и подвергается гидролизу, в результате образуются более мелкие полисахариды, конечным продуктом является
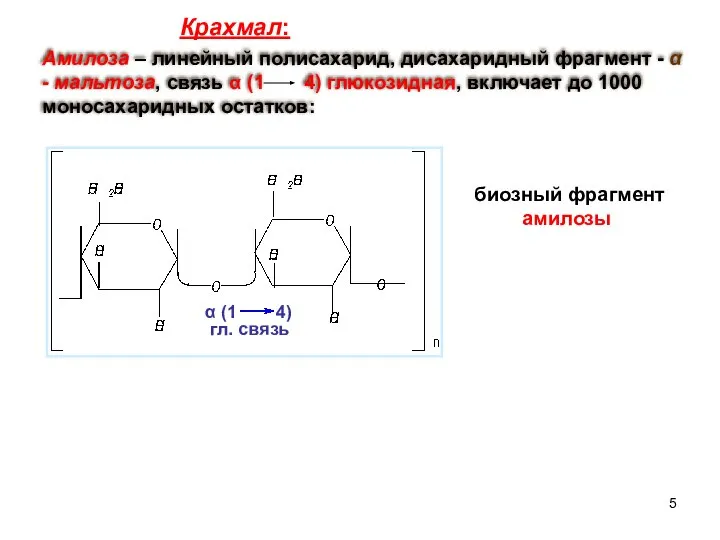
- 5. Амилоза – линейный полисахарид, дисахаридный фрагмент - α - мальтоза, связь α (1 4) глюкозидная, включает
- 6. Неразветвленная макромолекула свернута в спираль, на каждый виток приходится 6 моносахаридных звеньев. Внутри спирали могут проходить
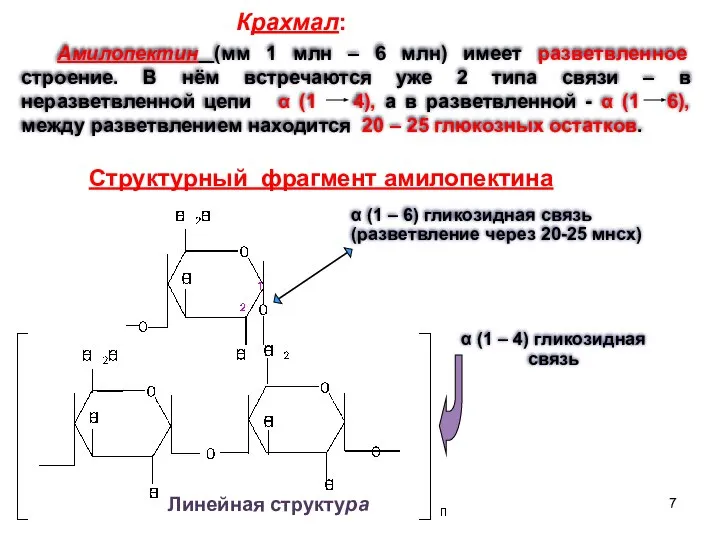
- 7. Амилопектин (мм 1 млн – 6 млн) имеет разветвленное строение. В нём встречаются уже 2 типа
- 8. Гликоген – животный крахмал, это структурный и функциональный аналог растительного крахмала, вернее, ее разветвленной фракции –
- 9. Сильное разветвление обеспечивает гликогену выполнение энергетической функции, позволяя в стрессовых ситуациях быстро отщеплять нужное количество глюкозы
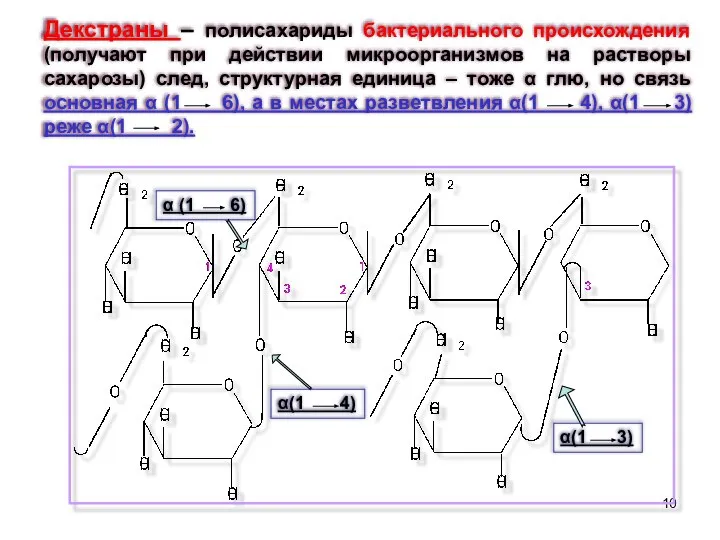
- 10. Декстраны – полисахариды бактериального происхождения (получают при действии микроорганизмов на растворы сахарозы) след, структурная единица –
- 11. Декстраны используются как заменители крови. Но так как большая Мм мешает их растворимости, с помощью кислотного
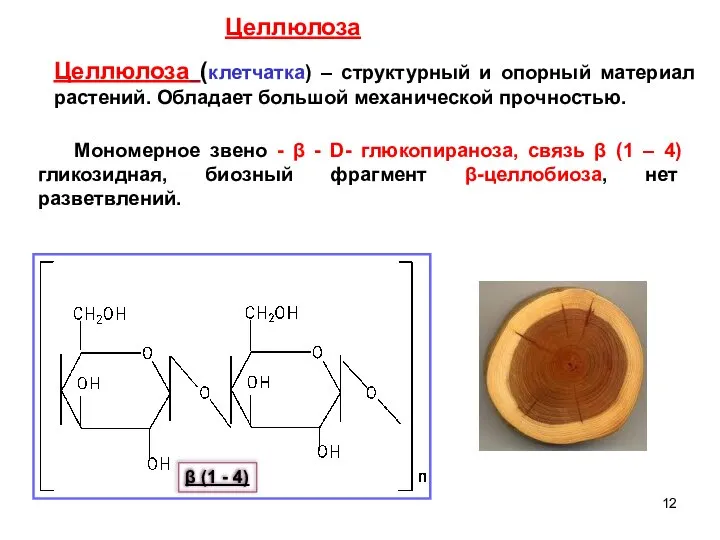
- 12. Целлюлоза (клетчатка) – структурный и опорный материал растений. Обладает большой механической прочностью. Мономерное звено - β
- 13. В макромолекуле содержится (2500 – 12 тыс. ) глюкозных звеньев. Мм достигает 1 – 2 млн.
- 14. Целлюлоза не расщепляется ферментом, желудочно-кишечного тракта (нет β глюкозидазы), но есть необходимые вещества, активизирующие перистальтику желудка
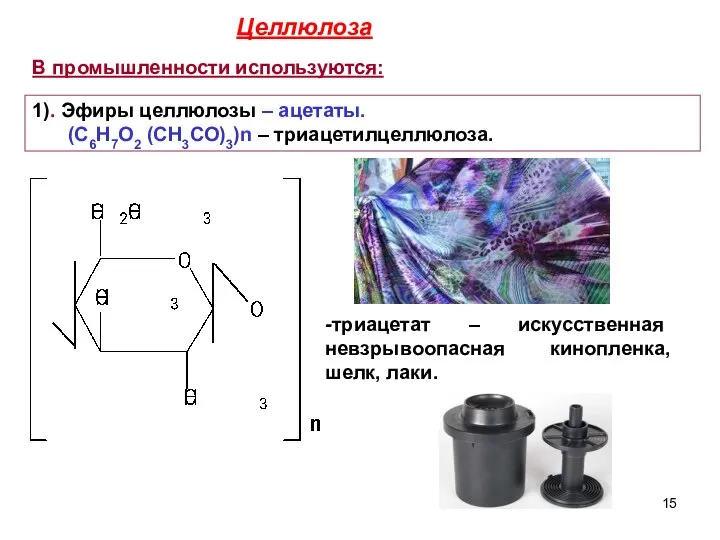
- 15. В промышленности используются: 1). Эфиры целлюлозы – ацетаты. (С6Н7О2 (СН3СО)3)n – триацетилцеллюлоза. -триацетат – искусственная невзрывоопасная
- 16. 3). Нитрат целлюлозы (ди – и три -) тринитрат –пироксилен, взрывчатое вещество, бездымный порох 2). Этиловый
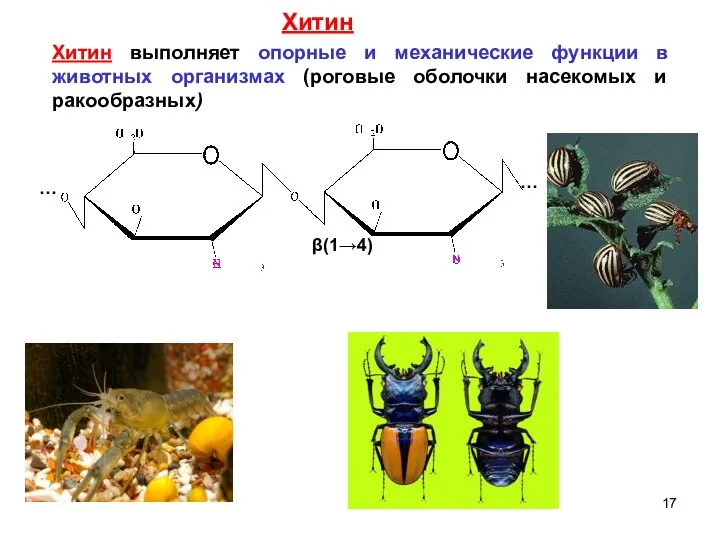
- 17. Хитин выполняет опорные и механические функции в животных организмах (роговые оболочки насекомых и ракообразных) … …
- 18. Гетерополисахариды Гетерополисахариды – состоят из остатков разных моносахаридов. Изучены меньше, чем гомополисахариды. Очень важны гетерополисахариды соединительной
- 19. В строении этих гетерополисахаридов есть общее: в их неразветвленные цепи входят дисахаридные фрагменты из уроновых кислот
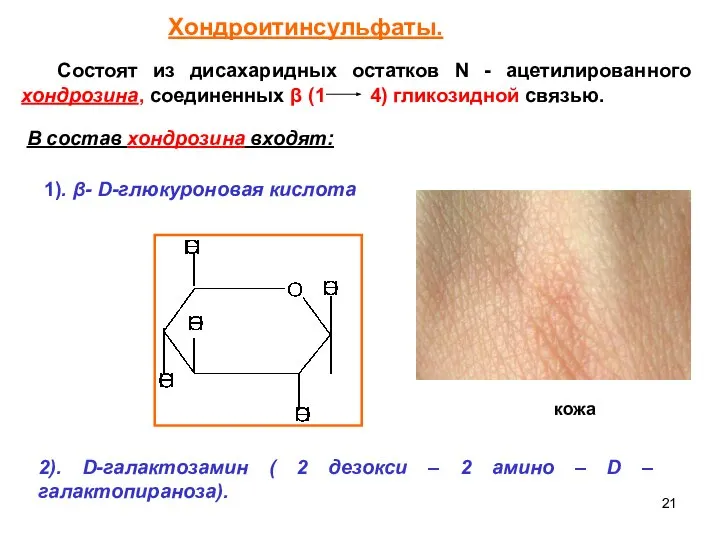
- 20. Хондроитинсульфаты. (кожа, хрящи, сухожилия).(Мм – 10 тыс. до 60 тыс.)
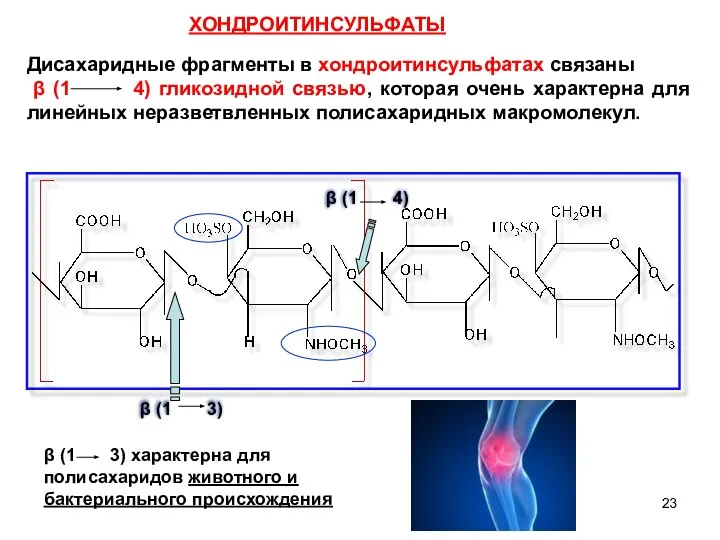
- 21. Состоят из дисахаридных остатков N - ацетилированного хондрозина, соединенных β (1 4) гликозидной связью. В состав
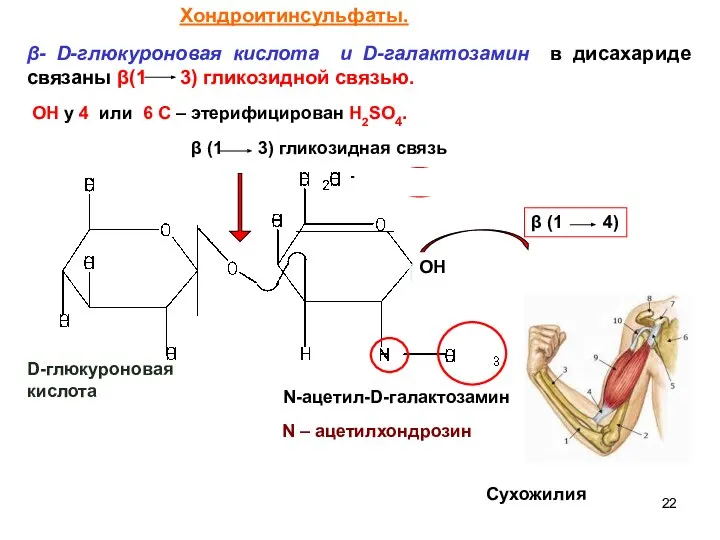
- 22. β- D-глюкуроновая кислота и D-галактозамин в дисахариде связаны β(1 3) гликозидной связью. β (1 3) гликозидная
- 23. ХОНДРОИТИНСУЛЬФАТЫ Дисахаридные фрагменты в хондроитинсульфатах связаны β (1 4) гликозидной связью, которая очень характерна для линейных
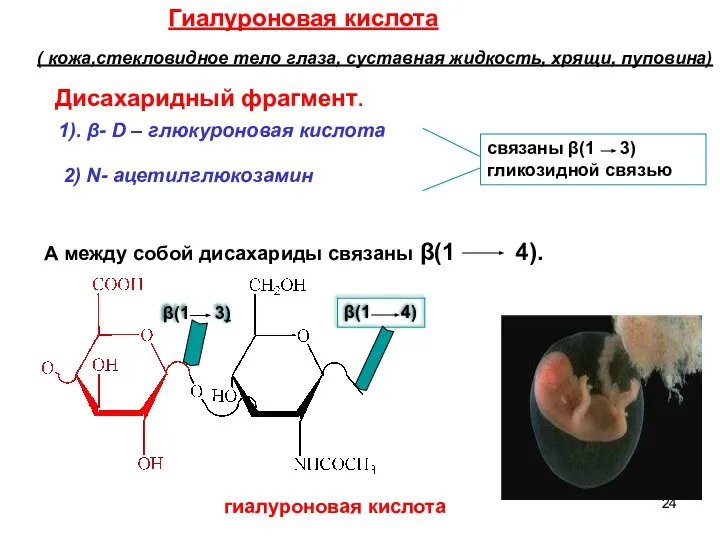
- 24. Гиалуроновая кислота ( кожа,стекловидное тело глаза, суставная жидкость, хрящи, пуповина) Дисахаридный фрагмент. 1). β- D –
- 25. Гиалуроновая кислота Одним из основных факторов старения кожи является снижение содержания гиалуроновой кислоты и тесно связанное
- 26. Обмен гиалуроновой кислоты в организме человека совершается быстро — период её полураспада в организме 2 дня.
- 27. Гидролиз гиалуроновой кислоты осуществляется гиалуронидазой, которая присутствует в оболочках болезнетворных бактерий, сперме, яде змей, пауков, пчёл,
- 28. Основу клеток и жидкостей животных организмов составляют смешанные биополимеры С преобладанием углеводной --пептидогликаны и протеогликаны, преобладанием
- 29. Хондроитинсульфаты в свободном состоянии не встречаются, они всегда связаны с белками. На конце цепи хондроитинсульфата имеется
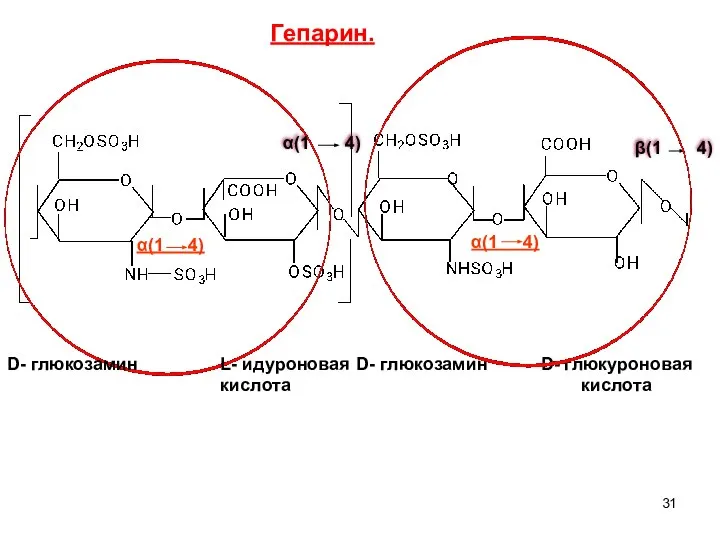
- 30. Дисахаридные остатки: D – глюкозамин и 2 уроновые кислоты – D - глюкуроновая и L -
- 31. α(1 4) β(1 4) α(1 4) α(1 4) D- глюкозамин L- идуроновая кислота D- глюкозамин D-
- 32. Биохимические свойства гепарина Синтезируется в организме животных и человека. Антикоагулянтные свойства: препятствует свертываемости крови. Регулятор многих
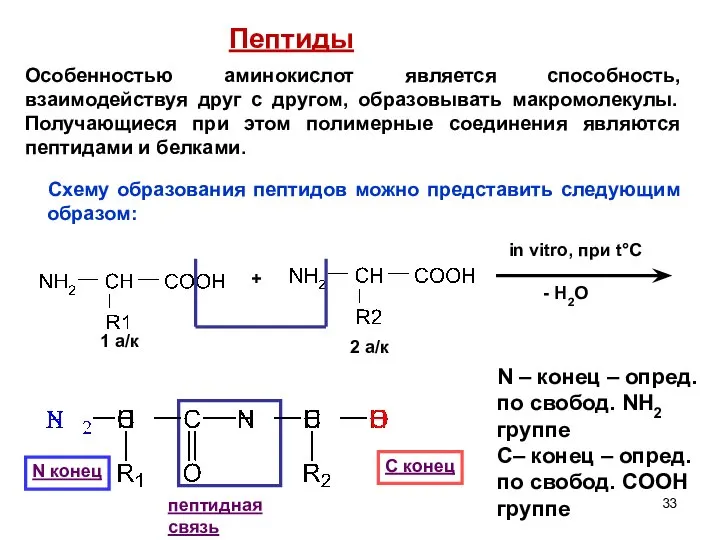
- 33. + in vitro, при t°C - H2O 1 а/к 2 а/к N конец С конец пептидная
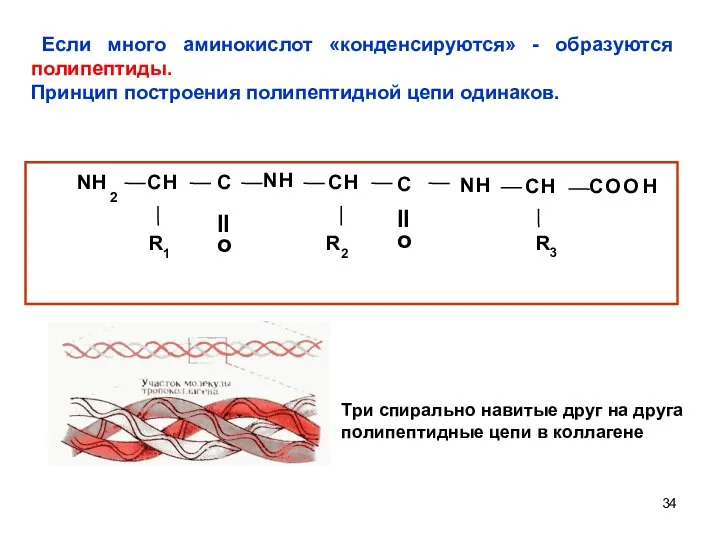
- 34. Если много аминокислот «конденсируются» - образуются полипептиды. Принцип построения полипептидной цепи одинаков. Три спирально навитые друг
- 35. Все операции проводятся в определённой запрограммированной последовательности Каскадный синтез пептидов. (ала-гли) Защита NH2 группы I ак
- 36. 1) Защита NH2 – группы I ак С ацилирующим реагентом , (RCO)2O, R – COOH, C6H5CH2OCOCl
- 37. 2) Защита СООН – группы II ак сухой гли Реакция этерификации
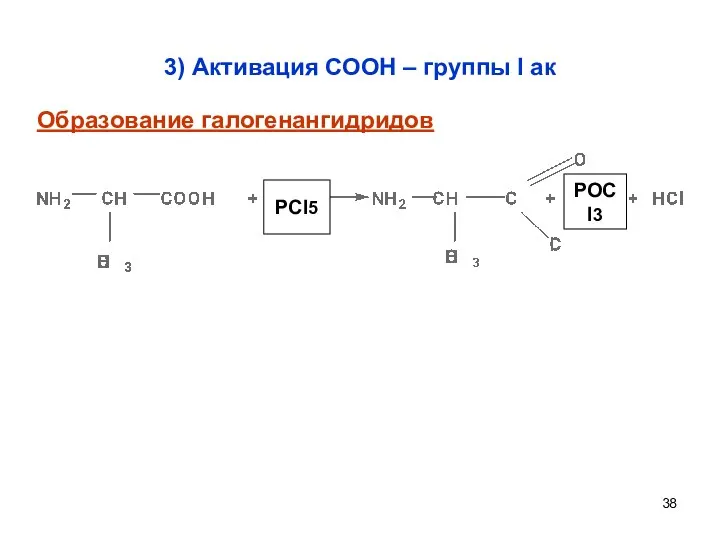
- 38. 3) Активация СООН – группы I ак PCl5 POCl3 Образование галогенангидридов
- 39. 4) Синтез 5) Снятие защиты --Сложный процесс
- 40. Название полипептидов : перечисляются аминокислоты с N-конца с использованием суффикса –ил, а последняя кислота имеет обычное
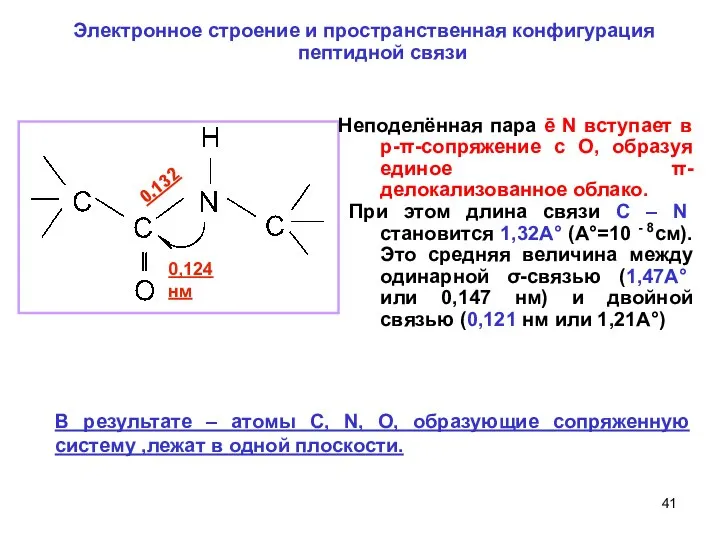
- 41. 0,132 0,124 нм Электронное строение и пространственная конфигурация пептидной связи Неподелённая пара ē N вступает в
- 42. Электронное строение и пространственная конфигурация пептидной связи Кратность связи C – O и C – N
- 43. Взаимное положение плоскостей пептидных групп в полипептидной цепи
- 44. лактамная форма лактимная форма Электронное строение и пространственная конфигурация пептидной связи О В результате p-π сопряжения
- 45. Фишер (Fischer) Эмиль (9.10.1852– 15.7.1919), немецкий химик-органик и биохимик. Иностранный член-корреспондент Петербургской АН (1899). Нобелевская премия
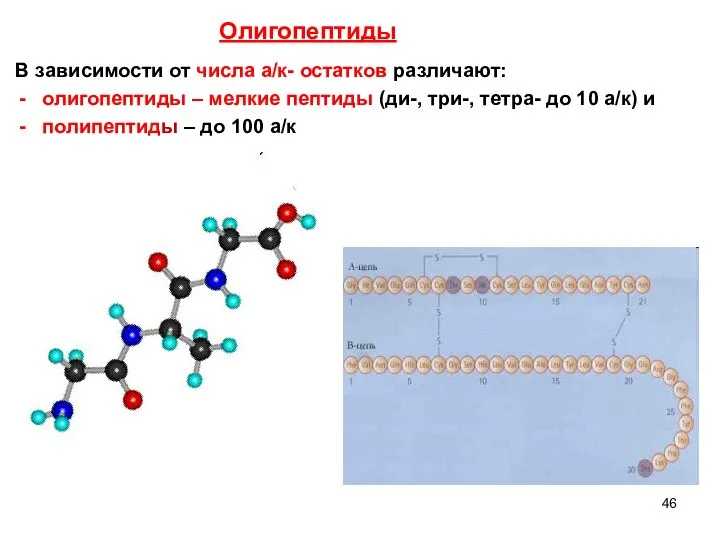
- 46. В зависимости от числа а/к- остатков различают: олигопептиды – мелкие пептиды (ди-, три-, тетра- до 10
- 47. Классификация пептидов по функциям в организме Ферментативная функция Пептиды - природные катализаторы
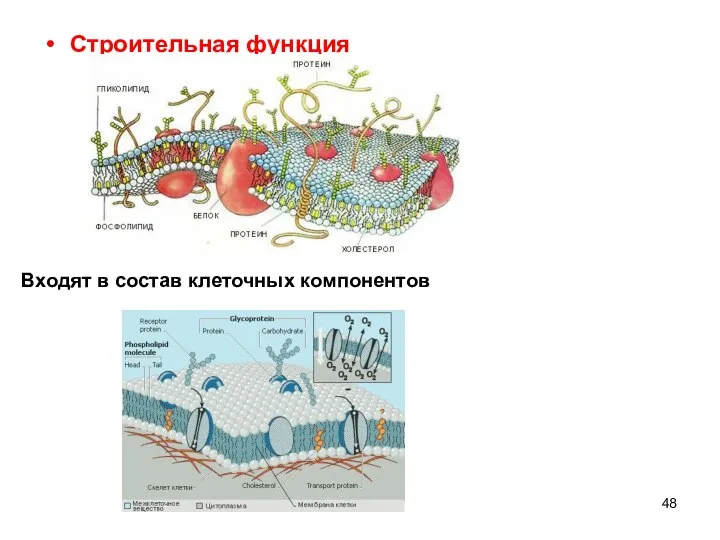
- 48. Строительная функция Входят в состав клеточных компонентов
- 49. Энергетическая функция 1 грамм пептида = 17,6 кДж энергии Двигательная функция 3 белковые системы: Флагелин Актин
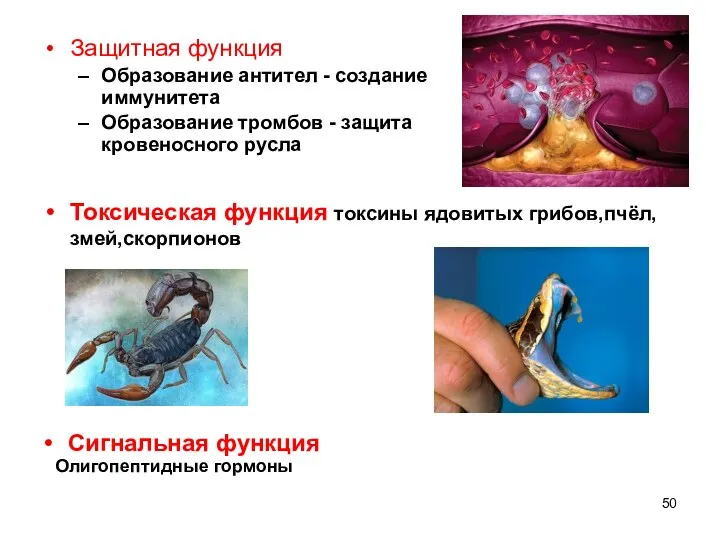
- 50. Защитная функция Образование антител - создание иммунитета Образование тромбов - защита кровеносного русла Токсическая функция токсины
- 51. Транспортная функция Антибиотическая функция Олигопептидные антибиотики синтезируются бактериями и низшими грибами Рецепторная фунция Взаимодействие с окружающей
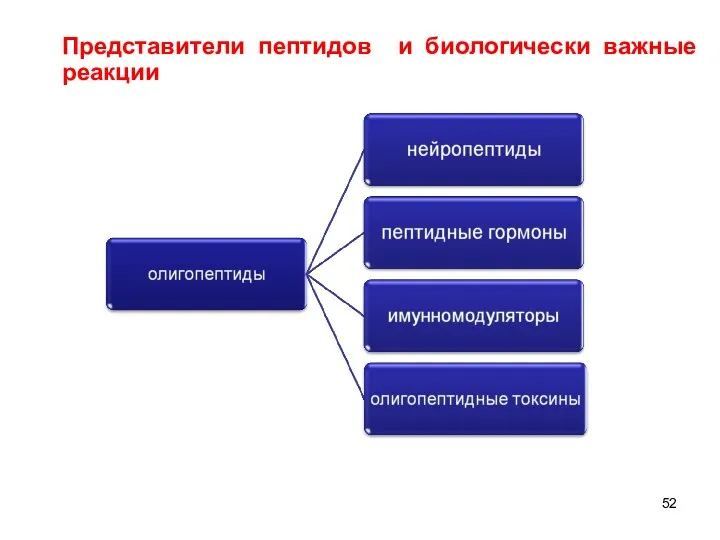
- 52. Представители пептидов и биологически важные реакции
- 53. Глутатион -γ-глутамилцистеинилглицин (трипептид)
- 54. Эритроциты в норме Клетки в отсутствии глутатиона Защищает гемоглобин и его белки, мембрану эритроцитов от окислителей.
- 55. Основной антиоксидант, вырабатываемый клетками организма. Глутатион -γ-глутамилцистеинилглицин
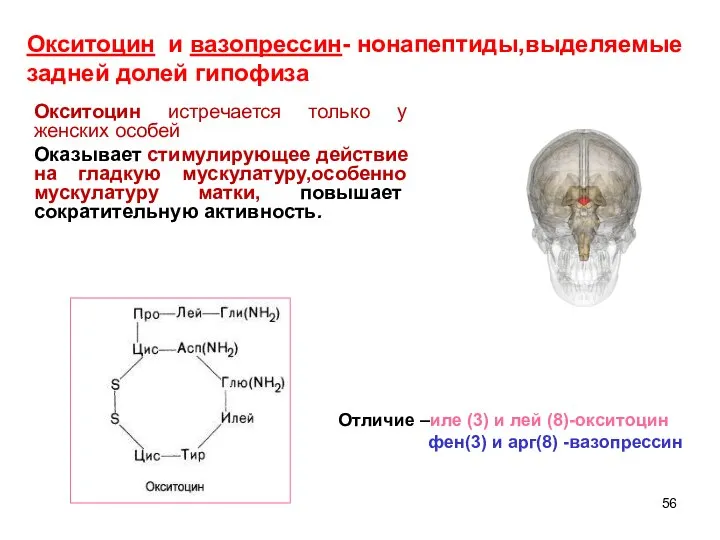
- 56. Окситоцин истречается только у женских особей Оказывает стимулирующее действие на гладкую мускулатуру,особенно мускулатуру матки, повышает сократительную
- 57. Гормон доверчивости. Участвует сразу же после родов в формировании отношения мать-ребенок. Окситоцин
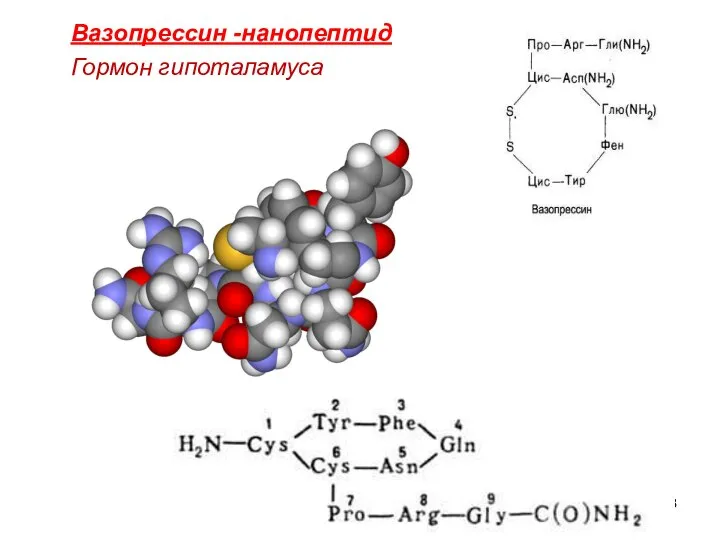
- 58. Вазопрессин -нанопептид Гормон гипоталамуса
- 59. Вазопрессин -нонапептид Вазопрессин содержится в женском и мужском организме Регулирует минеральный обмен и баланс жидкости
- 60. Таблетки верности Вазопрессин управляет родительским поведением, а также узнаванием "своих" и формированием привязанности, нежности и ласки.
- 61. Инсулин – гормон поджелудочной железы, с недостатком инсулина связано нарушение УВ обмена и сахарный диабет, как
- 62. Расшифровка первичной структуры пептидов – мощный стимул для развития работ по их синтезу. Впервые бычий инсулин
- 63. Нейропептиды - природные олигопептиды, образующиеся в центральной или периферической нервной системе и регулирующие физиологические функции организма
- 64. Пептиды служат важным «средством общения» между собой нервных клеток наряду с давно известными медиаторами – дофамином,
- 65. Нейропептиды: влияют на процессы обучения и запоминания регулируют сон обладают обезболивающей функцией ответственны за чувство голода,
- 66. Многие пептиды работают в системе удовольствия, моделируя поведение нервных импульсов по тем нервным путям, которые создают
- 67. К таким пептидам относятся опиоидные нейропептиды – энкефалины и эндорфины. Они образуются в мозге и оказывают
- 68. Опиоидные пептиды Опиоидные пептиды - группа природных и синтетических пептидов, сходных с опиатами (морфин, кодеин и
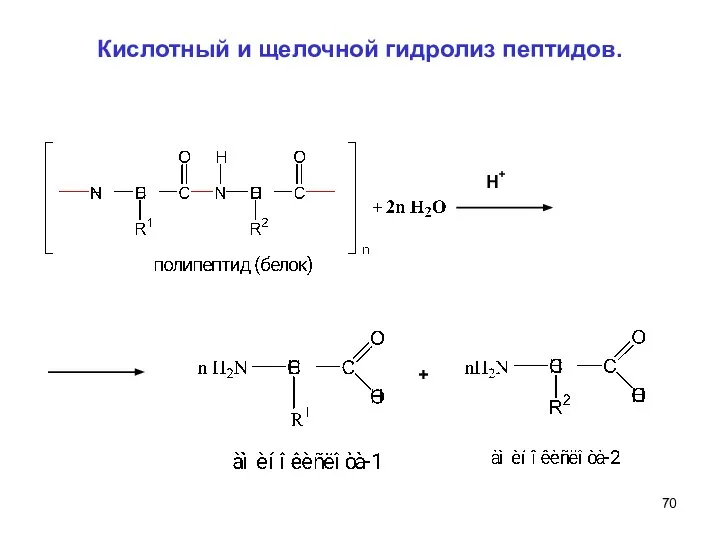
- 69. Кислотный и щелочной гидролиз пептидов. Важное свойство пептидов - способность к гидролизу. При гидролизе происходит полное
- 70. Кислотный и щелочной гидролиз пептидов. H + +
- 71. Структура белка Белковые молекулы – полимерные, неразветвлённые цепи из α-аминокислот (> 100 аминокислот), структурные единицы –
- 72. Порядок расположения ковалентно связанных аминокислот в полипептидной цепи называют аминокислотной последовательностью, или первичной структурой белков. Первичная
- 73. Вторичная структура фиксируется водородными связями между пептидными группами. II Вторичная структура - укладка первичной структуры белка,
- 74. Вторичная структура белка
- 75. Третичная структура – укладка вторичных структур одной полипептидной цепи в глобулу. В формировании третичной структуры, кроме
- 76. Третичная структура белка
- 77. IV Четвертичная структура – способ укладки в пространстве отдельных полипептидных цепей, и формирование единого макромолекулярного комплекса,
- 78. 1.Гликопротеины. 2.Липопротеины. 3.Нуклеопротеины. 4. Фосфопротеины. 5. Металлопротеины. Классификация сложных белков
- 80. Скачать презентацию






















































 Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1)
Электрохимия. Понятие электрохимии. Электроды. Гальванические цепи. Окислительно-восстановительные электроды. (Лекция 6.1) Штучні і синтетичні волокна
Штучні і синтетичні волокна  Химиялық реакция белгілерін атаңыз
Химиялық реакция белгілерін атаңыз Металлы и сплавы с высокой удельной прочностью
Металлы и сплавы с высокой удельной прочностью Физические и химические явления
Физические и химические явления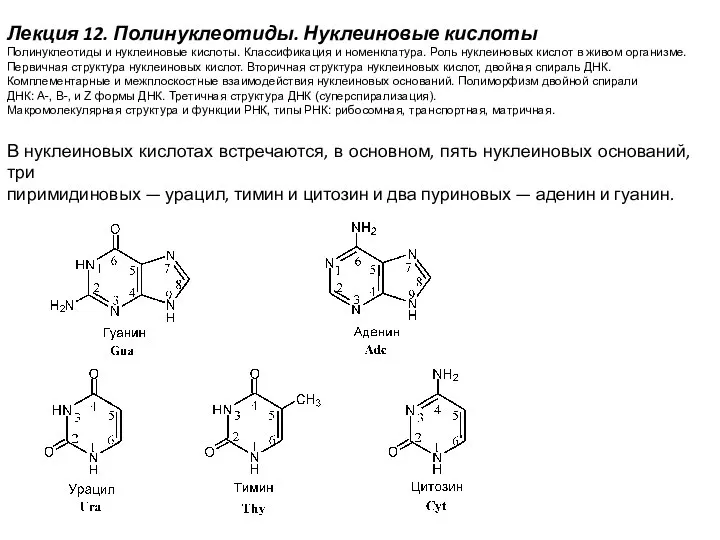 Полинуклеотиды. Нуклеиновые кислоты
Полинуклеотиды. Нуклеиновые кислоты Выдающиеся ученые - химики и их заслуги
Выдающиеся ученые - химики и их заслуги Классификация моющих средств
Классификация моющих средств Узинская ООШ исслед.работа Лобановой Елизаветы
Узинская ООШ исслед.работа Лобановой Елизаветы Молярный объём газообразного вещества
Молярный объём газообразного вещества Материаловедение и технологии конструкционных материалов
Материаловедение и технологии конструкционных материалов Тыңайтқыштар
Тыңайтқыштар Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат
Құрамында металл атомдарымен байланысқан бір немесе бірнеше гидорсотоптары бар күрделі зат Неидеальные растворы
Неидеальные растворы Introduction to metabolism
Introduction to metabolism Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов.
Посвящение в химики. Игра-викторина. Внеклассное мероприятие по химии для учащихся 8 классов. Алкены
Алкены Презентация Лекарства дома
Презентация Лекарства дома Химия (Органическая химия)
Химия (Органическая химия) Цикли трикарбонових кислот
Цикли трикарбонових кислот Алкадиены
Алкадиены Оксиды азота.
Оксиды азота. Общая химия, понятия
Общая химия, понятия Р-элементы IV группы: C, Si, Ge, Sn, Pb
Р-элементы IV группы: C, Si, Ge, Sn, Pb Основні класи неорганічних сполук
Основні класи неорганічних сполук Общая и неорганическая химия
Общая и неорганическая химия Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще
Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии
Применение ЗДМ к равновесиям комплексообразования и их роль в аналитической химии