Содержание
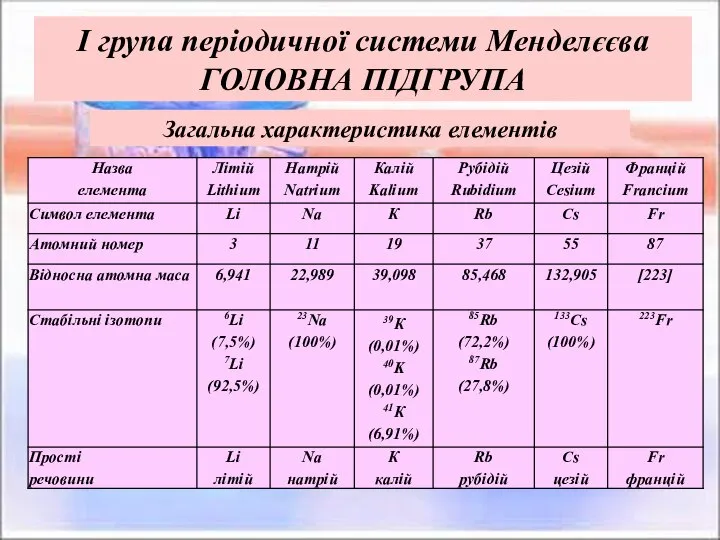
- 2. І група періодичної системи Менделєєва ГОЛОВНА ПІДГРУПА Загальна характеристика елементів
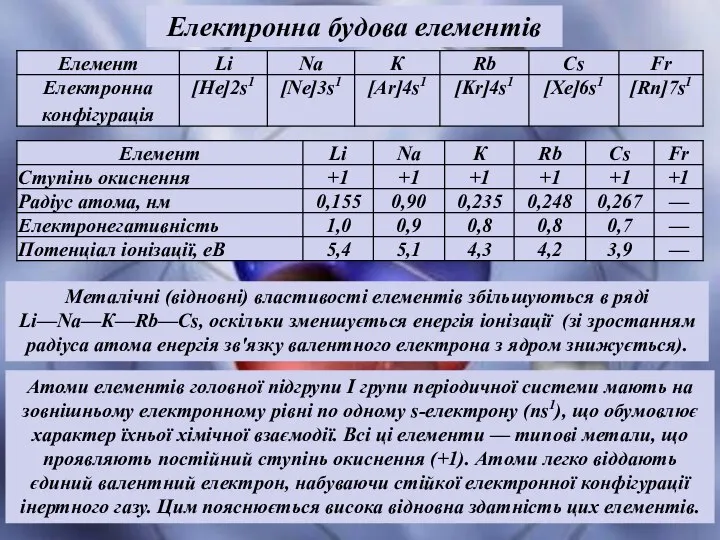
- 3. Електронна будова елементів Металічні (відновні) властивості елементів збільшуються в ряді Li—Na—К—Rb—Cs, оскільки зменшується енергія іонізації (зі
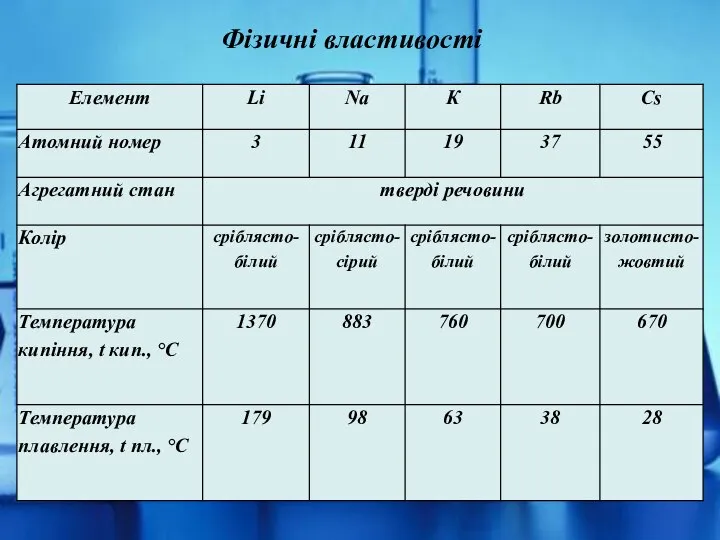
- 4. Фізичні властивості
- 5. Знаходження в природі Літій досить широко розповсюджений. Кількість літію в земній корі досягає 0,002 ат. %.
- 6. Хімічні властивості Основні властивості оксидів посилюються в ряді Li2О — Na2O — К2О — Rb2O —
- 7. Літій — високоактивний метал, тому більшість реакцій, у які він вступає, протікають украй бурхливо. На повітрі
- 8. Натрій оксид одержують тільки непрямим шляхом — нагріванням (t = 180 °С) металу при нестачі кисню:
- 9. На відміну від літію, натрій реагує з азотом і вуглецем тільки при нагріванні: t0 6Na +
- 10. НАТРІЙ ОКСИД І НАТРІЙ ПЕРОКСИД Натрій пероксид Na2O2 — продукт взаємодії металу з киснем. Пероксид натрію
- 11. Хімічні властивості NaOH — сильна основа, добре розчинна у воді. У водному розчині гідроксид натрію дисоціює
- 12. Продукти взаємодії гідроксид натрію з неметалами досить різноманітні: 2NaOH + С12 ↔ NaCl + NaOCl +
- 13. Натрієві солі різних кислот мають величезне промислове значення. Серед них найширше використовуються натрій хлорид, а також
- 14. Натрій сульфат Na2SO4 у техніці зветься просто «сульфат» й у великих кількостях використовується в скляній промисловості.
- 15. Хімічно чисту питну соду одержують, пропускаючи вуглекислий газ через водний розчин натрій карбонату: Na2CO3 + СО2
- 16. Натрій карбонат Na2CO3 або кальцинована сода Біла тверда речовина, яка розчиняється у воді, утворюючи лужний розчин.
- 17. Калій, Рубідій, Цезій і Францій об'єднують в одну підгрупу, оскільки вони є повними електронними аналогами. Відмінність
- 18. КАЛІЙ ТА СПОЛУКИ КАЛІЮ Калій і його аналоги активно окиснюються на повітрі, покриваючись плівкою із продуктів
- 19. Калій і його аналоги при згорянні в повітрі утворюють надпероксиди MetO2, Пероксиди Met2O2 і оксиди Met2O
- 20. Гідроксиди калію і його аналогів — безбарвні гігроскопічні речовини, добре розчинні у воді. Розчинення супроводжується виділенням
- 21. Калій сульфат K2SO4 — один з найважливіших реагентів у скляній промисловості. Його одержання є або побічним
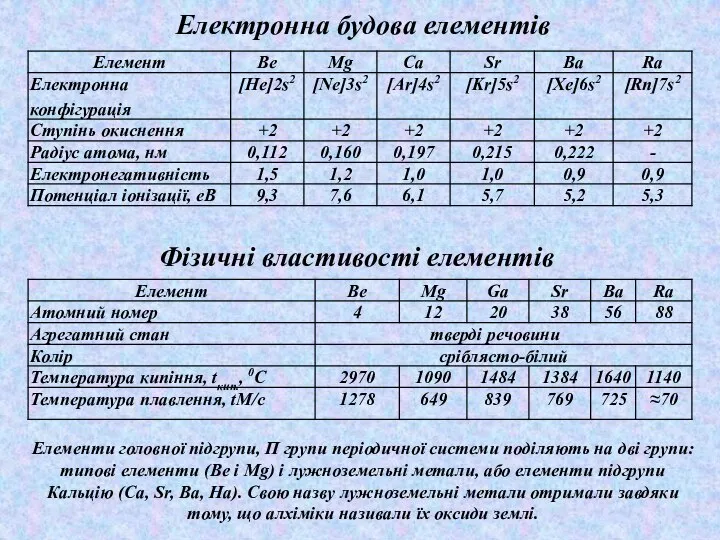
- 22. Електронна будова елементів Елементи головної підгрупи, П групи періодичної системи поділяють на дві групи: типові елементи
- 23. Берилій зустрічається в природі досить рідко. Його кількість у земній корі не перевищує 0,001 ат. %.
- 24. Кількість Кальцію у земній корі наближається до кількості Магнію (1,5 ат. %). Він входить до складу
- 25. Берилій і його аналоги — типові метали. Вони проявляють себе як сильні відновники. У сполуках ці
- 26. Для всіх елементів підгрупи характерні такі хімічні властивості: 1. Горіння: Met + О2 = MetO (для
- 27. БЕРИЛІЙ. СПОЛУКИ БЕРІЛІЮ Хімічні властивості Берилій є типовим амфотерним елементом. Берилій проявляє подібність із елементом, що
- 28. Бериліди d-елементів (ТіВе12, ТаВе12, NbB11 та ін.) украй тугоплавкі й стійкі до дії окисників навіть при
- 29. Горіння магнію описується наступним рівнянням: 2Mg + О2 = 2MgO + Q При цьому виділяється така
- 30. Взаємодія магнію з азотом супроводжує горіння на повітрі: 3Mg + N2 = Mg3N2 Магній активно взаємодіє
- 31. Наприклад, у ряді сполук Магнію з елементами III періоду зліва направо відбувається зменшення частки металевого й
- 32. Магній оксид MgO (палена магнезія) — біла кристалічна речовина. Дуже тугоплавкий (tпл. = 2800 °С). У
- 33. Магній гідроксид Mg(OH)2 — нерозчинна у воді речовина білого кольору. Легко розчиняється в кислотах: Mg(OH)2 +
- 34. ПІДГРУПА КАЛЬЦІЮ Підгрупу Кальцію (підгрупу лужноземельних металів) складають Кальцій, Стронцій, Барій і Радій. Виділення їх в
- 35. Сполуки (карбіди, сульфіди, нітриди й фосфіди) піддаються гідролізу з утворенням погано розчинного у воді кальцій гідроксиду:
- 36. Знаходячись в ряді напруг задовго до Гідрогену, лужноземельні метали настільки активні, що витісняють водень не тільки
- 37. Кальцій оксид СаО — типовий основний оксид. Він бурно реагує з водою з виділенням великої кількості
- 38. Продукт реакції Са(ОН)2 називають гашеним вапном. Розчин Са(ОН)2 у воді називають вапняним молоком. Основні властивості СаО
- 39. Одночасно із зазначеним явищем, під час затвердіння вапняного розчину відбувається утворення кальцій силікату відповідно до рівняння:
- 40. , Згодом розчин знову стає прозорим, оскільки кальцій карбонат переходить у розчинний гідрокарбонат: CaCO + H2O
- 41. , «Схоплювання» цементу описується наступними реакціями: Ca3SiO5 + 5Н2О = Ca2SiO4 • 4Н2О + Са(ОН)2 Ca2SiO4
- 42. , Скелет тварин. Сполуки кальцію виявлені у кістках та зубах.
- 43. , Природні води містять у розчиненому вигляді деякі солі. Наявність у воді іонів Са2+, Mg2+ й
- 44. , У результаті кип'ятіння відбувається руйнування гідрокарбонату, виділяється вуглекислий газ і випадає в осад нерозчинний карбонат
- 45. , Всі указані недоліки води можна усунути шляхом її пом'якшення. Розрізняють фізичні й хімічні методи пом'якшення.
- 46. , За типом іонів, які обмінюють іонообмінники, останні поділяють на катіоніти, аніоніти й амфоліти. Катіоніти містять
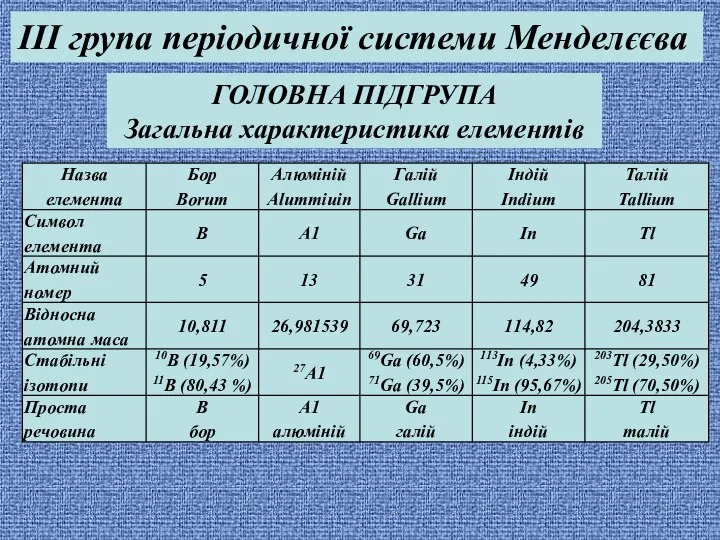
- 47. , ГОЛОВНА ПІДГРУПА Загальна характеристика елементів IІІ група періодичної системи Менделєєва
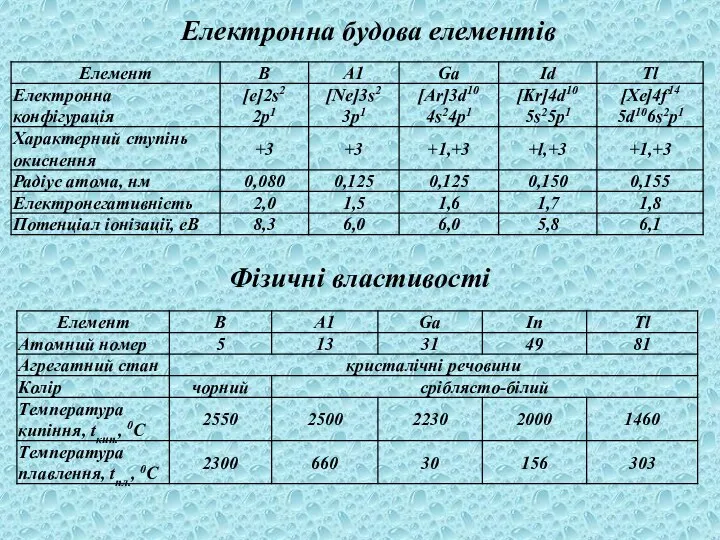
- 48. , Електронна будова елементів Фізичні властивості
- 49. , Відновні (металічні) властивості елементів підгрупи посилюються зі зростанням радіуса атома. Із цієї закономірності вибивається лише
- 50. , Хімічна активність елементів у підгрупі посилюється зверху вниз. У цьому ж напрямку відбувається посилення металічних
- 51. , Для всіх елементів головної підгрупи характерним є утворення оксидів із загальною формулою R2O3 (для Талію
- 52. , Бор активно взаємодіє з киснем. 4В + 3О2 = 2В2О3 Бор оксид В2О3 (борний ангідрид)
- 53. , Реакція нейтралізації ортоборної кислоти лугами призводить до утворення солей тетраборної кислоти: 4Н3ВО3 + 2NaOH =
- 54. , Галогеніди бору мають загальну формулу ВНа13. Це легкоплавкі мономірні сполуки, що не мають забарвлення. Бор
- 55. , Бор карбід В4С — чорна блискуча кристалічна речовина. Утворюється при розжарюванні суміші вільного бору або
- 56. , Алюміній належить до активних елементів — у ряді напруг він займає місце після лужноземельних металів.
- 57. , З воднем алюміній не взаємодіє, але з більшістю неметалів реагує, хоча й при високих температурах.
- 58. , Оскільки алюміній активний метал, він легко витісняє водень із кислот (крім нітратної): 2А1 + 6НС1
- 59. , У водяних розчинах лугів алюміній розчиняється з утворенням комплексної сполуки: 2Al + 2NaOH +10Н2O =
- 60. , А12О3 — амфотерний оксид, у кислотах вів розчиняється з утворенням солі й води: А12О3 +
- 61. , Солі алюмінію, як і алюмінати, у розчині піддаються гідролізу, тому можуть існувати тільки в сильнокислому
- 62. , Природний А12О3 (корунд) — дуже тверда речовина; він застосовується для виготовлення шліфувальних приладів. У роздробленому
- 63. , Сульфат алюмінію Al2(SO4)3 Біла водорозчинна кристалічна речовина, яка використовується для очищення води та у виробництві
- 65. Скачать презентацию
























































 Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Химия биогенных элементов
Химия биогенных элементов Химические элементы в быту
Химические элементы в быту Углеводороды. Структура и функции биолекул
Углеводороды. Структура и функции биолекул Полисилоксаны. Классификация полимеров
Полисилоксаны. Классификация полимеров Методы познания химии
Методы познания химии Высокомолекулярные соединения (ВМС) или полимеры
Высокомолекулярные соединения (ВМС) или полимеры Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения: Используя оксид ртути (II) напишит
Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения: Используя оксид ртути (II) напишит Ювелирное дело. Империя самоцветов
Ювелирное дело. Империя самоцветов Алкандар. (қаныққан көмірсутектер. Парафиндер.)
Алкандар. (қаныққан көмірсутектер. Парафиндер.) Определение подлинности лекарственных веществ
Определение подлинности лекарственных веществ Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Строение твердого вещества
Строение твердого вещества Золото. Свойство золота
Золото. Свойство золота Сверхразветвленные полимеры: типы, получение, применение
Сверхразветвленные полимеры: типы, получение, применение Арены. Бензол
Арены. Бензол В гостях у Хозяйки Медной горы. Покровская сельская библиотека
В гостях у Хозяйки Медной горы. Покровская сельская библиотека Рождающий воду
Рождающий воду Химическая связь
Химическая связь Газообразные вещества
Газообразные вещества Ртуть. Нахождение в природе. Применение
Ртуть. Нахождение в природе. Применение Изомерия комплексных соединений
Изомерия комплексных соединений Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Вспомогательные вещества. Флюсы и их применение. Кислоты, соли, щёлочи применяемые в ювелирном деле. (Лекция 3)
Вспомогательные вещества. Флюсы и их применение. Кислоты, соли, щёлочи применяемые в ювелирном деле. (Лекция 3) Производство синтетических моющих средств
Производство синтетических моющих средств Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду
Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду Твердофазное восстановление металлов и образование карбидов из хромовых концентратов Аганозерского месторождения
Твердофазное восстановление металлов и образование карбидов из хромовых концентратов Аганозерского месторождения Простейшие операции с веществом (химический практикум)
Простейшие операции с веществом (химический практикум)