Содержание
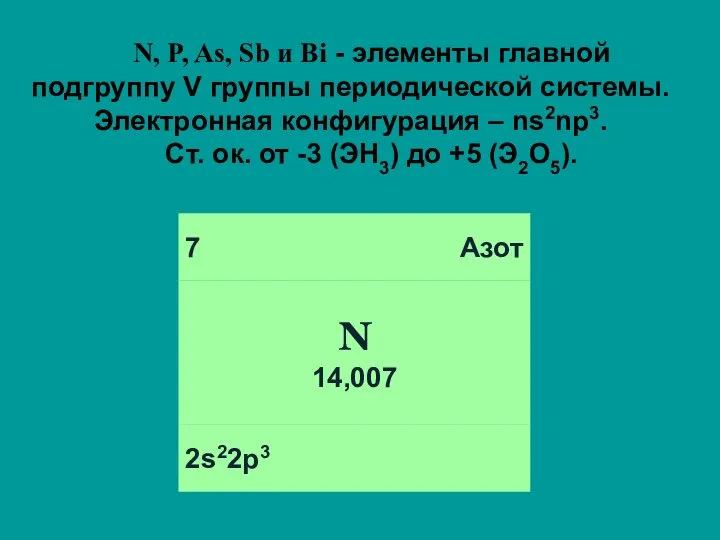
- 2. N, P, As, Sb и Bi - элементы главной подгруппу V группы периодической системы. Электронная конфигурация
- 3. Азот. В природе: NaNO3 (чилийская или натриевая селитра) и калия KNO3 (индийская или калиевая селитра). Осадки
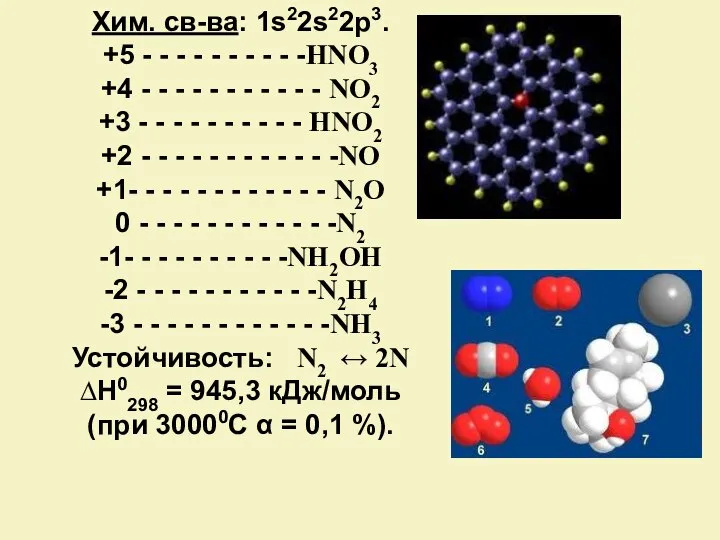
- 4. Хим. св-ва: 1s22s22p3. +5 - - - - - - - - - -HNO3 +4 -
- 5. Ст.ок. -3 Нитриды: основные (Na3N, Mg3N2), амфотерные (AlN), кислотные (Si3N4). Необратимый гидролиз: Li3N + 3H2O →
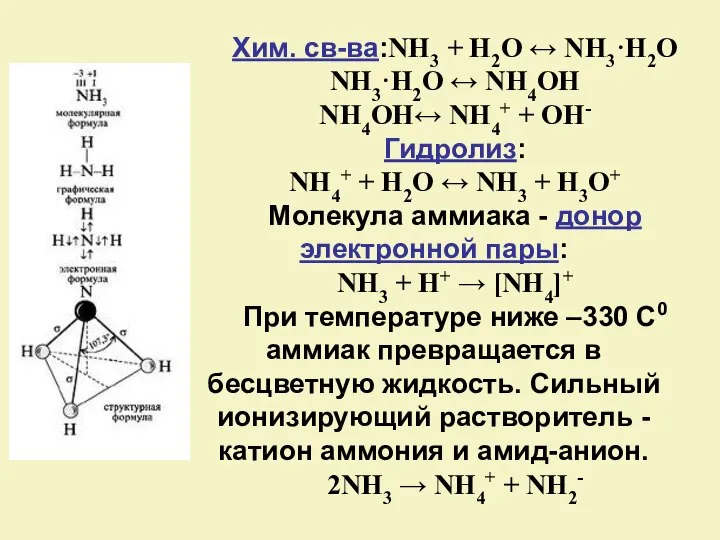
- 6. Хим. св-ва:NH3 + H2O ↔ NH3·H2O NH3·H2O ↔ NH4OH NH4OH↔ NH4+ + OH- Гидролиз: NH4+ +
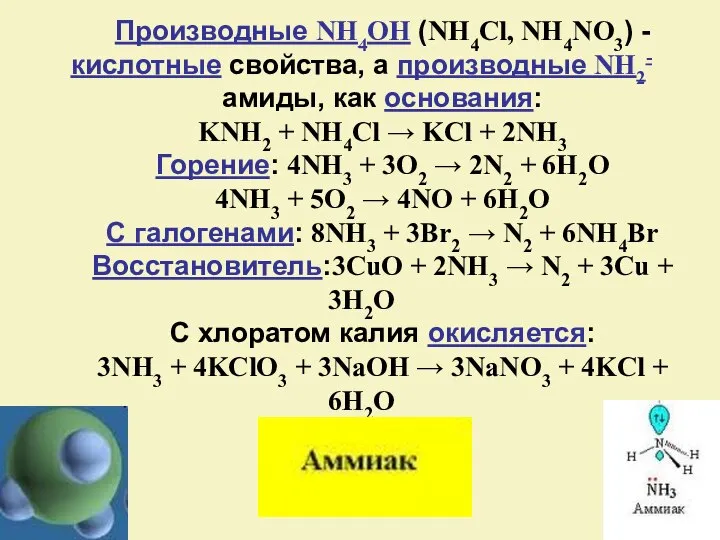
- 7. Производные NH4OH (NH4Cl, NH4NO3) - кислотные свойства, а производные NH2- амиды, как основания: KNH2 + NH4Cl
- 8. C щелоч. и щел-зем. Ме образует амиды металлов: 2Na + 2NH3 → 2NaNH2 + H2 Соли
- 9. Соли аммония - реакционноспособны. NH4Cl (нашатырь) - для удаления оксидных пленок:4CuO + 2NH4Cl → 3Cu +
- 10. N2H4 – ионизир. растворитель, щелочная реакция: N2H4 + H2O = N2H5+ + OH- N2H5+ + H2O
- 11. Получают а). Пропуская NO и H2 через Pt: 2NO + 3H2 → 2NH2OH б). Восстановление путем
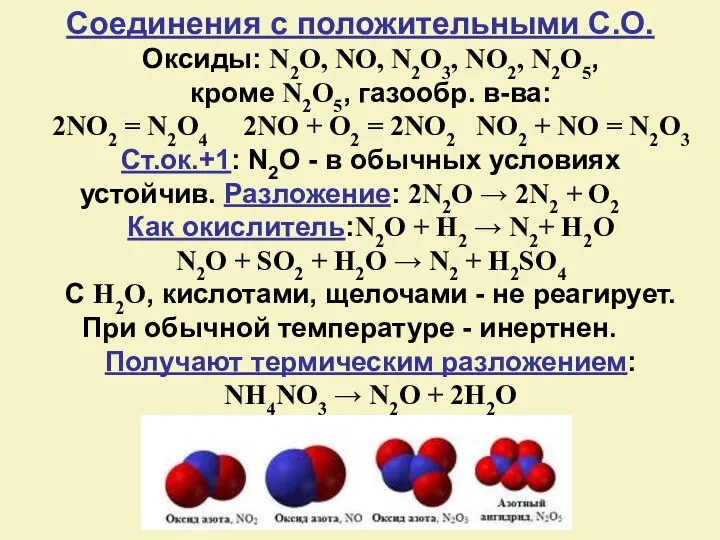
- 12. Оксиды: N2O, NO, N2O3, NO2, N2O5, кроме N2O5, газообр. в-ва: 2NO2 = N2O4 2NO + O2
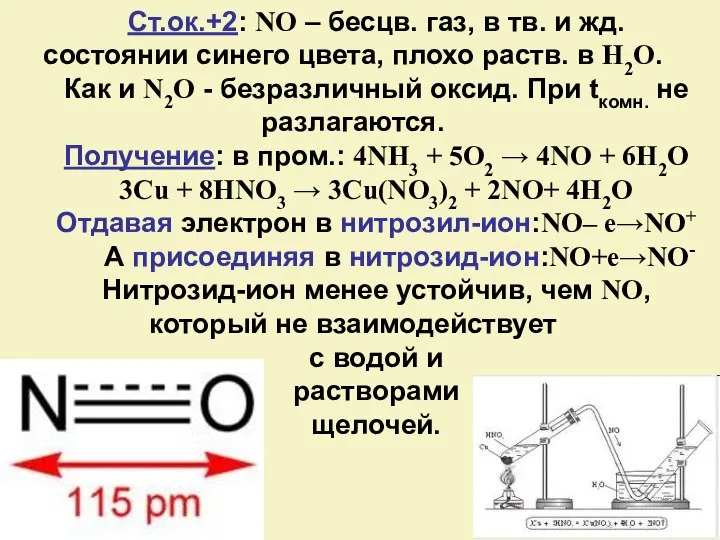
- 13. Ст.ок.+2: NO – бесцв. газ, в тв. и жд. состоянии синего цвета, плохо раств. в H2O.
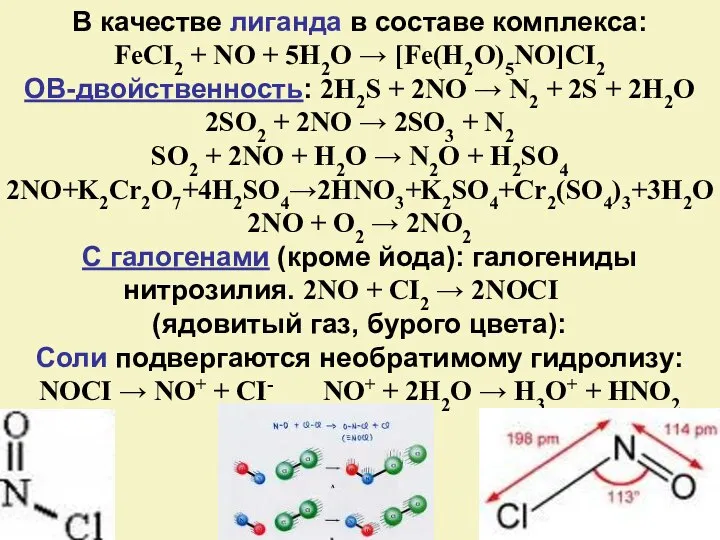
- 14. В качестве лиганда в составе комплекса: FeCI2 + NO + 5H2O → [Fe(H2O)5NO]CI2 ОВ-двойственность: 2H2S +
- 15. Ст.ок.+3: оксид N2O3, HNO2 и ее солях. N2O3 - бурый яд. газ, при t ниже –400С
- 16. В конц. р-ах или при высоких температурах распадается: 3HNO2 → HNO3 + 2NO + H2O Разлагается:
- 17. Нитриты щел. Ме плавятся, а остальные разлагаются: Ca(NO2)2 → CaO + NO2 + NO AgNO2 →
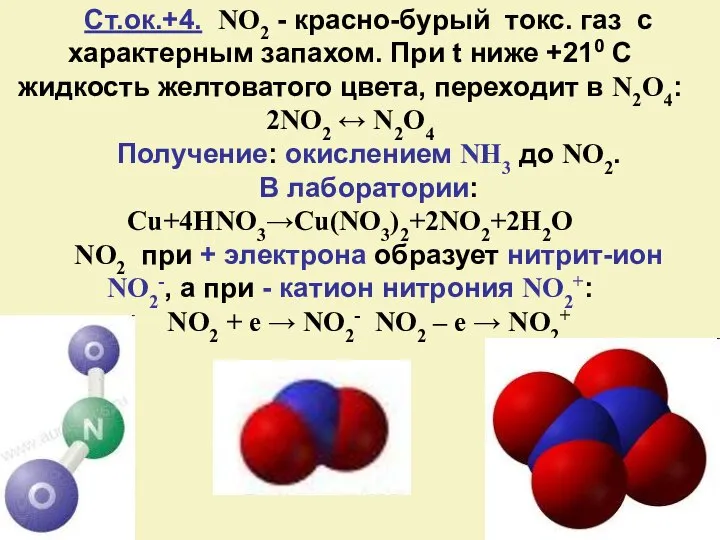
- 18. Ст.ок.+4. NO2 - красно-бурый токс. газ с характерным запахом. При t ниже +210 С жидкость желтоватого
- 19. Диспропорционирование: 2NO2+H2O→HNO2+HNO3 2NO2 + 2KOH → KNO2 + KNO3 + H2O C водой: 4NO2 + O2
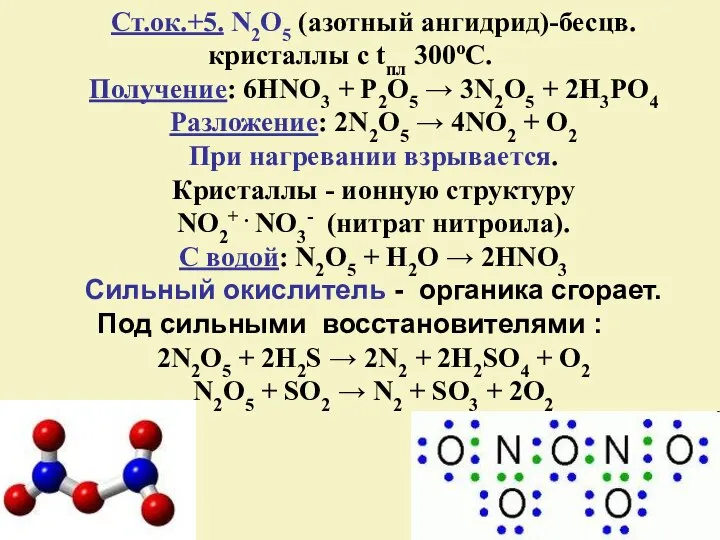
- 20. Ст.ок.+5. N2O5 (азотный ангидрид)-бесцв. кристаллы с tпл 300оС. Получение: 6HNO3 + P2O5 → 3N2O5 + 2H3PO4
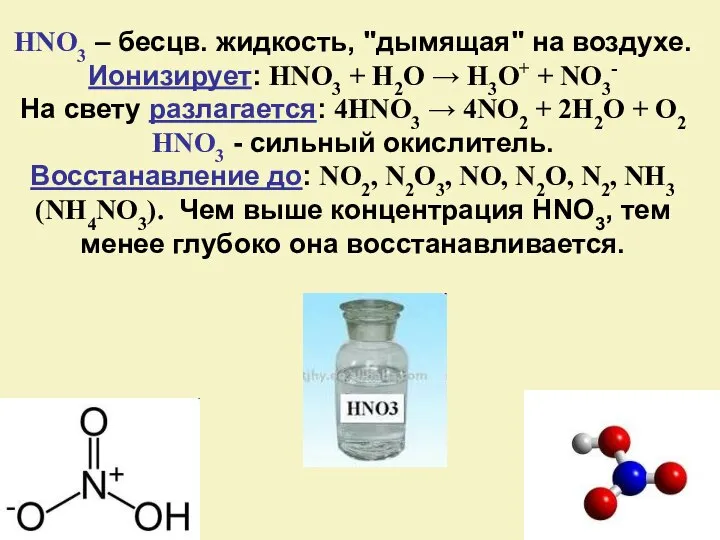
- 21. HNO3 – бесцв. жидкость, "дымящая" на воздухе. Ионизирует: HNO3 + H2O → H3O+ + NO3- На
- 22. При взаимодействии Ме с HNO3 водород не выделяется. Окисляясь, он образует воду. Конц. HNO3 (W =
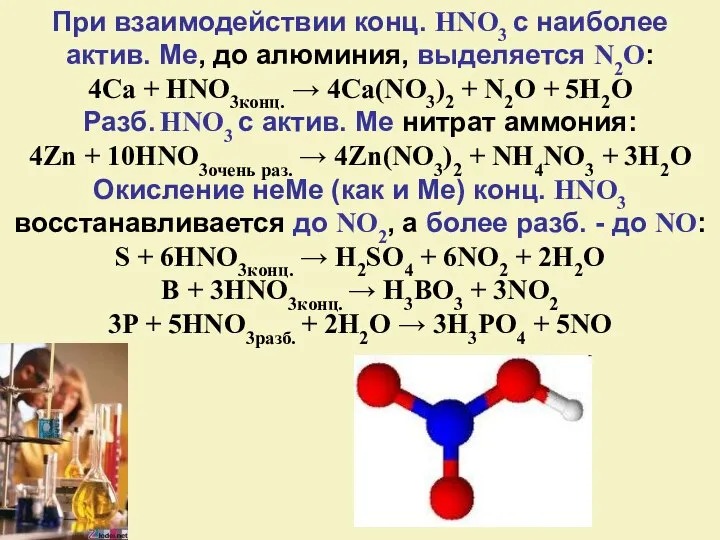
- 23. При взаимодействии конц. HNO3 с наиболее актив. Ме, до алюминия, выделяется N2O: 4Ca + HNO3конц. →
- 24. Смесь конц. HCl и конц. HNO3 3:1 - "царская водка“, т.к. растворяет Au и Pt. Более
- 25. Окисление Ме с избытком HCl – комплексы: H[AuCl4] и H2[PtCl6]. Соли азотной кислоты:нитраты – бесцв. кристалл.
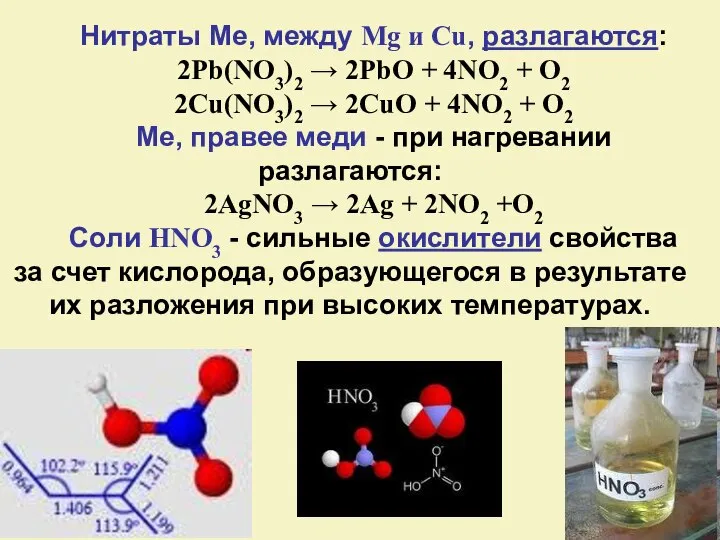
- 26. Нитраты Ме, между Mg и Cu, разлагаются: 2Pb(NO3)2 → 2PbO + 4NO2 + O2 2Cu(NO3)2 →
- 27. Нитраты применяют для легко воспламеняющихся и взрывчатых смесей (например, черного пороха: 68% KNO3, 15% S u
- 29. Скачать презентацию












![Окисление Ме с избытком HCl – комплексы: H[AuCl4] и H2[PtCl6]. Соли](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1397692/slide-24.jpg)

 «Пластмаси» Тема проекту:
«Пластмаси» Тема проекту:  Современные проблемы химии. Межфакультетский курс для студентов
Современные проблемы химии. Межфакультетский курс для студентов Физико - химические основы получения лекарственных препаратов (лекция 3)
Физико - химические основы получения лекарственных препаратов (лекция 3) Чистые вещества и смеси
Чистые вещества и смеси Химия в профессиях
Химия в профессиях Азотная кислота и ее свойства
Азотная кислота и ее свойства алгоритм
алгоритм Процессы в растворах: электролитическая диссоциация (ЭД) Презентация подготовлена учителем биологии и химии МОУ СОШ д.Городищ
Процессы в растворах: электролитическая диссоциация (ЭД) Презентация подготовлена учителем биологии и химии МОУ СОШ д.Городищ Применение центрифугирования
Применение центрифугирования Практикум по химической термодинамике и кинетике
Практикум по химической термодинамике и кинетике Көміртек
Көміртек Домашний эксперимент № 7 по химии Цветные опыты - на стыке двух наук
Домашний эксперимент № 7 по химии Цветные опыты - на стыке двух наук Алюминий
Алюминий Реакции Фаворского
Реакции Фаворского Подготовил учитель химии МОУ СОШ № 16 С. Александровского Александровского района Кононенко Светлана Юрьевна
Подготовил учитель химии МОУ СОШ № 16 С. Александровского Александровского района Кононенко Светлана Юрьевна От монументов до безделушек
От монументов до безделушек Нефть Состав, свойства, переработка
Нефть Состав, свойства, переработка  Химический элементы в нашей жизни
Химический элементы в нашей жизни Юные химики
Юные химики Основные сведения о композитах. Понятие о композитах
Основные сведения о композитах. Понятие о композитах Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури
Обчислення швидкості хімічних реакцій в залежності від концентрації реагуючих речовин і температури Презентация по Химии "Лекарства дома" - скачать смотреть
Презентация по Химии "Лекарства дома" - скачать смотреть  Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека».
Информационно-поисковый исследовательский проект: «Влияние пищевых добавок на здоровье человека». Дисахариды Ширяева София ХБ-4 г.Липецк 2012
Дисахариды Ширяева София ХБ-4 г.Липецк 2012 Кислородные соединения азота
Кислородные соединения азота Токсины в быту. Классификация товаров бытовой химии
Токсины в быту. Классификация товаров бытовой химии Реакции замещения и реакции обмена
Реакции замещения и реакции обмена Минеральные вещества
Минеральные вещества