Содержание
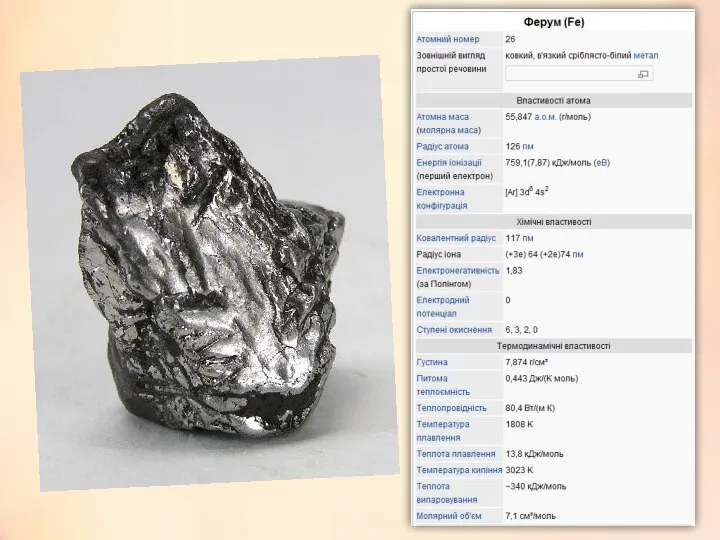
- 3. Ферум – d-елемент VІІІБ групи (або побічної підгрупи VІІІ групи) періодичної системи. Будова атома: 26Fe)2)8)14)2 Електронна
- 4. Поширення в природі За поширеністю у природі ферум посідає друге місце серед металів (після алюмінію). На
- 5. Залізо — блискучий сріблясто-білий важкий метал. Густина його 7,86 т/м³; температура плавлення 1538 °C, температура кипіння
- 6. Хімічні властивості Ферум належить до восьмої групи періодичної системи елементів Менделєєва. Його атоми на зовнішній електронній
- 7. При нагріванні залізо може легко реагувати з хлором, сіркою та іншими неметалами: 2Fe + 3Cl2 =
- 8. Цікаві перетворення сполук Феруму Якісні реакції на сполуки Fe2+ та Fe3+ Реакція солі тривалентного Феруму (Fe2(SO4)3)
- 9. Використання жовтої та червоної кров’яних солей Жовта кров’яна сіль (калій гексаціаноферат (ІІ) K4[Fe (CN)6]) – реактив
- 10. Раніше вважали, що берлінська лазур і турнбулева синь – різні речовини, зараз вже відомо, що в
- 11. Чисте залізо має досить обмежене застосування. Його використовують при виготовленні сердечників електромагнітів та якорів електромашин, як
- 12. Ферум є біологічно важливим елементом. Він міститься в організмах усіх тварин і в рослинах. Ферум входить
- 13. Цікаві факти про залізо Які істоти винні в кольорі Кривавого водоспаду в Антарктиді? В Антарктиді з
- 14. Перше залізо, як метал, потрапило до рук людини «з неба». Не дарма люди вважали залізо -
- 16. Скачать презентацию
Ферум – d-елемент VІІІБ групи (або побічної підгрупи VІІІ групи) періодичної
Ферум – d-елемент VІІІБ групи (або побічної підгрупи VІІІ групи) періодичної
Будова атома: 26Fe)2)8)14)2
Електронна конфігурація атома Феруму: 1s22s22p62s23p63d64s2
Розміщення електронів зовнішнього і передостаннього енергетичних рівнів за енергетичними комірками:
В атомі Феруму вісім валентних електонів (3d64s2), тому він виявляє змінні ступені окиснення.
Найхарактерніші ступені окиснення +2 і +3
Будова атома Феруму
Поширення в природі
За поширеністю у природі ферум посідає друге місце серед
Поширення в природі
За поширеністю у природі ферум посідає друге місце серед
Найважливішими природними сполуками феруму, що мають промислове значення, є магнітний залізняк Fe3O4, червоний залізняк Fe2O3, бурий залізняк Fe2O3 · nH2O та пірит FeS2. Оксиди феруму служать рудами, з яких добувають залізо, а пірит — сировиною для сульфатно-кислотного виробництва.
Гідротермальне джерело з високим вмістом заліза
Найважливіші мінерали феруму: гематит Fe2O3 (70 % Fe), магнетит Fe3O4 (72,4 % Fe), ґетит FeOOH (62,9 % Fe), лепідокрокіт FeO(OH) (62,9 % Fe), лімоніт — суміш гідрооксидів Fe з SiO2 та ін. речовинами (40-62 % Fe), сидерит FeCO3 (48,2 % Fe), ільменіт FeTiO3 (36,8 % Fe), шамозит (34-42 % FeO), вівіаніт (43,0 % FeO), скородит (34,6 % Fe2О3), ярозит (47,9 % Fe2О3) та ін.
Залізо — блискучий сріблясто-білий важкий метал.
Густина його 7,86 т/м³;
температура
Залізо — блискучий сріблясто-білий важкий метал.
Густина його 7,86 т/м³;
температура
Фізичні властивості
Хімічні властивості
Ферум належить до восьмої групи періодичної системи елементів Менделєєва. Його
Хімічні властивості
Ферум належить до восьмої групи періодичної системи елементів Менделєєва. Його
У сухому повітрі за звичайної температури залізо досить стійке, але у вологому швидко іржавіє, вкриваючись товстим шаром іржі. Іржа є сумішшю оксидів і гідроксидів феруму. Основну частину іржі складає сесквіоксид заліза Fe2O3 і тригідроксид заліза Fe(OH)3. Крім того, до її складу входить монооксид заліза FeO, дигідроксид заліза Fe(OH)2 та інші сполуки.
Процес ржавіння заліза можна зобразити такими приблизними рівняннями:
2Fe + O2 + 2Н2О = 2Fe(OH)2
4Fe(OH)2 + O2 + 2Н2О = 4Fe(OH)3
Fe(OH)2 = FeO + H2O
2Fe(OH)3 = Fe2O3 + 3H2O
При нагріванні залізо може легко реагувати з хлором, сіркою та іншими
При нагріванні залізо може легко реагувати з хлором, сіркою та іншими
2Fe + 3Cl2 = 2FeCl3
Fe + S = FeS
В електрохімічному ряді напруг залізо стоїть лівіше від водню, тому воно легко реагує з розведеними хлоридною і сульфатною кислотами:
Fe + 2HCl = FeCl2 + Н2 ↑
Fe + H2SO4 = FeSO4 + H2 ↑
З розведеною нітратною кислотою залізо теж легко реагує:
Fe + HNO3 + 3HNO3 = Fe (NO3)3 + 2H2O + NO ↑
Але з концентрованою нітратною і концентрованою сульфатною кислотами без нагрівання залізо не реагує. Воно стає «пасивним», вкриваючись тонкою оксидною плівкою, яка не розчиняється в кислотах і ізолює метал від дії кислоти. Завдяки цьому концентровану нітратну і концентровану сульфатну кислоту можна зберігати і транспортувати в залізній тарі.
Залізо може відновлювати менш активні метали з розчинів їхніх солей, наприклад:
Fe + CuSO4=FeSO4 + Cu
Горіння заліза в кисні
Утворення ферум (II) сульфіду
Цікаві перетворення сполук Феруму
Якісні реакції на сполуки Fe2+ та Fe3+
Реакція солі
Цікаві перетворення сполук Феруму
Якісні реакції на сполуки Fe2+ та Fe3+
Реакція солі
Взаємодія ферум(ІІІ) хлориду з калій тіоцианатом
Використання жовтої та червоної кров’яних солей
Жовта кров’яна сіль (калій гексаціаноферат
Використання жовтої та червоної кров’яних солей
Жовта кров’яна сіль (калій гексаціаноферат
FeCl3 + K4[Fe (CN)6] =KFe[Fe (CN)6] + 3KCl
або в йонному вигляді
Fe3+ + [Fe(CN)6]4− → Fe[Fe(CN)6] −
Утворюється осад синього кольору , який називають «берлінська лазур».
Якісна реакція на солі тривалентного Феруму
Червона кров’яна сіль (калій гексаціаноферат (ІІІ) K3[Fe (CN)6]) - реактив на Fe2+
в результаті реакції утворюється речовина синього кольору «турнбулева синь».
4Fe2+ + 3[Fe(CN)6]3− → FeIII4[FeII(CN)6]3↓
Якісна реакція на солі двовалентного Феруму
Раніше вважали, що берлінська лазур і турнбулева синь – різні речовини,
Раніше вважали, що берлінська лазур і турнбулева синь – різні речовини,
"Турнбулева синь"
"Берлінська лазур"
Чисте залізо має досить обмежене застосування. Його використовують при виготовленні сердечників
Чисте залізо має досить обмежене застосування. Його використовують при виготовленні сердечників
Застосування
Залізний порошок використовують при зварюванні, а також для цементації міді.
Залізовуглецеві сплави чавун і сталь — основний конструкційний матеріал, що застосовується у всіх галузях промисловості. Виробництво заліза та його сплавів становить більше 90 % виробництва всіх металів і утворює окрему галузь промисловості — чорну металургію.
Сталі містять до 2,14 % карбону, чавун — понад 2,14 %. Фундаментом науки про сталь і чавун, як сплави заліза з вуглецем є діаграма стану сплавів залізо-вуглець — графічне відображення фазового стану сплавів заліза з вуглецем в залежності від їх хімічного складу і температури.
Ферум є біологічно важливим елементом. Він міститься в організмах усіх тварин
Ферум є біологічно важливим елементом. Він міститься в організмах усіх тварин
Біологічна роль заліза
Цікаві факти про залізо
Які істоти винні в кольорі Кривавого водоспаду в
Цікаві факти про залізо
Які істоти винні в кольорі Кривавого водоспаду в
В Антарктиді з льодовика Тейлора часом виходить Кривавий водоспад. Вода в ньому містить двовалентне залізо, яке, з'єднуючись з атмосферним повітрям, окислюється і утворює іржу. Це і надає водоспаду криваво-рудий колір. Однак двовалентне залізо у воді виникає не просто так - його виробляють бактерії, що живуть в ізольованому від зовнішнього світу водоймі глибоко під льодом. Ці бактерії зуміли організувати життєвий цикл при повній відсутності сонячного світла і кисню. Вони переробляють залишки органіки, а «дихають» тривалентні залізом з навколишніх порід.
Різнобарвний метал з візерунком
Немає нічого незвичайного в тому, що будь-який з відомих нам металів, піддаючись будь-якої обробці, може змінювати колір. Колір того чи іншого металу залежить і від ступеня нагріву, і від самої обробки, і від хімічних властивостей. Але неможливо уявити блакитне золото або червоне срібло. Навпаки, залізо, а відповідно, і сталь, і чавун у всіх своїх «іпостасях» мають незрівнянну ні з яким іншим металом колірну палітру. У холодному стані воно може бути сірим і чорним, майже білим, блакитним і синім, золотавим і червонуватим. Більше того, залізо є єдиним металом, який може сам себе прикрашати декоративним орнаментом, що проступає як би зсередини. Варіанти цього фактурного орнаменту нескінченні, і їх не можна зарахувати до жодного із загальновідомих, так як цей малюнок народжується самим металом.
Перше залізо, як метал, потрапило до рук людини «з неба».
Перше залізо, як метал, потрапило до рук людини «з неба».
Залізо в організм тварин і людини надходить з їжею. Найбільш багаті залізом такі продукти, як м'ясо, печінка, яйця, бобові, крупи, хліб, буряк. Цікаво зауважити, що колись у цей список був помилково внесено шпинат (з причини друкарські помилки в записах результатів аналізу, а саме був загублений «зайвий» нуль після розділової коми).












 Химические свойства оксидов
Химические свойства оксидов Химические элементы в организме человека Выполнил ученик 9 «Г» класса МОУ «сош №50» Жадан Михаил
Химические элементы в организме человека Выполнил ученик 9 «Г» класса МОУ «сош №50» Жадан Михаил Теория электролитической диссоциации
Теория электролитической диссоциации Плотнейшие упаковки одинаковых сфер
Плотнейшие упаковки одинаковых сфер Алканы. Алкены. Алкины
Алканы. Алкены. Алкины Аттестационная работа. Образовательная программа, элективный курс Химия в задачах и упражнениях
Аттестационная работа. Образовательная программа, элективный курс Химия в задачах и упражнениях Неорганические вяжущие вещества. (Лекция 6)
Неорганические вяжущие вещества. (Лекция 6) Периодический закон и периодическая система элементов Д.И. Менделеева
Периодический закон и периодическая система элементов Д.И. Менделеева Полімери. Будова і властивості полімерів
Полімери. Будова і властивості полімерів Свойства серной кислоты и солей
Свойства серной кислоты и солей Диспергаторы. Добавки для печатных красок
Диспергаторы. Добавки для печатных красок Діагностика за показами газоаналізатора. Типи газоаналізаторів
Діагностика за показами газоаналізатора. Типи газоаналізаторів Article review. Getting a two-component cold-cast products in polyurethane silicone mold in a vacuum
Article review. Getting a two-component cold-cast products in polyurethane silicone mold in a vacuum Периодический закон и периодическая система Д.И. Менделеева
Периодический закон и периодическая система Д.И. Менделеева Топливо. Механические топки
Топливо. Механические топки Антибиотики как лекарственные вещества. Источники получения. Классификация
Антибиотики как лекарственные вещества. Источники получения. Классификация Определение содержания растворенного кислорода в природной воде
Определение содержания растворенного кислорода в природной воде Виды присадок к моторным топливам (бензин)
Виды присадок к моторным топливам (бензин) Э.М. Спиридонов. Эволюция минералов ртути в зоне гипергенеза
Э.М. Спиридонов. Эволюция минералов ртути в зоне гипергенеза Производные салициловой и индолуксусной кислоты
Производные салициловой и индолуксусной кислоты Лантаноидтар. Лантаноидтардың қасиеттері
Лантаноидтар. Лантаноидтардың қасиеттері Химический состав и физические свойства продовольственных товаров
Химический состав и физические свойства продовольственных товаров Железо
Железо Выделение нефтегазоматеринских пород по данным пиролиза. Построение геохимического разреза
Выделение нефтегазоматеринских пород по данным пиролиза. Построение геохимического разреза Белки и пептиды. Ферменты
Белки и пептиды. Ферменты Хімія у побуті
Хімія у побуті  Гормоны
Гормоны  Происхождение жизни на Земле
Происхождение жизни на Земле