Содержание
- 2. Антибиотики – вещества продуцируемые микроорганизмами, высшими растениями, животными тканями в процессе их жизнедеятельности и продукты модификации
- 3. СПОСОБЫ ПОЛУЧЕНИЯ АНТИБИОТИКОВ: 1). Микробиологический синтез на основе плесневых (Penicillum) или лучистых (Streptomyces) грибов. Включает такие
- 4. КЛАССИФИКАЦИЯ АНТИБИОТИКОВ 1. По молекулярному механизму действия: нарушение синтеза клеточной оболочки (пенициллины, цциклосерин); мембраноактивные антибиотики (полиены,
- 5. 3. Химическая классификация атибиотиков: 1). Антибиотики алициклического строения (группа тетрациклинов и их полусинтетические аналоги); 2). Антибиотики
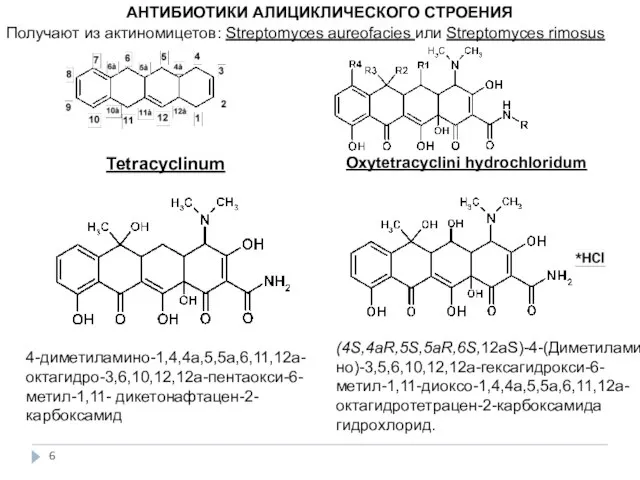
- 6. АНТИБИОТИКИ АЛИЦИКЛИЧЕСКОГО СТРОЕНИЯ Tetracyclinum 4-диметиламино-1,4,4а,5,5а,6,11,12а-октагидро-3,6,10,12,12а-пентаокси-6-метил-1,11- дикетонафтацен-2-карбоксамид Oxytetracyclini hydrochloridum (4S,4aR,5S,5aR,6S,12аS)-4-(Диметиламино)-3,5,6,10,12,12а-гексагидрокси-6-метил-1,11-диоксо-1,4,4а,5,5а,6,11,12а-октагидротетрацен-2-карбоксамида гидрохлорид. Получают из актиномицетов: Streptomyces aureofacies или
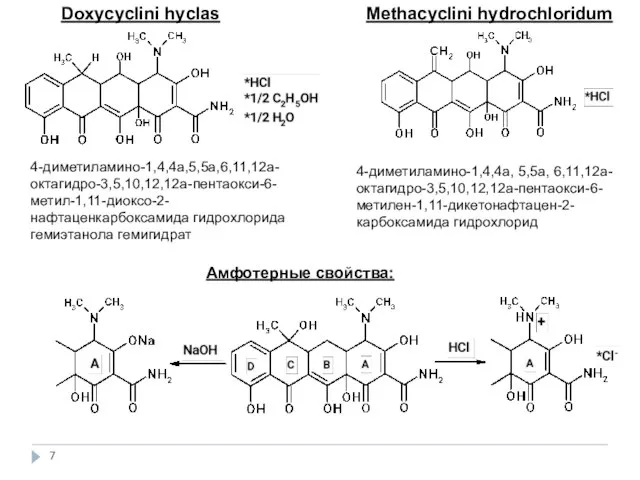
- 7. Doxycyclini hyclas 4-диметиламино-1,4,4а,5,5а,6,11,12а-октагидро-3,5,10,12,12а-пентаокси-6-метил-1,11-диоксо-2-нафтаценкарбоксамида гидрохлорида гемиэтанола гемигидрат Methacyclini hydrochloridum 4-диметиламино-1,4,4а, 5,5а, 6,11,12а-октагидро-3,5,10,12,12а-пентаокси-6-метилен-1,11-дикетонафтацен-2-карбоксамида гидрохлорид Амфотерные свойства:
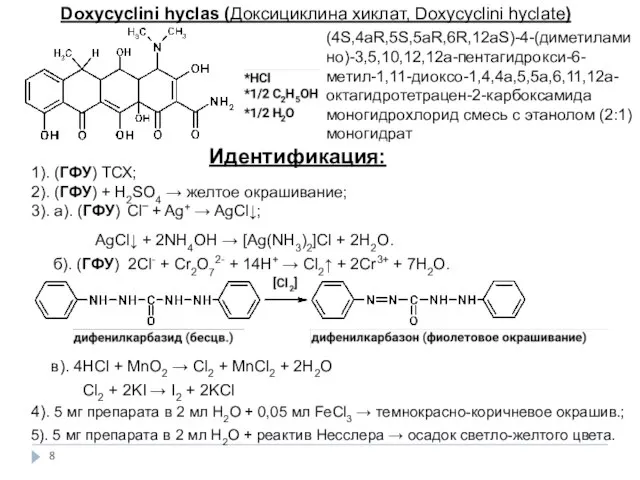
- 8. Doxycyclini hyclas (Доксициклина хиклат, Doxycyclini hyclate) (4S,4aR,5S,5aR,6R,12aS)-4-(диметиламино)-3,5,10,12,12а-пентагидрокси-6-метил-1,11-диоксо-1,4,4а,5,5а,6,11,12а-октагидротетрацен-2-карбоксамида моногидрохлорид смесь с этанолом (2:1) моногидрат Идентификация: 1). (ГФУ)
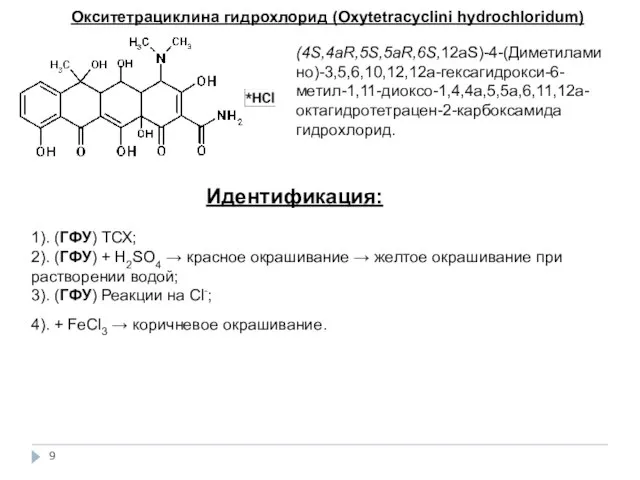
- 9. Окситетрациклина гидрохлорид (Oxytetracyclini hydrochloridum) (4S,4aR,5S,5aR,6S,12аS)-4-(Диметиламино)-3,5,6,10,12,12а-гексагидрокси-6-метил-1,11-диоксо-1,4,4а,5,5а,6,11,12а-октагидротетрацен-2-карбоксамида гидрохлорид. Идентификация: 1). (ГФУ) ТСХ; 2). (ГФУ) + H2SO4 → красное
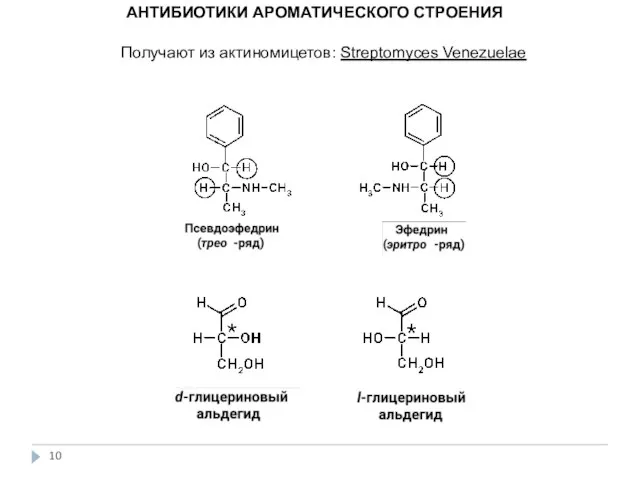
- 10. АНТИБИОТИКИ АРОМАТИЧЕСКОГО СТРОЕНИЯ Получают из актиномицетов: Streptomyces Venezuelae
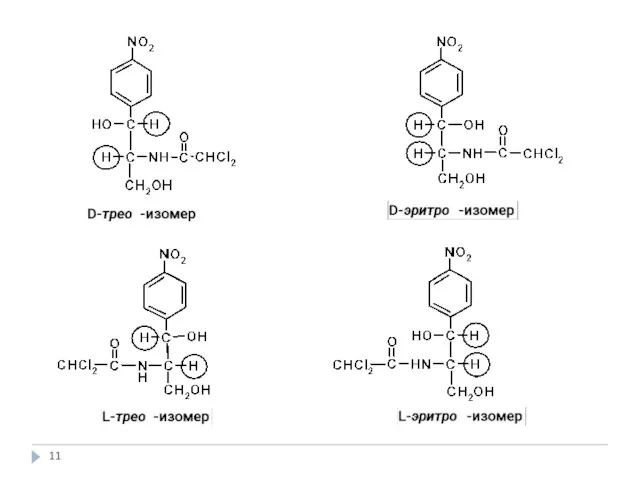
- 12. Левомицетин Сhloramphenicolum Laevomycetinum Laevomycetini stearas Сhloramphenicoli stearas* Laevomycetini succinas solubile 2,2-Дихлор-N-[(1R,2R)-2-гидрокси-1-(гидроксиметил)-2-(4-нитрофенил)этил] ацетамид или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропан-1,3-диола. D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропанди-ола-1,3-3-стеарат D(-)-трео-1-п-нитрофе-нил-2-дихлорацетамино-пропанди-ола-1,3-3-сукци-нат
- 13. Сhloramphenicoli palmitas* D(-)-трео-2,2-дихлор-N-[(3-гидрокси-α-(гидроксиметил)-п-нитрофенил] ацетамида α-пальмитат или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропандиола-1,3-3-пальмитат.
- 14. Левомицетин (Laevomycetinum, Хлорамфеникол, Сhloramphenicolum, ) 2,2-Дихлор-N-[(1R,2R)-2-гидрокси-1-(гидроксиметил)-2-(4-нитрофенил)этил] ацетамид или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропан-1,3-диола.
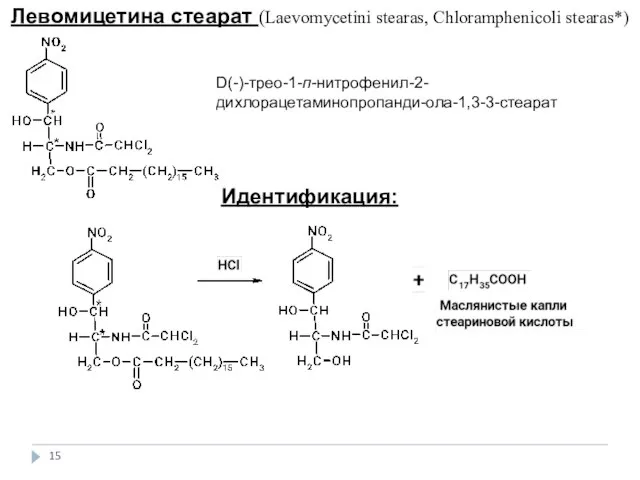
- 15. Левомицетина стеарат (Laevomycetini stearas, Сhloramphenicoli stearas*) D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропанди-ола-1,3-3-стеарат Идентификация:
- 16. Левомицетина пальмитат (Сhloramphenicoli palmitas*) D(-)-трео-2,2-дихлор-N-[(3-гидрокси-α-(гидроксиметил)-п-нитрофенил] ацетамида α-пальмитат или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропандиола-1,3-3-пальмитат.
- 18. Скачать презентацию




![Левомицетин Сhloramphenicolum Laevomycetinum Laevomycetini stearas Сhloramphenicoli stearas* Laevomycetini succinas solubile 2,2-Дихлор-N-[(1R,2R)-2-гидрокси-1-(гидроксиметил)-2-(4-нитрофенил)этил]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/598170/slide-11.jpg)
![Сhloramphenicoli palmitas* D(-)-трео-2,2-дихлор-N-[(3-гидрокси-α-(гидроксиметил)-п-нитрофенил] ацетамида α-пальмитат или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропандиола-1,3-3-пальмитат.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/598170/slide-12.jpg)
![Левомицетин (Laevomycetinum, Хлорамфеникол, Сhloramphenicolum, ) 2,2-Дихлор-N-[(1R,2R)-2-гидрокси-1-(гидроксиметил)-2-(4-нитрофенил)этил] ацетамид или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропан-1,3-диола.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/598170/slide-13.jpg)
![Левомицетина пальмитат (Сhloramphenicoli palmitas*) D(-)-трео-2,2-дихлор-N-[(3-гидрокси-α-(гидроксиметил)-п-нитрофенил] ацетамида α-пальмитат или D(-)-трео-1-п-нитрофенил-2-дихлорацетаминопропандиола-1,3-3-пальмитат.](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/598170/slide-15.jpg)
 Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4)
Коллигативные свойства растворов. Осмос. Осмотическое давление. (Лекция 4) Поверхностные явления
Поверхностные явления Биохимия и молекулярная биология. Биосинтез липидов. Лекция 8
Биохимия и молекулярная биология. Биосинтез липидов. Лекция 8 Спирти та етери. Медико-біологічне значення
Спирти та етери. Медико-біологічне значення Кислородсодержащие органические соединения. Сложные эфиры
Кислородсодержащие органические соединения. Сложные эфиры Минералогия и кристаллография
Минералогия и кристаллография Ферум. Залізо ПІДГОТУВАВ УЧЕНЬ 8-Б КЛАСУ
Ферум. Залізо ПІДГОТУВАВ УЧЕНЬ 8-Б КЛАСУ  Окислительно-восстановительные реакции (ОВР). ОВР с участием органических веществ. Окисление углеводородов
Окислительно-восстановительные реакции (ОВР). ОВР с участием органических веществ. Окисление углеводородов Медь, ее маркировка. Латуни. Бронзы
Медь, ее маркировка. Латуни. Бронзы Основной государственный экзамен. Химия 2021. Задание 7
Основной государственный экзамен. Химия 2021. Задание 7 Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства
Твердые растворы Zn1,92-2хMg0,08Mn2xSiO4 и Zn1,76-2хMg0,24Mn2xSiO4: синтез и спектроскопические свойства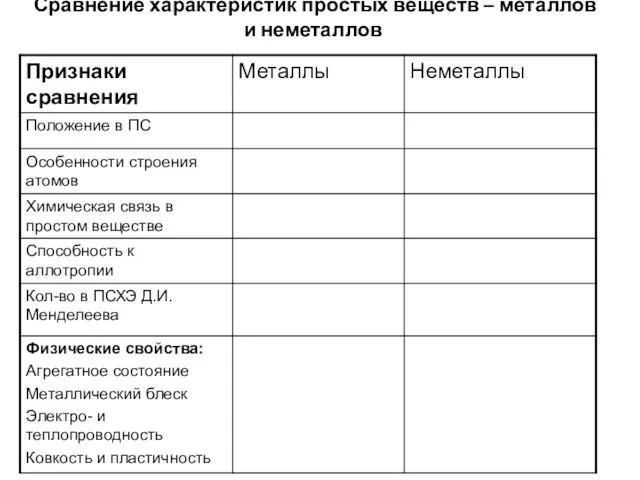 характеристика металлов и неметаллов
характеристика металлов и неметаллов Лекция 8. Стационарная кинетика (продолжение). Сложные ферментативные реакции
Лекция 8. Стационарная кинетика (продолжение). Сложные ферментативные реакции Генетическая связь между классами веществ
Генетическая связь между классами веществ Презентация по Химии "Физико-химические свойства алкинов" - скачать смотреть
Презентация по Химии "Физико-химические свойства алкинов" - скачать смотреть  Группы атомов водорода (12 групп)
Группы атомов водорода (12 групп) 1. Взаємодія неметалів з металами: 1. Взаємодія неметалів з металами: а) Сu0 + Cl20 = Сu+2 Cl2-1 – купрум (ІІ) хлорид Сu0 – 2e-→ Сu+2 2 Cl20 + 2(1e-) → Cl2−1 2 б) Fe0 + Cl20 = Fe+3 Cl3-1 – ферум
1. Взаємодія неметалів з металами: 1. Взаємодія неметалів з металами: а) Сu0 + Cl20 = Сu+2 Cl2-1 – купрум (ІІ) хлорид Сu0 – 2e-→ Сu+2 2 Cl20 + 2(1e-) → Cl2−1 2 б) Fe0 + Cl20 = Fe+3 Cl3-1 – ферум Водородная, ионная, донорно-акцепторная химические связи
Водородная, ионная, донорно-акцепторная химические связи Prezentatsia_2-10_Enoly
Prezentatsia_2-10_Enoly Алкены
Алкены Тонколистовой металл и проволока
Тонколистовой металл и проволока Производство сульфата аммония (лекция)
Производство сульфата аммония (лекция) Предмет химии. Вещества и их физические свойства. (8 класс)
Предмет химии. Вещества и их физические свойства. (8 класс) Курс «Химия» Цели изучения курса: дать современное представление о веществе как одной из форм материи. дать запас знаний по хим
Курс «Химия» Цели изучения курса: дать современное представление о веществе как одной из форм материи. дать запас знаний по хим Основные законы химии
Основные законы химии Насыпная плотность, методы определения, примеры
Насыпная плотность, методы определения, примеры Информационное письмо для студентов дистанционного обучения фармацевтического факультета по дисциплине Аналитическая химия
Информационное письмо для студентов дистанционного обучения фармацевтического факультета по дисциплине Аналитическая химия Полифункциональные соединения. Гетерофункциональные соединения. Структура и функции биолекул
Полифункциональные соединения. Гетерофункциональные соединения. Структура и функции биолекул