Содержание
- 2. История открытия Гамбургский алхимик Хеннинг Бранд - 1669 год «Фосфор» - от греческого «светоносный»
- 3. Строение атома фосфора. Положение в ПСХЭ. Р
- 4. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ Р БЕЛЫЙ КРАСНЫЙ ЧЕРНЫЙ
- 5. Молекулы P4 имеют форму тетраэдра. Это легкоплавкое t(пл)=44,1оС, t(кип)=275оС, мягкое, бесцветное воскообразное вещество. Хорошо растворяется в
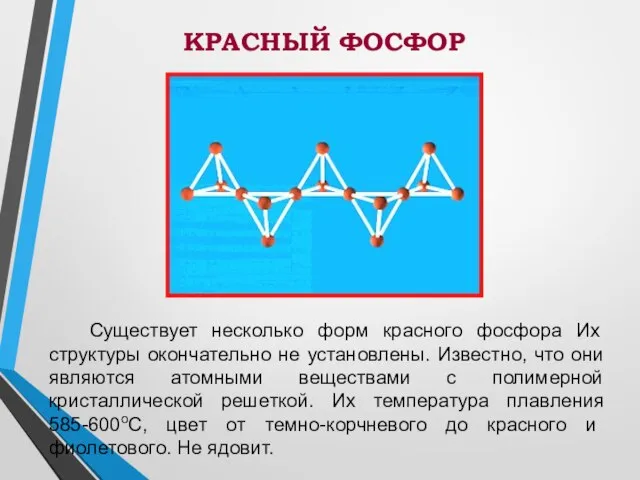
- 6. Существует несколько форм красного фосфора Их структуры окончательно не установлены. Известно, что они являются атомными веществами
- 7. Черный фосфор имеет слоистую атомную кристаллическую решетку. По внешнему виду похож на графит, но является полупроводником.
- 8. Р ОРГАНИЗМЫ МИНЕРАЛЫ ФОСФОЛИПИДЫ, ФЕРМЕНТЫ, ФОСФАТ КАЛЬЦИЯ ЭФИРЫ ОРТОФОСФОРНОЙ КИСЛОТЫ В ЗУБАХ И КОСТЯХ ФОСФОРИТ БИРЮЗА
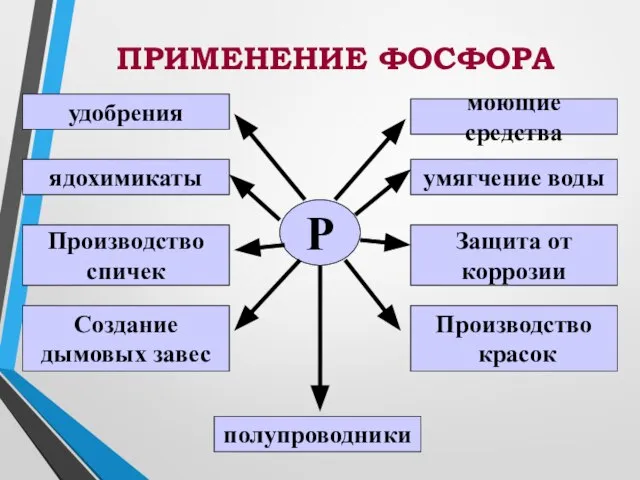
- 9. ПРИМЕНЕНИЕ ФОСФОРА Р удобрения ядохимикаты Производство спичек Создание дымовых завес полупроводники Производство красок Защита от коррозии
- 10. Войска США использовали фосфорные Бомбы в Ираке, 2004 г.
- 11. 1. металлами: Ca + P = 2. с неметаллами: P + O2 = P + S
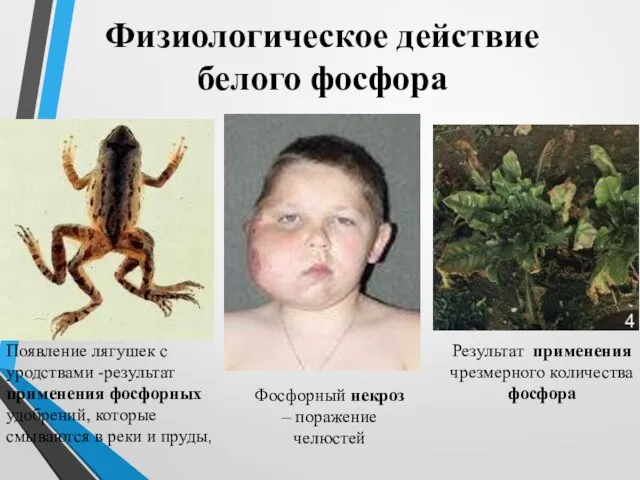
- 12. Результат применения чрезмерного количества фосфора Появление лягушек с уродствами -результат применения фосфорных удобрений, которые смываются в
- 13. 2. Задача: Какова масса фосфора в вашем теле, если известно, что фосфор составляет ≈1% от массы
- 15. Скачать презентацию









 Простые и сложные вещества. Металлы и неметаллы. Бинарные соединения
Простые и сложные вещества. Металлы и неметаллы. Бинарные соединения Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха
Понятие фазы вещества. Насыщенный пар и его свойства. Влажность воздуха. Приборы для измерения влажности воздуха Полимерные материалы
Полимерные материалы Презентация по Химии "Сміття 1" - скачать смотреть
Презентация по Химии "Сміття 1" - скачать смотреть  Химический состав свежих плодов и овощей
Химический состав свежих плодов и овощей Готовимся к контрольной работе по химии
Готовимся к контрольной работе по химии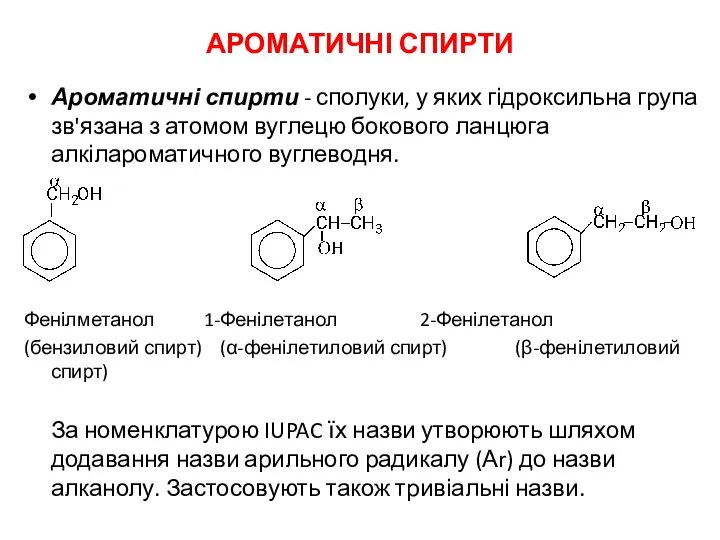 Ароматичні спирти
Ароматичні спирти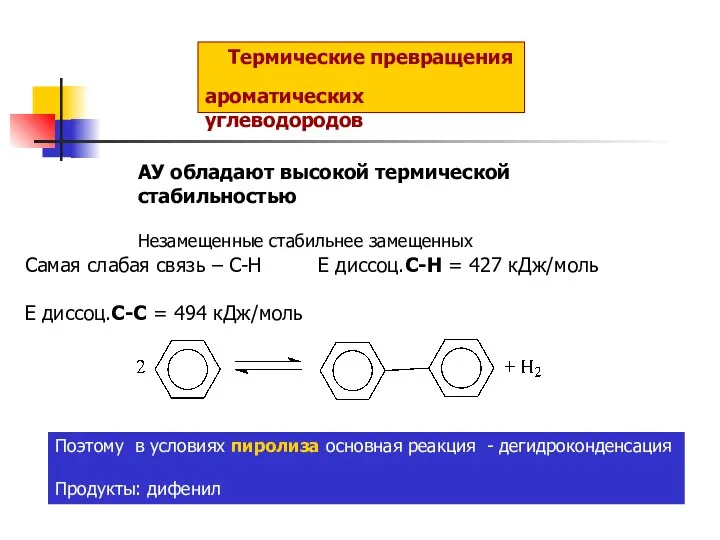 Термические превращения ароматических углеводородов
Термические превращения ароматических углеводородов Минералы натрия
Минералы натрия Алканы
Алканы Поверхностные явления. Лекция 15
Поверхностные явления. Лекция 15 Камни и Лев
Камни и Лев Гетерофункциональные органические соединения. Определение
Гетерофункциональные органические соединения. Определение Химическая посуда и ее значение (1)
Химическая посуда и ее значение (1) Материаловедение. Химические волокна (7 класс)
Материаловедение. Химические волокна (7 класс) Свойства растворов
Свойства растворов Аттестационная работа. Проектная и исследовательская деятельность как способ формирования химических знаний и умений
Аттестационная работа. Проектная и исследовательская деятельность как способ формирования химических знаний и умений Натуральный яблочный уксус
Натуральный яблочный уксус Губна помада та ії призначення
Губна помада та ії призначення Углерод. 9 класс
Углерод. 9 класс Электронная формула химических элементов
Электронная формула химических элементов Кислород. Характеристика и применение
Кислород. Характеристика и применение Строение соединений d-элементов
Строение соединений d-элементов Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі
Қалдық мөлшерлер. Бромды метил буының концентрациясын анықтау тәсілдемесі Обменные реакции в растворах электролитов
Обменные реакции в растворах электролитов Сложное вещество
Сложное вещество Cложные липиды (липоиды)
Cложные липиды (липоиды) Азот. Химические свойства азота
Азот. Химические свойства азота