Содержание
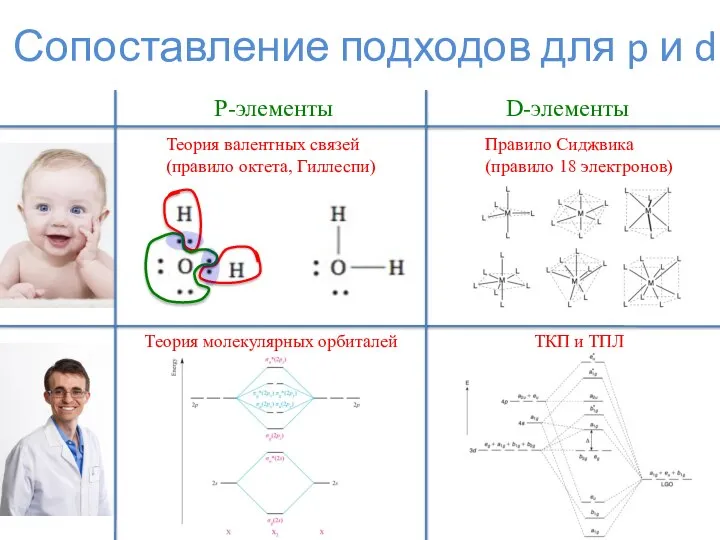
- 2. Сопоставление подходов для p и d P-элементы D-элементы Теория валентных связей (правило октета, Гиллеспи) Правило Сиджвика
- 3. Правило Сиджвика Комплексные соединения d-элементов в малых или отрицательных степенях окисления предпочитают лигандное окружение, обеспечивающее 18-электронное
- 4. Основные принципы Типы электронов в комплексных соединениях: Собственные электроны центральных атомов (d-металлов), не задействованные в связях
- 5. Характеристики лигандов 3) Формальный заряд – заряд лиганда в свободном состоянии 4) Мостиковость – количество атомов
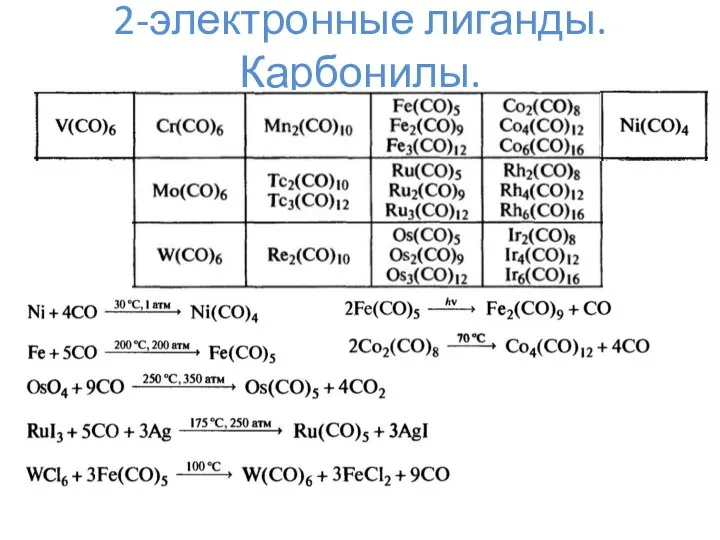
- 6. 2-электронные лиганды. Карбонилы.
- 7. 2-электронные лиганды. Карбонилы.
- 8. 2-электронные лиганды. Карбонилы. Mm(CO)n L = 2*n K = 18*m – L – N
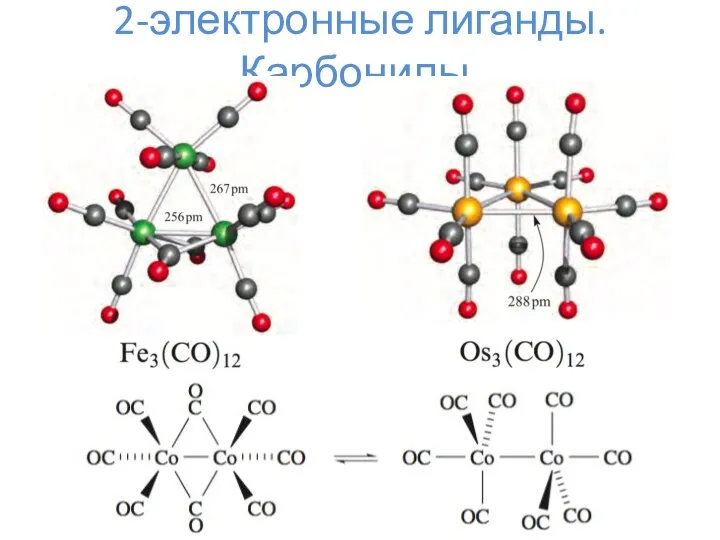
- 9. 2-электронные лиганды. Карбонилы.
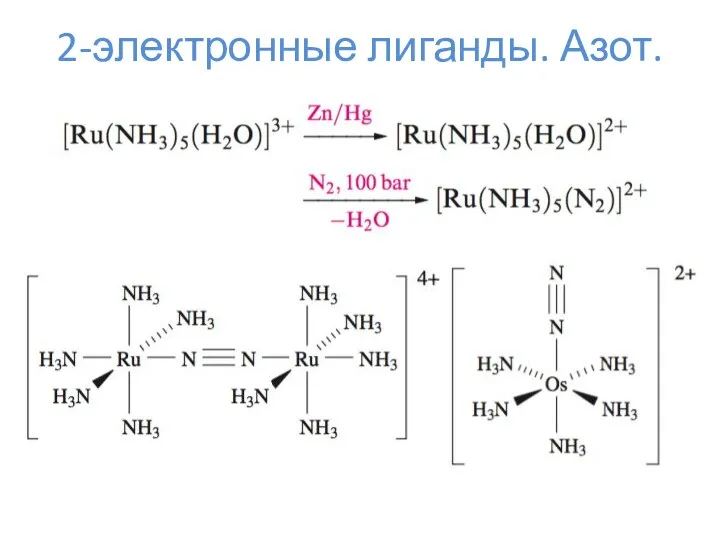
- 10. 2-электронные лиганды. Азот.
- 11. 2-электронные лиганды. Гидриды.
- 12. 2-электронные лиганды. Гидриды.
- 13. 2-электронные π-лиганды
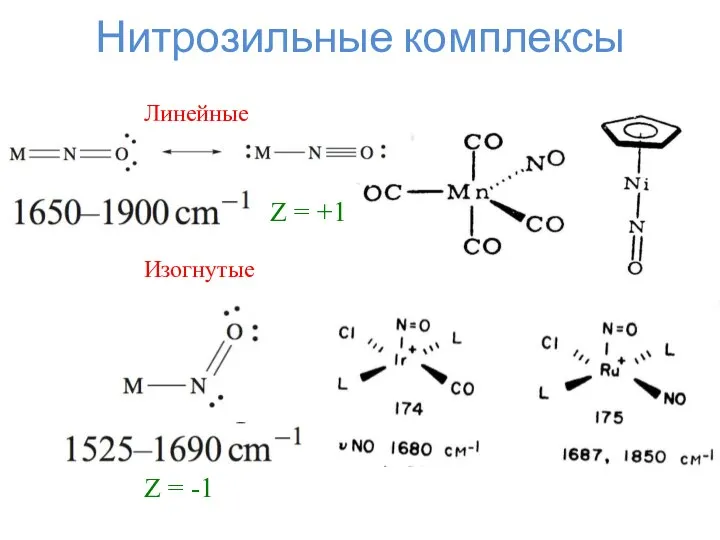
- 14. Нитрозильные комплексы Линейные Изогнутые Z = +1 Z = -1
- 15. 2-электронные π-лиганды 4-электронный аллильный лиганд Комплексы с конфигурацией d8 (если заряд металла положительный) - 16-электронные!!!
- 16. 6-электронный циклопентадиенид L = 6*n Z = (-1)*n FeCp2 N(Fe) = 8 + Z = 6
- 17. 6-электронный циклопентадиенид
- 18. 6-электронный бензол
- 19. 4-кратная связь!!!
- 20. 4-кратная связь!!!
- 21. Давайте посчитаем HRe3(CO)14 Mn2(CO)7(NO)3 [H2Re4(CO)12]2- [HCr2(CO)10]- MoCp2H2 [Fe(CN)5(NO)]2- [VCp(CO)4] [Co3(CO)10]-
- 22. Позволяет предсказать магнитные свойства (число неспаренных электронов) Позволяет оценить устойчивость комплекса и его реакционноспособность Позволяет сравнить
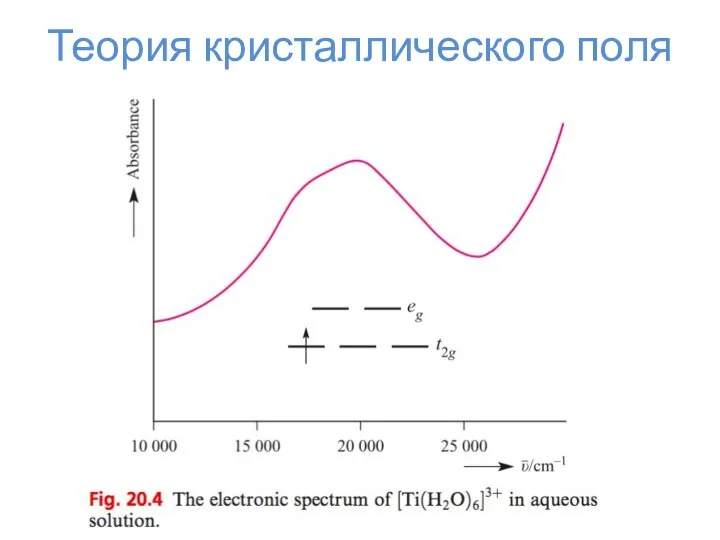
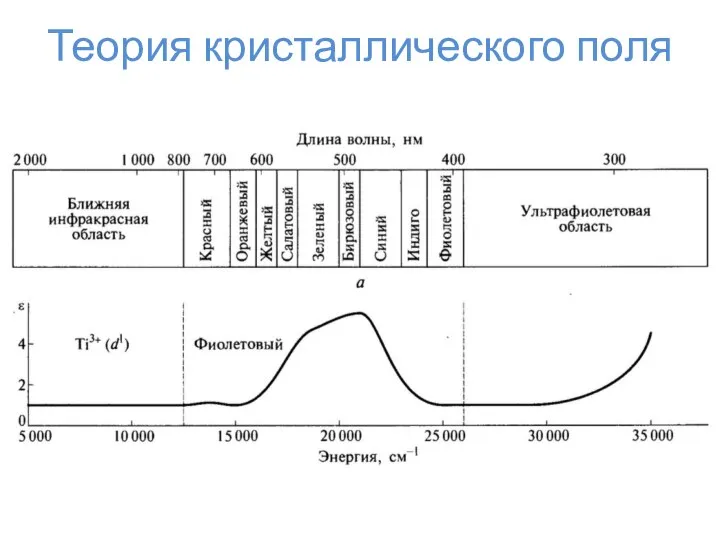
- 23. Теория кристаллического поля
- 24. Теория кристаллического поля Δо Энергия стабилизации кристаллическим полем ЭСКП = n*⅖Δо – m*⅗Δо – kP n
- 25. Теория кристаллического поля
- 26. Теория кристаллического поля
- 27. Теория кристаллического поля
- 28. Теория кристаллического поля
- 29. Теория кристаллического поля
- 30. Теория кристаллического поля
- 31. Теория кристаллического поля
- 32. Эффект Яна-Теллера d1, d4, d5 (сил. поле), d9, d6 (сл. поле), d7 (сл. поле) – искажение
- 33. Теория кристаллического поля d2, d7, d0, d10, d5 (слабое поле) – тетраэдр
- 35. Скачать презентацию














![Давайте посчитаем HRe3(CO)14 Mn2(CO)7(NO)3 [H2Re4(CO)12]2- [HCr2(CO)10]- MoCp2H2 [Fe(CN)5(NO)]2- [VCp(CO)4] [Co3(CO)10]-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1318674/slide-20.jpg)










 Вклад ученых Казахстана в развитие органической химии
Вклад ученых Казахстана в развитие органической химии Metals
Metals Классификация нефтей и нефтепродуктов
Классификация нефтей и нефтепродуктов Гидролиз солей
Гидролиз солей Презентация Химический состав мороженного
Презентация Химический состав мороженного Квантовая механика- теоретическая основа современной химии
Квантовая механика- теоретическая основа современной химии Названия алканов
Названия алканов Обмен веществ и энергии в клетке
Обмен веществ и энергии в клетке Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования
Методы исследования наносистем и наноматериалов. Классификация физико-химических методов исследования Железо, хром, марганец. Свойства, получение
Железо, хром, марганец. Свойства, получение Розв’язування задач і вправ з теми Алкани. 9 клас
Розв’язування задач і вправ з теми Алкани. 9 клас Алкалоиды природного происхождения
Алкалоиды природного происхождения II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra
II главная подгруппа ПС: Be, Mg, Ca, Sr, Ba, Ra Тема: «Алкины»
Тема: «Алкины»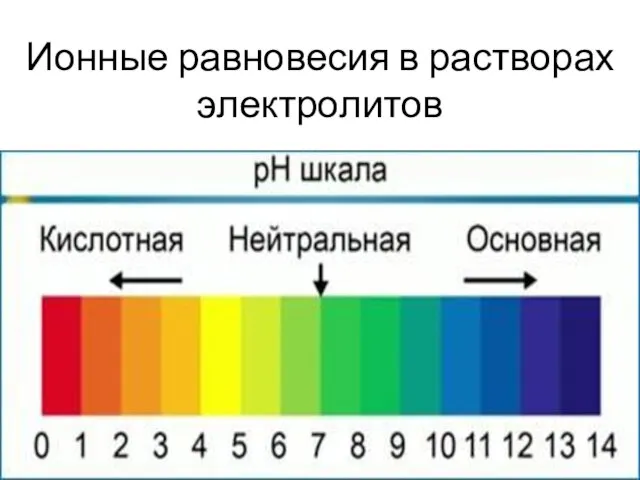 Ионные равновесия в растворах электролитов
Ионные равновесия в растворах электролитов Металлические стёкла (аморфные металлы)
Металлические стёкла (аморфные металлы) Алкины
Алкины Строение атома
Строение атома Презентация по Химии "Биохимия печени" - скачать смотреть
Презентация по Химии "Биохимия печени" - скачать смотреть  Нанохимия и нанотехнологии. Методы и средства исследования нанообъектов. (Лекция 3)
Нанохимия и нанотехнологии. Методы и средства исследования нанообъектов. (Лекция 3) Сера. Нахождение в природе. Химические свойства серы
Сера. Нахождение в природе. Химические свойства серы Anti-anxiety drugs
Anti-anxiety drugs Наноструктурные и нанокристаллические материалы
Наноструктурные и нанокристаллические материалы Серебро - химический элемент в периодической таблице с атомным номером 47. 8 класс
Серебро - химический элемент в периодической таблице с атомным номером 47. 8 класс Нефть и способы её переработки
Нефть и способы её переработки Именные реакции в органической химии
Именные реакции в органической химии Неоднородные системы (процессы и аппараты химической технологии, 8 лекция)
Неоднородные системы (процессы и аппараты химической технологии, 8 лекция) Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока
Вторичное квантование. Применение оболочечной модели. Метод Хартри - Фока