Содержание
- 2. Галогенидные комплексы постпереходных элементов -малая ширина запрещенной зоны -компоненты солнечных батарей Термохромизм Факторы: Природа катиона Соотношение
- 3. Максимальный интерес: компоненты солнечных батарей Первые работы – 2009 КПД около 20% Сравнительно дешевые Проблемы с
- 4. Цель: Изучение закономерностей образования галогенидных и полигалогенидных комплексов висмута и теллура и изучение их физико-химических свойств
- 5. 1. Иодовисмутаты: Синтез, структурная характеризация и оптические свойства
- 6. Реакции BiI3 с N-метилпиридинием иодистым А1 РФА, CHN, ИК, ШЗЗ = 1.78 эВ Выход: 52 %
- 7. BiI3 с N-этилпиридинием иодистым А3 РФА, CHN, ИК, ШЗЗ = 1.70 эВ Выход: 49 % А4
- 8. BiI3 с 1-метил-4-этилпиридинием А6 РФА, CHN, ИК, ШЗЗ = 2.06 эВ Выход: 58 % А5 РФА,
- 9. BiI3 с 1-MeDMAP А8 РФА, CHN, ИК, ШЗЗ = 1.97 эВ Выход: 52 % А7 РФА,
- 10. BiI3 с производными хинолина и изохинолина А10 РФА, CHN, ИК, ШЗЗ = 1.98 эВ Выход: 72
- 11. Иодовисмутаты c биядерными анионами А14 РФА, CHN, ИК, ШЗЗ = 2.11 эВ Выход: 53% А13 РФА,
- 12. Иодовисмутаты с дискретными анионами большей ядерности А18 РФА, CHN, ИК, ШЗЗ = 1.82 эВ Выход: 55
- 13. Иодовисмутат с анионом двухмерного строения А20 РФА, CHN, ИК, ШЗЗ = 1.84 эВ Выход: 50% *D.B.
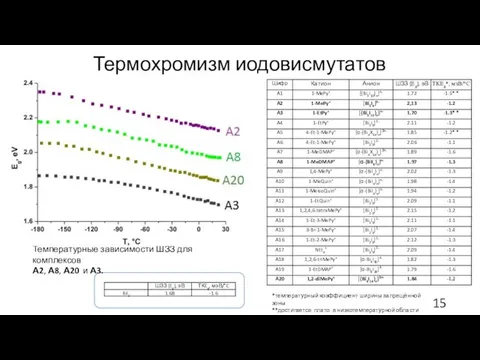
- 14. Оптические спектры иодовисмутатов Спектры диффузного отражения при комнатной температуре для A2 (1), A8 (2), A20 (3)
- 15. Термохромизм иодовисмутатов Температурные зависимости ШЗЗ для комплексов А2, А8, А20 и А3. *температурный коэффициент ширины запрещённой
- 16. 2. Галогенидные и полигалогенидные комплексы теллура: Синтез, структурная характеризация, термические стабильность и оптические свойства
- 17. Литературный обзор Hauge S. et al. //Acta Chem. Scand. 1998. Vol. 52. P. 445–449. Hauge S.
- 18. Полибромотеллураты TeO2 + Br2 + HBr + 2CatBr Rwdw(Br) = 1.83 Å Br-Br (Br2) = 2.33
- 19. Полибромотеллураты TeO2 + Br2 + HBr + 2CаtBr Br-Br (Br2) = 2.33 Å Brterm-Br = 3.10-3.11
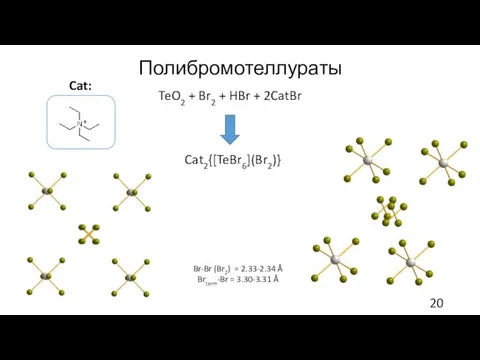
- 20. Полибромотеллураты TeO2 + Br2 + HBr + 2CatBr Br-Br (Br2) = 2.33-2.34 Å Brterm-Br = 3.30-3.31
- 21. Термическая стабильность полибромотеллуратов с производными пиридина Cat2{[TeBr6](Br2)} Тёмно-красный Cat2[TeBr6] Оранжевый -Br2 *A.N. Usoltsev, S. A. Adonin,
- 22. Термическая стабильность полибромотеллуратов с производными аммония Cat2{[TeBr6](Br2)} ω(Br2) = 15% Тпл(Te) = 449.6°C Cat:
- 23. Характеризация веществ состава: Сat2{[TeBr6](Br2)}
- 24. Полииодо-бромотеллураты I - I (I2) = 2.70-2.71 Å Brterm- I = 3.32-3.33 Å Te-Brterm-I = 159◦
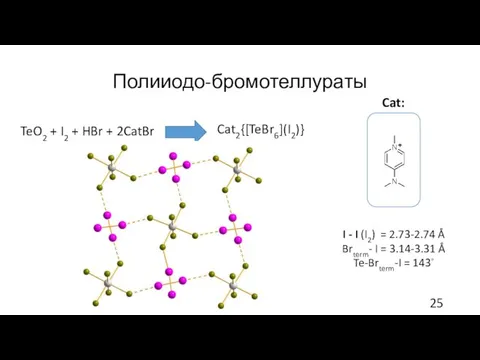
- 25. Полииодо-бромотеллураты I - I (I2) = 2.73-2.74 Å Brterm- I = 3.14-3.31 Å Te-Brterm-I = 143◦
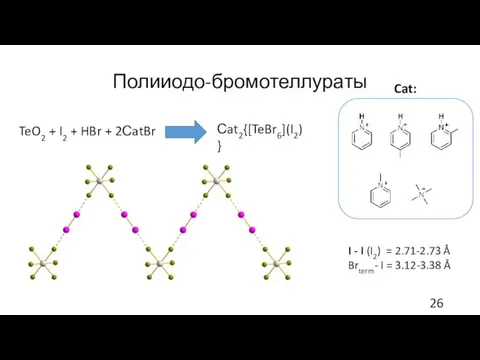
- 26. Полииодо-бромотеллураты I - I (I2) = 2.71-2.73 Å Brterm- I = 3.12-3.38 Å TeO2 + I2
- 27. Термическая стабильность полииодо-бромотеллуратов с производными пиридина Сat2{[TeBr6](I2)} ω(I2) = 22.4 % Cat:
- 28. Термическая стабильность полииодо-бромотеллуратов с производными аммония Сat2{[TeBr6](I2)} Cat:
- 29. Характеризация веществ состава: Сat2{[TeBr6](I2)}
- 30. Бромидные комплексы теллура Cat2[TeBr6] E1-E16 TeO2 + X2 + HBr + 2CatBr Cat2{[TeBr6](X2)}
- 31. Оптические спектры бромотеллуратов Спектры диффузного отражения при комнатной температуре для Е2 (1), Е12 (2) и Е15
- 32. Термохромизм бромотеллуратов Температурная зависимость оптической ширины запрещенной зоны для образца Е2 *температурный коэффициент ширины запрещённой зоны
- 33. Выводы: 1) Разработаны методы синтеза серии новых иодовисмутатных комплексов с анионами различного строения, в том числе
- 34. Выводы: 3) Получено 7 полииодид-бромотеллуратных комплексов состава Сat2{[TeBr6](I2)}. Показано, что термическая стабильность полигалогенидных комплексов теллура при
- 35. Основное содержание диссертации изложено в следующих работах: 1) Usoltsev A.N., Adonin S.A., Novikov A.S., Samsonenko D.G.,
- 36. Благодарность! Работа была выполнена при поддержке Российского Научного Фонда (грант № 14-23-00013 и № 18-73-10040)
- 37. Благодарность! Адонину С.А. (Науч. Рук.) Соколову М.Н. (Зав. Лаб.) Абрамову П.А. (РСА) Самсоненко Д.Г. (РСА) Плюснину
- 38. ФГБУН Институт элементоорганических соединений им. А.Н. Несмеянова РАН Доктор химических наук, Перекалин Дмитрий Сергеевич 1) Одной
- 39. Кандидат химических наук, научный сотрудник Николаевский Станислав Александрович ФГБУН Институт общей и неорганической химии им. Н.С.
- 40. Кандидат химических наук, научный сотрудник Николаевский Станислав Александрович ФГБУН Институт общей и неорганической химии им. Н.С.
- 41. Доктор химических наук, профессор, заведующий кафедрой неорганической химии МГУ Шевельков Андрей Владимирович ФГБОУ ВО «Московский государственный
- 42. Отзывы на автореферат без замечаний поступили от: 1) Ассистента института химии Санкт-Петербургский государственный университет, к.х.н. Иванова
- 43. Отзыв на автореферат с замечаниям поступил от: Профессора кафедры физической органической химии Инстутута химии ФГБОУВО «Санкт-Петербургский
- 44. Галогенидные комплексы висмута и теллура как компоненты солнечных батарей. Галогенидный комплекс выступает в роли поглотителя света
- 45. Причины термохромизма: 1 2 Изменение фононных колебаний решетки Термическое расширение кристаллической решетки
- 46. Коэффициент термической зависимости ШЗЗ для различных полупроводников
- 47. Галогеновая связь В соответствии с определением ИЮПАК, ГС представляет собой контакт R–X•••Y (X = галоген), для
- 48. Полупроводники Полупроводники отличаются от проводников сильной зависимостью проводимости от концентрации примесей, температуры и др.
- 49. Иодотеллураты TeО2 + HI + 2CatI + CH3CN Cat2[TeI6]
- 50. Иодотеллураты 3TeО2 + HI +4CatI + CH3CN Cat4[TeI6][Te2I10] {TeI6} Te-I 2.942-2.945 {Te2I10} Te-Iэкв 2.802-2.815 Å Te-Iакс
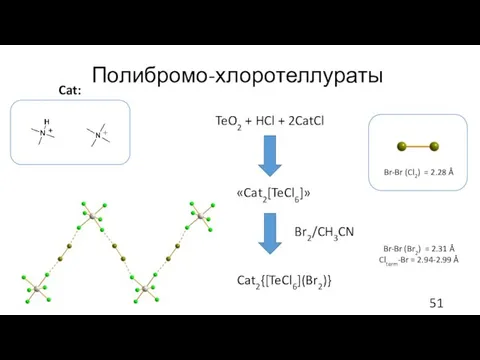
- 51. Полибромо-хлоротеллураты TeO2 + HCl + 2CatCl Br-Br (Br2) = 2.31 Å Clterm-Br = 2.94-2.99 Å Br-Br
- 52. Кристаллическая структура Cs3Bi2I9 была первоначально изучена в 1960-х годах. Почти 50 лет спустя, Парк и др.
- 53. Иодовисмутат с анионом двухмерного строения * D.B. Mitzi et al. // Inorg. Chem. 2000. Vol. 39,
- 54. Спектры КР для веществ состава Сat2{[TeBr6](Br2)} для В7(1), В3(2) и В4(3)
- 55. Спектр диффузного отражения и определение Eg в координатах Таука для соединения состава Сat2{[TeBr6](I2)} (С4) E –
- 57. Скачать презентацию

















} Тёмно-красный Cat2[TeBr6] Оранжевый -Br2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-20.jpg)
} ω(Br2) = 15% Тпл(Te) = 449.6°C Cat:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-21.jpg)
}](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-22.jpg)

} ω(I2) = 22.4 % Cat:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-26.jpg)
} Cat:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-27.jpg)
}](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-28.jpg)
![Бромидные комплексы теллура Cat2[TeBr6] E1-E16 TeO2 + X2 + HBr + 2CatBr Cat2{[TeBr6](X2)}](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-29.jpg)



}. Показано, что термическая](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-33.jpg)














![Иодотеллураты TeО2 + HI + 2CatI + CH3CN Cat2[TeI6]](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-48.jpg)
![Иодотеллураты 3TeО2 + HI +4CatI + CH3CN Cat4[TeI6][Te2I10] {TeI6} Te-I 2.942-2.945](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-49.jpg)


} для В7(1), В3(2) и В4(3)](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/603450/slide-53.jpg)
 Насыщенные углеводороды
Насыщенные углеводороды Нәруыз. Қасиеті және қызметі
Нәруыз. Қасиеті және қызметі Основы теории смазывания и стандарты качества моторных масел
Основы теории смазывания и стандарты качества моторных масел Химические источники тока
Химические источники тока Живые системы для производства углеводородов
Живые системы для производства углеводородов Презентация ОБЩАЯ ЖЕСТКОСТЬ ВОДЫ
Презентация ОБЩАЯ ЖЕСТКОСТЬ ВОДЫ  Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте
Массасы 4,2 г көміртек (IV) оксиді сумен әрекеттескенде қанша грамм көмір қышқылы (Н2СО3) түзілетінін есепте Нафта
Нафта  Point defects. Line defects. Surface Imperfections
Point defects. Line defects. Surface Imperfections Кристаллохимия как наука
Кристаллохимия как наука Кыргызстандагы химия онор жайы
Кыргызстандагы химия онор жайы Химическая связь. Природа химической связи
Химическая связь. Природа химической связи Nucleic acids
Nucleic acids Электролиз воды
Электролиз воды «Голубое золото» 10 класс базовый уровень
«Голубое золото» 10 класс базовый уровень  Схема катаболизма углеродного скилета аминокислот
Схема катаболизма углеродного скилета аминокислот Глицерин
Глицерин Природные источники углеводородов и их переработка
Природные источники углеводородов и их переработка Введение в биохимию. Строение и функции белков (часть 1)
Введение в биохимию. Строение и функции белков (часть 1) Химия и сельское хозяйство
Химия и сельское хозяйство Физические свойства металлов. Сплавы
Физические свойства металлов. Сплавы Презентация по химии Электролитическая диссоциация
Презентация по химии Электролитическая диссоциация  Հիալուրոնաթթվի անջատումը ձվի կեղևից և դրա նույնականացումը բարձրարդյունավետ. Հեղուկային քրոմատոգրաֆիայի եղանակով
Հիալուրոնաթթվի անջատումը ձվի կեղևից և դրա նույնականացումը բարձրարդյունավետ. Հեղուկային քրոմատոգրաֆիայի եղանակով Стеклянные товары. Основные сырьевые материалы для производства стекла
Стеклянные товары. Основные сырьевые материалы для производства стекла Презентация по Химии "Характеристика химического элемента – неметалла на основании его положения в Периодической системе хими
Презентация по Химии "Характеристика химического элемента – неметалла на основании его положения в Периодической системе хими Может ли вода приносить вред здоровью? Авторы: Козлова Ирина Владимировна, Ушакова Кристина Николаевна, 9 класс МОУ «СОШ №12», г. А
Может ли вода приносить вред здоровью? Авторы: Козлова Ирина Владимировна, Ушакова Кристина Николаевна, 9 класс МОУ «СОШ №12», г. А Строение полимера. Мономерное звено. Урок № 27
Строение полимера. Мономерное звено. Урок № 27 Ксенобиотики. Микросомальное окисление
Ксенобиотики. Микросомальное окисление