Содержание
- 2. План: История Положение в Периодической системе Химические свойства Применение
- 3. История: Фтор Фтор – это чрезвычайно химически активный неметалл и самый сильный окислитель, является самым лёгким
- 4. История: Хлор Впервые хлор был получен и описан К. Ш Однако ни сам Шееле, ни его
- 5. История Бром Впервые был получен Ю. Либихом, но он "проглядел" открытие, приняв бром за смесь хлора
- 6. История Йод Открыт в 1811 г. французским химиком-селитроваром Б. Куртуа. Согласно легенде, на заводе, где вырабатывалась
- 7. История Астат Предсказал(как «эка-иод») Д. И. Менделеев в 1869 Астат впервые получили искусственно Д. Корсон, К.
- 8. Положение в Периодичес-кой системе. Галогены находятся в VII группе главной подгруппе. К галогенам относятся: ФТОР-2 период
- 9. Химическая активность галогенов, как неметаллов, от фтора к Йоду ослабевает. Каждый галоген является самым сильным окислителем
- 10. 3. Отношение галогенов к сложным веществам. Фтор с водой реагирует так энергично, что происходит возгорание. Вода
- 11. Применение Фтор используют в производстве химически стойких пластмасс – Фторопластов Очень много его в чае, но
- 12. Применение Хлор применяют во многих отраслях промышленности, науки и бытовых нужд: Оконный профиль, изготовленный из хлорсодержащих
- 13. Применение Вещества на основе брома широко применяются в основном органическом синтезе. «Бромная вода» (водный раствор брома)
- 14. Применение Ученые выяснили, что астат, как и йод, накапливается в щитовидной железе. Но по силе действия
- 16. Скачать презентацию
План:
История
Положение в Периодической системе
Химические свойства
Применение
План:
История
Положение в Периодической системе
Химические свойства
Применение
История:
Фтор
Фтор – это чрезвычайно химически активный неметалл и самый сильный окислитель, является самым
История:
Фтор
Фтор – это чрезвычайно химически активный неметалл и самый сильный окислитель, является самым
О его существовании догадывались многие химики конца XVIII – начала XIX века. "Фторос" – разрушение, гибель (греч.). В 1771 г. Карл Шееле получил HF. Сам фтор был открыт в 1886 г. французским химиком А. Муассаном. Через 20 лет за открытие фтора А. Муассан получил Нобелевскую премию.
История:
Хлор
Впервые хлор был получен и описан К. Ш Однако ни сам
История:
Хлор
Впервые хлор был получен и описан К. Ш Однако ни сам
История
Бром
Впервые был получен Ю. Либихом, но он "проглядел" открытие, приняв бром
История
Бром
Впервые был получен Ю. Либихом, но он "проглядел" открытие, приняв бром
15 ноября 1825 г. исследователь отправил сообщение об открытии в Парижскую Академию наук, которое было заслушано 3 июля 1826 г. Комиссия, получив новое вещество согласно методам Балара и изучив его свойства, пришла к единодушному выводу, что бром является новым простым веществом. Комиссией было предложено для этого вещества другое название - бром (от греческого слова "бромос" - зловонный, дурно пахнущий).
История
Йод
Открыт в 1811 г. французским химиком-селитроваром Б. Куртуа.
Согласно легенде, на заводе,
История
Йод
Открыт в 1811 г. французским химиком-селитроваром Б. Куртуа. Согласно легенде, на заводе,
Куртуа заинтересовался этим явлением и внимательно стал изучать новое вещество. Новое вещество привлекло внимание двух знаменитых ученых – французского Ж.Л.Гей-Люссака и английского Г.Дэви, которые независимо друг от друга принялись изучать его свойства. Ученые пришли к выводу, что открытое Куртуа вещество новый элемент. Гей-Люссак назвал его йодом, а Дэви – йодином ("йоэйдэс" – "фиолетовый", древнегреч.).
История
Астат
Предсказал(как «эка-иод») Д. И. Менделеев в 1869 Астат впервые получили искусственно Д. Корсон, К. Макензи, Э. Сегре (см. СЕГРЕ Эмилио) в 1940. В 1943—46было установлено существование быстрораспадающихся изотопов астата в природе. году его существование и возможность открытия в
История
Астат
Предсказал(как «эка-иод») Д. И. Менделеев в 1869 Астат впервые получили искусственно Д. Корсон, К. Макензи, Э. Сегре (см. СЕГРЕ Эмилио) в 1940. В 1943—46было установлено существование быстрораспадающихся изотопов астата в природе. году его существование и возможность открытия в
Положение в Периодичес-кой системе.
Галогены находятся в VII группе главной подгруппе.
К галогенам
Положение в Периодичес-кой системе. Галогены находятся в VII группе главной подгруппе. К галогенам
Химическая активность галогенов, как неметаллов, от фтора к Йоду
ослабевает. Каждый галоген
Химическая активность галогенов, как неметаллов, от фтора к Йоду
ослабевает. Каждый галоген
периоде. Окислительные свойства галогенов отчетливо появляются при их
взаимодействии с металлами. При этом, как вы уже знаете, образуются соли. 1. Отношение галогенов к металлам.
Так, фтор уже при обычных условиях реагирует с большинством металлов,
а при нагревании – и с золотом, серебром, платиной, известными своей
химической пассивностью. Алюминий и цинк в атмосфере фтора
воспламеняются.
Zn + F2 = ZnF2 Остальные галогены реагируют с металлами в основном при нагревании.
2. Отношение галогенов к водороду.
С водородом соединяются все галогены, но при разных условиях.
H2 + F2 = 2HF реакция идет даже в темноте со взрывом.
H2 + CI2 = 2HCI реакция идет при горении спокойно, смесь на свету
реагирует со взрывом.
H2 + Br2 = 2HBr реакция идет при горении водорода в парах брома при
нагревании.
H2 + I2↔ 2HI реакция обратимая, идет при нагревании йода и горении
в его парах водорода.
3. Отношение галогенов к сложным веществам.
Фтор с водой реагирует так энергично,
3. Отношение галогенов к сложным веществам.
Фтор с водой реагирует так энергично,
2F2 + 2Н2О → 4HF + О
Хлор растворим в воде, при этом образуется хлорная вода, которая
обладает отбеливающим и обеззараживающими свойствами.
CI2 +H2O = 2HCI + O (атомарный кислород - сильный окислитель).
Здесь кислород выступает в непривычной для себя роли восстановителя.
Об уменьшении окислительных и увеличении восстановительных свойств
галогенов от фтора к иоду можно судить и по их способности вытеснять друг
друга из растворов солей. Так, хлор вытесняет бром и йод из растворов их
солей, например:
CI2 + 2KI = 2KCI + I2
4.Качественная реакция на галогенид-ион.
качественная реакция на йод – крахмал – синее окрашивание.
Высокая химическая активность – общее химическое свойство. Но от хлора к йоду активность падает. Фтор ещё активнее, чем хлор. Галоген с меньшим порядковым номером вытесняет любой галоген с большим порядковым номером из раствора соли, но не наоборот.
Применение
Фтор используют в производстве химически стойких пластмасс –
Фторопластов
Очень много его
Применение
Фтор используют в производстве химически стойких пластмасс –
Фторопластов
Очень много его
Сейчас ведутся активные кампании для запрета свободной продажи жевательных резинок и таблеток с фтором, а только лишь после рекомендаций лечащего врача и проведенных анализов.
Применение
Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:
Оконный
Применение
Хлор применяют во многих отраслях промышленности, науки и бытовых нужд:
Оконный
Основным компонентом отбеливателей является Лаббаракова вода.В производстве поливинилхлорида, пластикатов, синтетического каучука, из которых изготавливают: изоляцию для проводов, оконный профиль, упаковочные материалы, одежду и обувь, линолеум и грампластинки, лаки, аппаратуру и пенопласты, игрушки, детали приборов, строительные материалы. Поливинилхлорид производят полимеризацией винилхлорида, который сегодня чаще всего получают из этилена сбалансированным по хлору методом через промежуточный 1,2-дихлорэтан.
Отбеливающие свойства хлора известны с давних времен гексахлорциклогексан (часто называемый гексахлораном). Для обеззараживания воды — «хлорирования».
В пищевой промышленности зарегистрирован в качестве пищевой добавки E925.
В химическом производстве соляной кислоты, хлорной извести, бертолетовой соли, хлоридов металлов, ядов, лекарств, удобрений.
В металлургии для производства чистых металлов: титана, олова, тантала, ниобия.
Многие развитые страны стремятся ограничить использование хлора в быту, в том числе потому, что при сжигании хлорсодержащего мусора образуется значительное количество диоксинов.
Применение
Вещества на основе брома широко применяются в основном органическом синтезе.
«Бромная
Применение
Вещества на основе брома широко применяются в основном органическом синтезе.
«Бромная
Бромид серебра AgBr применяется в фотографии,как светочувствительное вещество.
Используется для создания антипиренов — добавок, придающих пожароустойчивость пластикам, древесине, текстильным материалам.
Пентафорид брома иногда используется как очень мощный окислитель ракетного топлива.
Растворы бромидов используются в нефтедобыче.
Растворы бромидов тяжёлых металлов используются как «тяжёлые жидкости» при обогащении полезных ископаемых методом флотации.
В медицине бромид натрия и бромид калия применяют как успокаивающие средства.
Со времен Первой мировой войны бром используется для производства боевых отравляющих веществ.
Применение
Ученые выяснили, что астат, как и йод, накапливается в щитовидной
Применение
Ученые выяснили, что астат, как и йод, накапливается в щитовидной













 Диены (диолефины, алкадиены)
Диены (диолефины, алкадиены) Конденсированные гетероциклические соединения. Пурины
Конденсированные гетероциклические соединения. Пурины Атомно – молекулярное учение
Атомно – молекулярное учение Получение меламина из карбамида
Получение меламина из карбамида Chemical equilibrium. (Chapter 3)
Chemical equilibrium. (Chapter 3) Понятие об адсорбционной влаге
Понятие об адсорбционной влаге Вспененные полимерные материалы. Классификация и принцип действия вспенивателей
Вспененные полимерные материалы. Классификация и принцип действия вспенивателей Презентация по Химии "Отбеливатели" - скачать смотреть
Презентация по Химии "Отбеливатели" - скачать смотреть  Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение
Монокристаллы CdTe и твердые растворы на его основе. Свойства, получение, применение Кислые породы умеренно-щелочного ряда
Кислые породы умеренно-щелочного ряда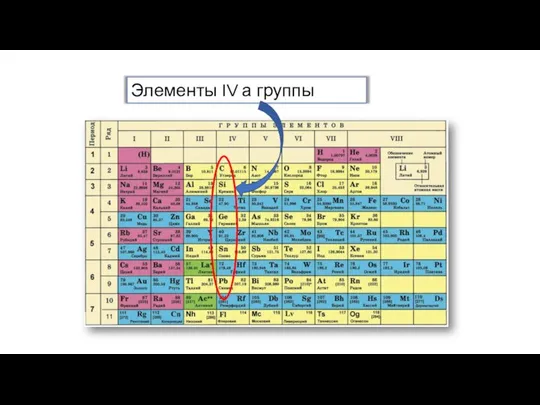 Углерод. Кремний
Углерод. Кремний Формальдегід. Будова та шкідливість
Формальдегід. Будова та шкідливість Мұнай. Мұнайдың шығу тарихы
Мұнай. Мұнайдың шығу тарихы Выделение урана из растворов (пульп)
Выделение урана из растворов (пульп) Средства и методы стерилизации
Средства и методы стерилизации Физические явления в химии. Чистые вещества и смеси
Физические явления в химии. Чистые вещества и смеси Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию ки
Кислоты, их состав и название. Цель урока: 1. Сформировать понятия о кислотах. 2. Рассмотреть состав, название и классификацию ки Кислотно-основное титрование
Кислотно-основное титрование ГБОУ СОШ № 1981
ГБОУ СОШ № 1981 Склеивание древесины. Клеи
Склеивание древесины. Клеи Методы термического обезвреживания промышленных газов
Методы термического обезвреживания промышленных газов Молярный объём
Молярный объём Применение метода кислотно-основного титрования в количественном анализе химических веществ и лекарственных средств. (Лекция 7)
Применение метода кислотно-основного титрования в количественном анализе химических веществ и лекарственных средств. (Лекция 7) Алканы. Гомологи, изомеры, номенклатура.
Алканы. Гомологи, изомеры, номенклатура.  Геохимические методы исследований
Геохимические методы исследований Сера и её соединения
Сера и её соединения Презентация по Химии "Хлор - физиологическая и патологическая роль в организме человека" - скачать смотреть бесплатно
Презентация по Химии "Хлор - физиологическая и патологическая роль в организме человека" - скачать смотреть бесплатно Кристаллооптический метод в петрографии
Кристаллооптический метод в петрографии