Содержание
- 2. Гидроксилпроизводные – это такие производные углеводородов, в состав молекулы которых входит одна или несколько гидроксильных групп.
- 3. Классификация В зависимости от количества гидроксильных групп различают: Одноатомные; Двухатомные; Трех- и многоатомные. В зависимости от
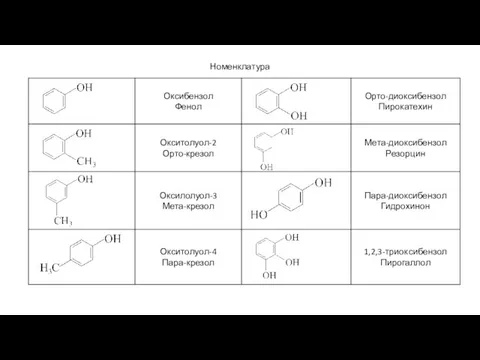
- 4. Номенклатура
- 5. классификация Таким образом получаем, что различают следующие группы гидроксилпроизводных: Насыщенные (предельные) одноатомные спирты Ненасыщенные одноатомные спирты
- 6. классификация Гидроксилпроизводные алкиларенов с гидроксильной группой в боковой цепи Дигидроксилпроизводные – двухатомные спирты (диолы)
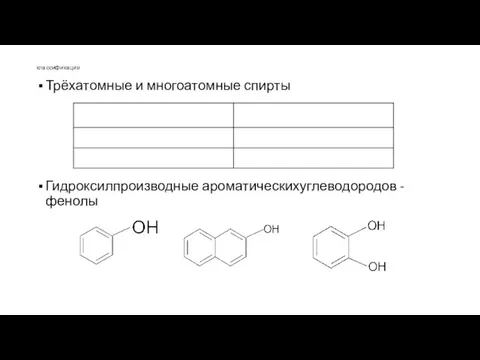
- 7. классификация Трёхатомные и многоатомные спирты Гидроксилпроизводные ароматическихуглеводородов - фенолы
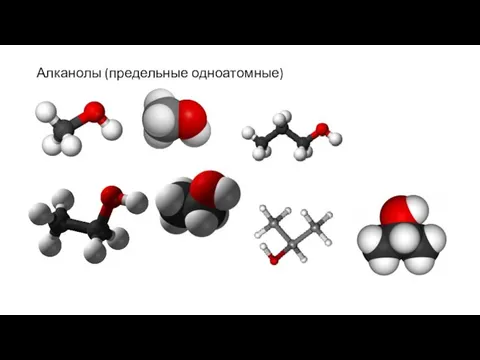
- 8. Алканолы (предельные одноатомные)
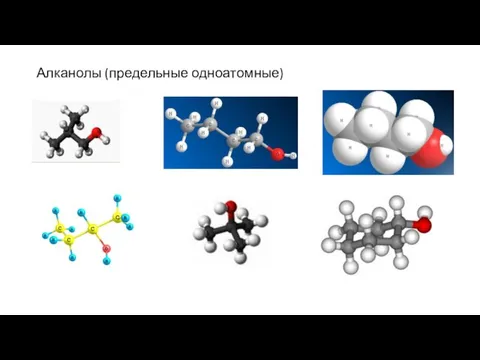
- 9. Алканолы (предельные одноатомные)
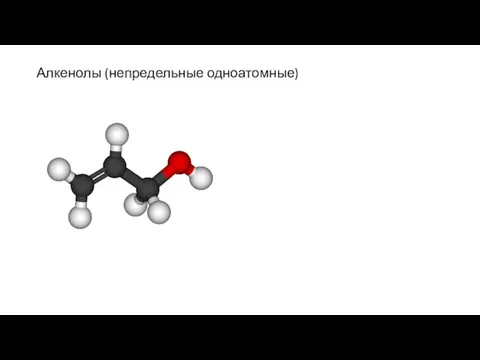
- 10. Алкенолы (непредельные одноатомные)
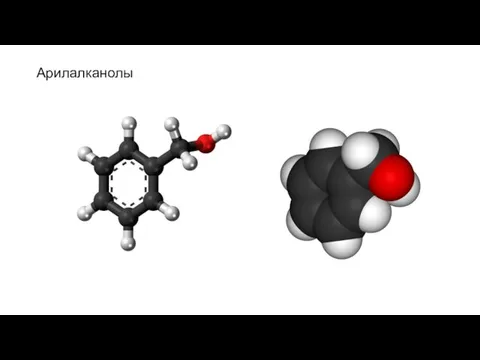
- 11. Арилалканолы
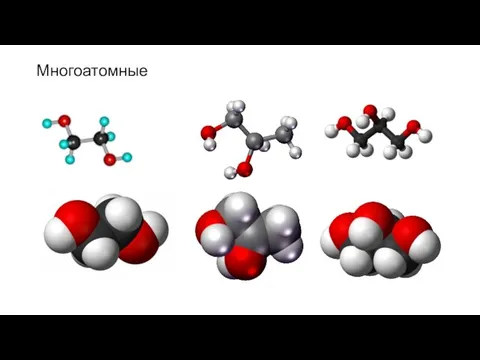
- 12. Многоатомные
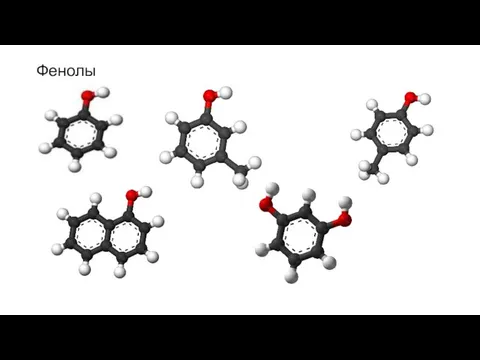
- 13. Фенолы
- 14. Спирты
- 15. Спирты - это производные углеводородов, содержащие одну или несколько гидроксильных групп (-O-H) R-OH
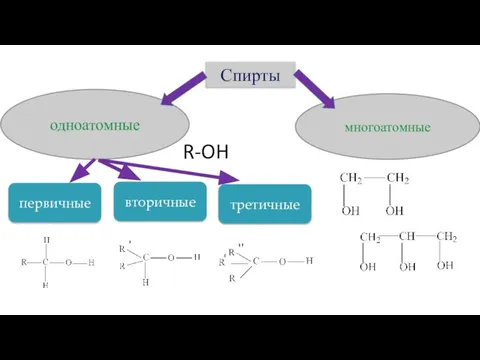
- 16. Классификация спиртов
- 17. третичные R-OH
- 18. Номенклатура спиртов
- 19. Название углеводородного радикала и окончание ОЛ CH3-OH метанол (метиловый спирт) CH3-CH2-OH этанол (этиловый спирт) CH3-CH2-CH2-OH пропанол-1
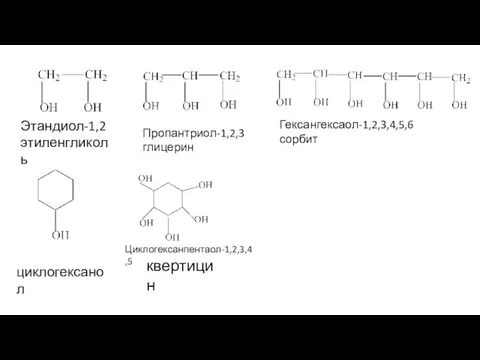
- 20. Этандиол-1,2 этиленгликоль Пропантриол-1,2,3 глицерин Гексангексаол-1,2,3,4,5,6 сорбит циклогексанол
- 21. Методы получения спиртов ЩЕЛОЧНОЙ ГИДРОЛИЗ ГАЛОГЕНУГЛЕВОДОРОДОВ: при нагревании с водными растворами щелочей Одноатомные спирты образуются из
- 22. Двухатомные спирты образуются из дигалогензамещенных углеводородов.
- 23. 2. Гидратация непредельных углеводородов При нагревании алкенов с водой в присутствии катализаторов (серная кислота, хлорид цинка
- 24. 2. Гидратация непредельных углеводородов При нагревании алкинов с водой в присутствии катализаторов (серная кислота, хлорид цинка
- 25. 3. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ Из монофункциональных альдегидов и кетонов образуются одноатомные спирты катализатор Ni (Pt,
- 26. 3. ВОССТАНОВЛЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ Из многофункциональных альдегидов и кетонов образуются многоатомные спирты (реакции идут при
- 27. 4. Синтез спиртов с помощью реактивов Гриньяра: Пропионовый альдегид метилмагнийиодид δ+ δ- δ- δ+ Алкоголят вторичный
- 28. Этанол получают из пищевого и непищевого органического сырья путем сбраживания: глюкоза ферменты
- 29. Гликоли получают окислением алкенов под действием водного раствора KMnO4
- 30. Получение смеси спиртов - синтола Условия: Нагревание, высокое давление, катализатор (Fe, Co) nCO +2nH2 → CnH2n+1OH
- 31. Кроме того многоатомные спирты получают по реакции Вагнера, гидроксилированием алкенов В качестве окислителей применяют перекись водорода
- 32. А так же многоатомные спирты получают из α-оксидов алкенов
- 33. Физические свойства спиртов Молекулы спиртов ассоциированы за счет образования межмолекулярных водородных связей: Низшие и средние предельные
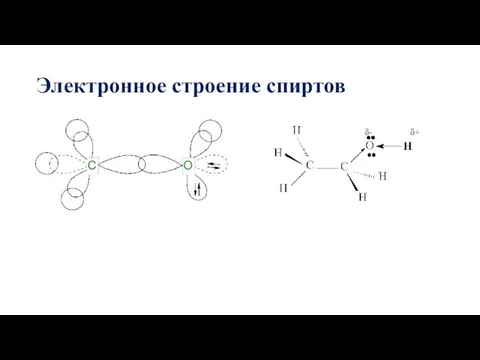
- 34. Электронное строение спиртов δ- δ+
- 35. Химические свойства спиртов Спирты очень слабые электролиты (слабее воды) CH3-CH2-O-H ↔CH3-CH2-O- + H+ Типы реакций Реакции
- 36. I. Реакции с участием водорода гидроксильной группы. 1. Замещение гидроксильного атома водорода на металл. (Na,Mg,Al) 2R-O-H
- 37. 2. Реакция этерификации – образование сложных эфиров
- 38. II. Реакции с отщеплением или замещением гидроксильной группы 1. Замещение гидроксила на галоген: CH3OH +PBr5 ↔
- 39. 2. Отщепление воды с образованием алкенов Условия: Нагревание с конц. H2SO4 или ZnCl2 (Al2O3)
- 40. 3. Межмолекулярная дегидратация Условия: нагревание избытка спирта с серной кислотой или пары спирта при 2000С через
- 41. 4. Замена гидроксила на аминогруппу Условия: 3000С, Al2O3 R-O-H + NH3 → R-NH2 + HOH спирт
- 42. III. Реакции окисления, в которых одновременно принимают участие гидроксильная группа, α-водородные атомы или соседние связи С-С
- 43. 1. Дегидрогенизация (отщепление водорода) Условие: пропускание паров спирта при 200 -3000С над мелкораздробленной медью или серебром
- 44. 2. Окисление Условия : сильные окислители (H2SO4 +KMnO4; H2SO4+ K2Cr2O7) Первичные спирты: Этанол этаналь (альдегид)
- 45. Вторичные спирты пропанол-2 пропанон-2 Вторичный спирт кетон
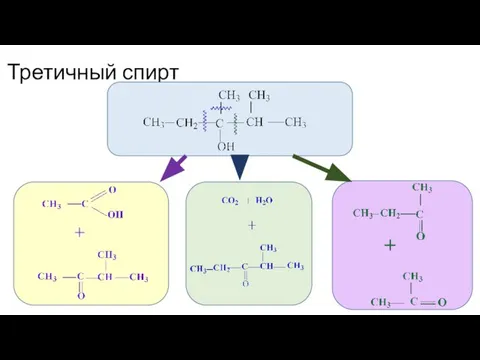
- 46. Третичный спирт
- 47. Многоатомные спирты Взаимодействие с металлами (Na, K, Mg, Al)
- 48. Многоатомные спирты Взаимодействие с гидроксидами металлов
- 49. Многоатомные спирты Взаимодействие с гидроксидами металлов При взаимодействии с гидроксидами d-металлов образуются комплексные соединения
- 50. Многоатомные спирты Взаимодействие с кислотами (реакция этерефикации) протекает ступенчато
- 51. Многоатомные спирты Замещение гидроксила на галоген
- 52. Дегидратация Межмолекулярная При нагревании со спиртами в присутствии сильных кислот (серной или ортофосфорной) Многоатомные спирты
- 53. Дегидратация Межмолекулярная При нагревании с сильными кислотами (серной или ортофосфорной) образуют циклические эфиры Многоатомные спирты
- 54. Дегидратация Внутримолекулярная В случае гликолей с изолированными гидроксогруппами (γ-гликоли и т.д.) происходит образование внутренних циклических эфиров
- 55. Дегидратация Внутримолекулярная В случае гликолей с изолированными гидроксогруппами (β-гликоли) происходит образование непредельных спиртов Многоатомные спирты
- 56. Дегидратация Особым образом происходит этот процесс в случае пинаконов (спиртов, в молекулах которых рядом находятся две
- 57. Окисление В общем виде окисление многоатомных спиртов на примере этиленгликоля может быть представлено следующим образом Многоатомные
- 58. Окисление Особым образом протекает окисление пинаколинов тетраацетатом свинца и периодатами Многоатомные спирты
- 59. Отдельные представители спиртов
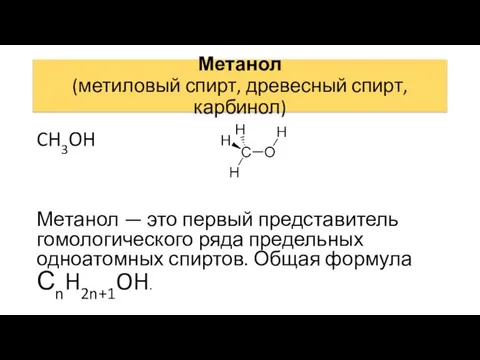
- 60. Метанол (метиловый спирт, древесный спирт, карбинол) CH3OH Метанол — это первый представитель гомологического ряда предельных одноатомных
- 61. Метанол -жидкость без цвета с температурой кипения 64 0С, с характерным запахом, легче воды, горит бесцветным
- 62. ПРИМЕНЕНИЕ метилового спирта
- 63. метанол Форм-альдегид (смолы) Уксусная кислота Изопрен Формалин Эфиры Растворитель в лакокрасочной промышленности Топливные элементы Добавка к
- 64. В газовой промышленности используется для борьбы с образованием гидратов. (При добыче газа гидраты могут образовываться в
- 65. Во многих странах метанол применяется в качестве добавки к этиловому спирту при производстве парфюмерии. В России
- 66. Метанол — опаснейший яд, приём внутрь 5—10 мл метанола приводит к тяжёлому отравлению и слепоте, а
- 67. Этиловый спирт (Этанол)
- 68. Этанол-бесцветная жидкость с характерным запахом и жгучим вкусом, температурой кипения78 0С. Легче воды. Смешивается с ней
- 69. Применение этанола
- 70. Химическая промышленность Ацет-альдегид диэтиловый эфир Тетраэтил-свинец уксусная кислота хлороформ этилацетат этилен
- 71. Растворитель В лакокрасочной промышленности, в производстве товаров бытовой химии (в чистящих и моющих средствах, в особенности
- 72. Парфюмерия и косметика Является универсальным растворителем различных веществ и основным компонентом духов, аэрозолей. Входит в состав
- 73. Этиловый спирт также используется как топливо. Применяется для консервирования биологических препаратов. Является наполнителем в спиртовых термометрах*.
- 74. В медицине антисептик; подсушивающие и дубящие свойства 96%-го этилового спирта используются для обработки операционного поля или
- 75. Пищевая промышленность Является основным компонентом спиртных напитков. В небольших количествах содержится в ряде напитков, получаемых брожением,
- 76. Этиловый спирт по своему действию на организм человека является: Депресантом – психоактивным веществом, угнетающим центральную нервную
- 77. Этиленгликоль Прозрачная бесцветная жидкость слегка маслянистой консистенции. Не имеет запаха и обладает сладковатым вкусом. Токсичен.
- 78. Применение Как компонент автомобильных антифризов и тормозных жидкостей. Смесь 60 % этиленгликоля и 40 % воды
- 79. В органическом синтезе для получения многих веществ и как высокотемпературный растворитель Как компонент жидкости «И», используемой
- 80. Этиленгликоль — горючее вещество. Температура вспышки паров 120 °C Этиленгликоль токсичен. По степени воздействия на организм
- 81. Глицерин трехатомный предельный спирт. Бесцветная, вязкая, гигроскопичная, сладкая (гликос — сладкий) на вкус жидкость. Смешивается с
- 82. Применяется в производстве взрывчатых веществ нитроглицерина. При обработке кожи. Как компонент некоторых клеев. При производстве пластмасс
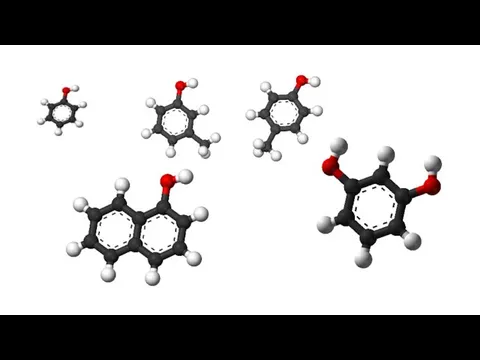
- 83. Гидроксилпроизводные ароматических углеводородов Фенолы
- 85. Номенклатура
- 86. Номенклатура
- 87. Номенклатура
- 88. Изомерия Положения гидроксильных групп Строения и положения заместителей Межклассовая изомерия
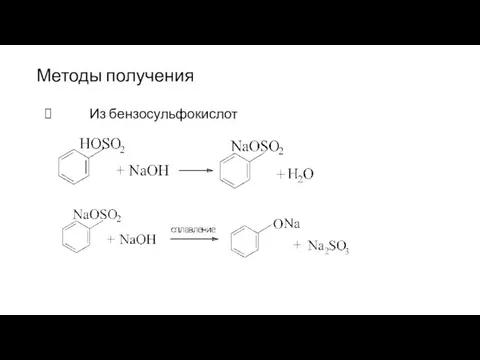
- 89. Методы получения Из бензосульфокислот
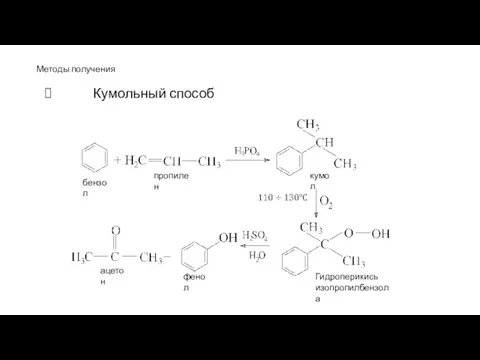
- 90. Методы получения Кумольный способ
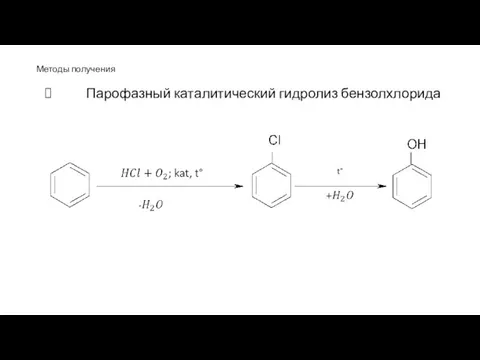
- 91. Методы получения Парофазный каталитический гидролиз бензолхлорида
- 92. Физические свойства и природа связей Фенолы при обычных условиях представляют собой жидкости или твёрдые вещества с
- 93. Химические свойства Кислотность и реакции с участием атома кислорода. Фенолы являются слабыми кислотами, но значительно более
- 94. Химические свойства. Кислотность и реакции с участием атома кислорода. Фенолы имеют очень характерную цветную реакцию: в
- 95. Химические свойства. Кислотность и реакции с участием атома кислорода. Алкилирование
- 96. Химические свойства. Кислотность и реакции с участием атома кислорода. Ацилирование
- 97. Химические свойства. Окисление.
- 98. Химические свойства. Реакции с электрофильными реагентами. Галогенирование.
- 99. Химические свойства. Реакции с электрофильными реагентами. Нитрование.
- 100. Химические свойства. Реакции с электрофильными реагентами. Сульфирование.
- 101. Химические свойства. Реакции с электрофильными реагентами. Ацилирование.
- 102. Химические свойства. Реакции с электрофильными реагентами. Алкилирование.
- 104. Скачать презентацию
















































































 Интерактивные игры. Химия
Интерактивные игры. Химия Нуклеиновые кислоты
Нуклеиновые кислоты Оптические свойства коллоидных квантовых точек
Оптические свойства коллоидных квантовых точек Кислоты
Кислоты Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ольга Викторовна
Учитель химии МБОУ СОШ № 9 МО ЩР станица Новощербиновская Степучева Ольга Викторовна Роль металлов в нашей жизни
Роль металлов в нашей жизни Перемешивание в жидких средах
Перемешивание в жидких средах Химическая коррозия
Химическая коррозия Липиды: функции и обмен
Липиды: функции и обмен Organic molecules
Organic molecules Сухой спирт
Сухой спирт Периодический закон и периодическая система Д. И. Менделеева
Периодический закон и периодическая система Д. И. Менделеева Знаменитый русский учёный Д. И. Менделеев
Знаменитый русский учёный Д. И. Менделеев Типы химических реакций
Типы химических реакций 9 класс (обязательный минимум по химии) ПОЛИМЕРЫ
9 класс (обязательный минимум по химии) ПОЛИМЕРЫ  Chem-квест. Химический диктант
Chem-квест. Химический диктант Невидимое сокровище
Невидимое сокровище Кислоты и соли
Кислоты и соли Гидролиз органических и неорганических соединений
Гидролиз органических и неорганических соединений Олово и свинец. (Лекция 2)
Олово и свинец. (Лекция 2) Карбоновые кислоты, сложные эфиры
Карбоновые кислоты, сложные эфиры Нанотехнологии в быту
Нанотехнологии в быту Эксперимент. Принципы теории планирования эксперимента. Классификация и виды экспериментов
Эксперимент. Принципы теории планирования эксперимента. Классификация и виды экспериментов Как сделать петуха из бумаги
Как сделать петуха из бумаги  Участь антиоксидантної системи saccharomyces cerevisiae у горметичному ефекті пероксиду водню
Участь антиоксидантної системи saccharomyces cerevisiae у горметичному ефекті пероксиду водню Химия и физика полимеров. Курс лекций
Химия и физика полимеров. Курс лекций Полимеры. Природные и синтетические полимеры
Полимеры. Природные и синтетические полимеры Эмульгаторы. Коллоиды. Гелеобразующие и увлажняющие вещества в косметическом производстве
Эмульгаторы. Коллоиды. Гелеобразующие и увлажняющие вещества в косметическом производстве