Содержание
- 2. Химические свойства металлов 1.1. Ме+Неме=>Соль, Оксиды, Перооксиды. Mg+Cl2=> MgCl2 4Na+O2=> 2Na2O 2Na+O2=> Na2O2 1.2. Ме+Н2О=>Основание +
- 3. 1.3. Ме+Соль=>Н. Ме+Н. Соль Металл вступающий в реакцию должен быть сильнее металла входящего в состав соли
- 4. Химические свойства неметаллов 2.1. Неме+Ме=>Соль (См.1.1) 2.2. Неме+Неме=> ….. Неметалл с большей электроотрицательностью проявляет кислотные свойства.
- 5. 2.5. Неме+Кислота=>Н.Неме+Н.Кислота Неметалл вступающий в реакцию должен быть сильнее неметалла входящего в состав кислоты Сl2+2HBr=>Br2+2HCl
- 6. Химические свойства оксидов металлов 3.1. MeO+H2O=>Щелочь С водой взаимодействуют те металлы которые образуют щелочь. СaО+H2O=>Са(ОН)2 3.2.
- 7. 3.4. Амф.МеО+Щелочь+H2O=Соль+H2 ZnO+2KOH+2H2O=K2[Zn(OH)4]+H2 ZnO+2KOH=K2ZnO2+H2O 3.5. Амф.МеО+Соль=Н.Соль+НемеО С оксидами амфотерных металлов могут взаимодействовать соли слабых кислородосодержащих кислот
- 8. Химические свойства оксидов неметаллов 4.1. НемеО+МеО=Соль (См.3.2) 4.2. НемеО+Н2О=Кислота SO3+H2O=H2SO4 4.3. НемеО+Основание=Соль+Н2О Cl2O3+2NaOH=2NaClO2+H2O 4.4. НемеО+Соль=Н.НемеО+Н.Соль Оксид
- 9. Химические свойства оснований 5.1. Щелочь+Амф.Мет+ Н20=Комплексная соль + Н2 (См. 1.5.) 5.2. Щелочь+ Немет=Соль 1+ Соль
- 10. 5.6. Основание+Соль=Н.Соль+Н.Основание Реагенты растворимы, продукт взаимодействия нерастворим либо газообразен 2NaOH+MgCl2=Mg(OH)2 + 2NaCl 5.7. Основание+Кислая соль=Средняя соль+Н2О
- 11. Химические свойства кислот 6.1. Кислота+Мет=Соль+Н2 (См.1.4.) 6.2. Кислота+Немет=Н.Кислота+Н.Немет (См. 2.5.) 6.3. Кислота+Ме.О=Соль+Н20 (См. 3.3) 6.4. Кислота+Основание=
- 13. Скачать презентацию





![3.4. Амф.МеО+Щелочь+H2O=Соль+H2 ZnO+2KOH+2H2O=K2[Zn(OH)4]+H2 ZnO+2KOH=K2ZnO2+H2O 3.5. Амф.МеО+Соль=Н.Соль+НемеО С оксидами амфотерных металлов могут](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/701942/slide-6.jpg)




 Основные классы неорганических соединений
Основные классы неорганических соединений Синтетика в нашому житті
Синтетика в нашому житті  Роль воды в жизнедеятельности организма. Теория растворов электролитов и неэлектролитов коллигативные свойства растворов
Роль воды в жизнедеятельности организма. Теория растворов электролитов и неэлектролитов коллигативные свойства растворов Рибосомы, генетический код, трансляция. (Лекция 7)
Рибосомы, генетический код, трансляция. (Лекция 7)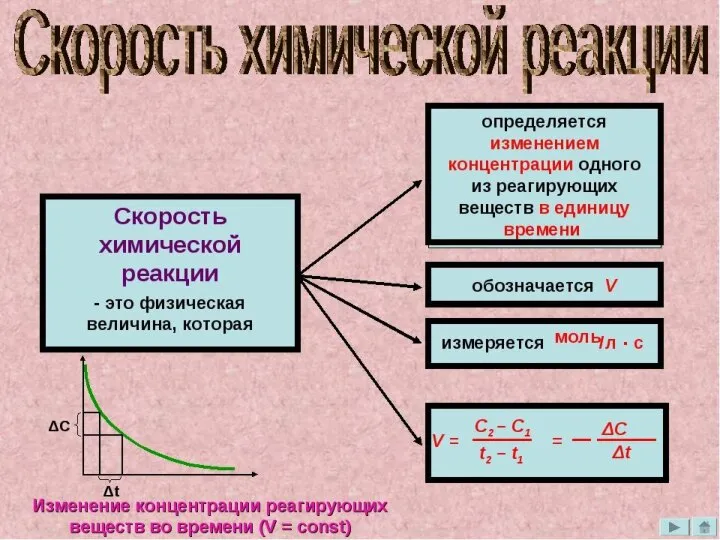 Скорость химичесой реакции и химическое равновесие
Скорость химичесой реакции и химическое равновесие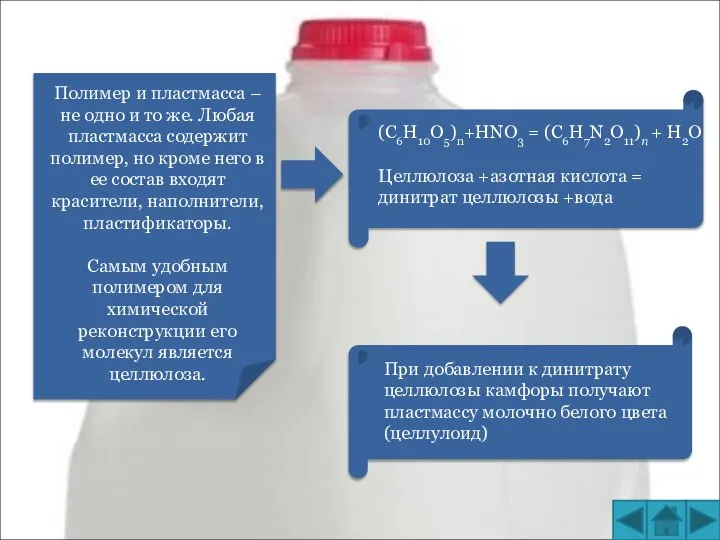 Полимер и пластмасса
Полимер и пластмасса Классификация химических элементов Й. Я. Берцелиус – выдающийся шведский ученый разделил все элементы на металлы и неметаллы.
Классификация химических элементов Й. Я. Берцелиус – выдающийся шведский ученый разделил все элементы на металлы и неметаллы. Гидролиз солей
Гидролиз солей Химия в судостроении
Химия в судостроении Сейсморазведка
Сейсморазведка Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія
Нітратна кислота. Нітрати Підготувала:Рибальчук Вікторія  Полимеры, их классификации и способы получения
Полимеры, их классификации и способы получения Термодинамика. Химическое равновесие. Кинетика
Термодинамика. Химическое равновесие. Кинетика Влияние давления на скорость химических реакций с участием газов
Влияние давления на скорость химических реакций с участием газов Композиционные материалы
Композиционные материалы Химиялық алғашқы ұғымдар тарауын қорытындылау
Химиялық алғашқы ұғымдар тарауын қорытындылау Теория химического строения органических соединений А.М. Бутлерова (ТХС)
Теория химического строения органических соединений А.М. Бутлерова (ТХС) Домашняя аптечка исследовательская работа Авторы: Полынникова Анастасия, Савина Мария учащиеся 9 «Б» класса Руководитель: Ма
Домашняя аптечка исследовательская работа Авторы: Полынникова Анастасия, Савина Мария учащиеся 9 «Б» класса Руководитель: Ма Эколого-химическая характеристика качества почвы
Эколого-химическая характеристика качества почвы Неньютоновская жидкость
Неньютоновская жидкость Щелочноземельные металлы
Щелочноземельные металлы Виконали: Алексеенко О.В. Перегонцева А.А.
Виконали: Алексеенко О.В. Перегонцева А.А.  Элементарные частицы вещества
Элементарные частицы вещества Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са
Відкриття радіоактивності. У 1896 р. французький учений Антуан Анрі Беккерель (1852-1908) відкрив радіоактивність солей Урану – явище са Химические свойства металлов
Химические свойства металлов Химические компоненты клетки. Неорганические компоненты
Химические компоненты клетки. Неорганические компоненты Образовательная программа дополнительного образования Химия в центре наук
Образовательная программа дополнительного образования Химия в центре наук Кафедра биохимии УГМУ в прошлом и настоящем. Локализация
Кафедра биохимии УГМУ в прошлом и настоящем. Локализация