Содержание
- 2. Цели урока: 1. Сформировать понятие обратимых процессов 2. Подвести к выводу о равенстве скоростей прямой и
- 3. Технологическая карта урока: - Вызов - Мозговой штурм - Составление кластера - Осмысление - Рефлексия -
- 4. Структура урока: Стадия "Вызов" Стадия "Осмысление" Стадия "Размышление"
- 5. Стадия «Вызов»
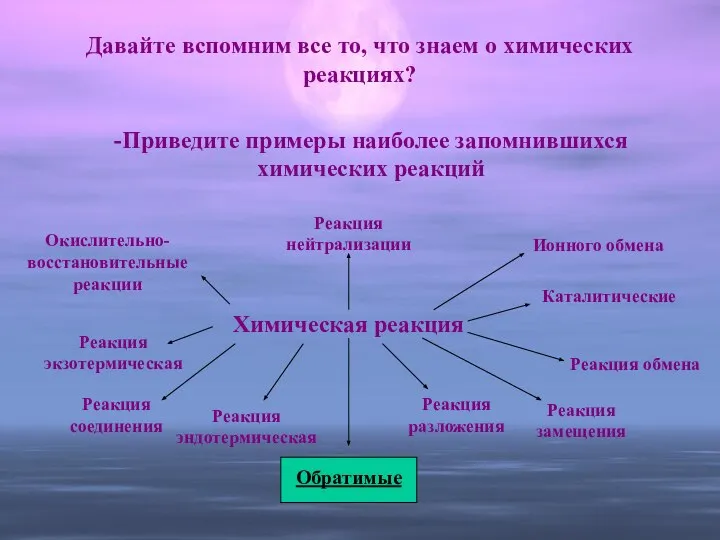
- 6. Давайте вспомним все то, что знаем о химических реакциях? -Приведите примеры наиболее запомнившихся химических реакций Химическая
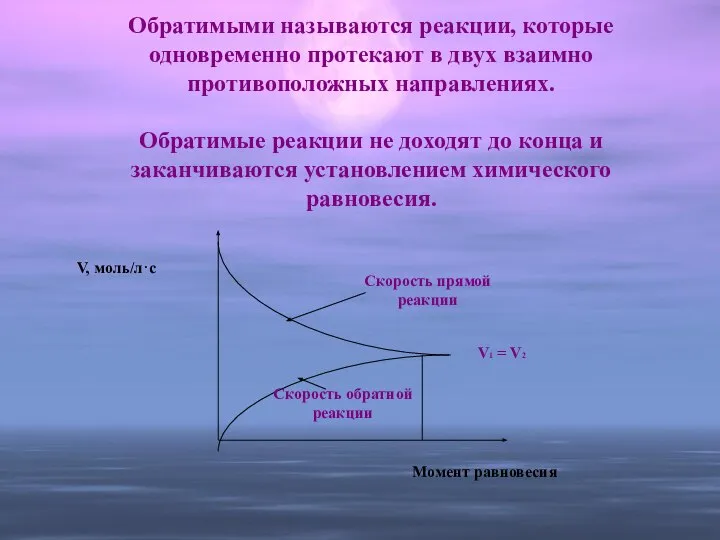
- 7. Обратимыми называются реакции, которые одновременно протекают в двух взаимно противоположных направлениях. Обратимые реакции не доходят до
- 8. Если вы правильно решите химический ребус, то получится название основного правила, которому подчиняются сдвиги химического равновесия.
- 9. Стадия «Осмысление»
- 10. Работа с информационным текcтом: I группа - § 19.2 стр. 81 II группа - § 19.2
- 11. Прочитайте текст. Цель: а) обогатить свои знания новой информацией. б) проверить, в чем мы правы, а
- 12. Читая текст, учащиеся делают пометки карандашом (метод «Инсерт») «?» - толстые и тонкие вопросы по ходу
- 13. Допустим, что химическая реакция представляет собой весы. На левой чаше весов находится исходные вещества, на правой
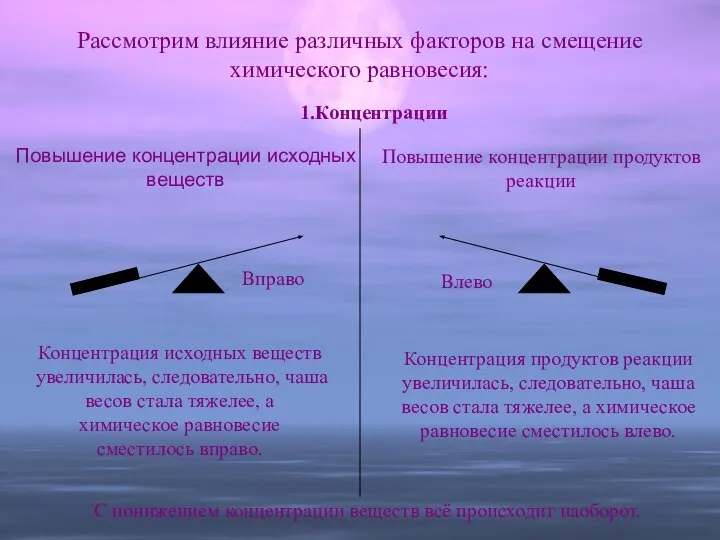
- 14. Рассмотрим влияние различных факторов на смещение химического равновесия: 1.Концентрации Повышение концентрации исходных веществ Вправо Концентрация исходных
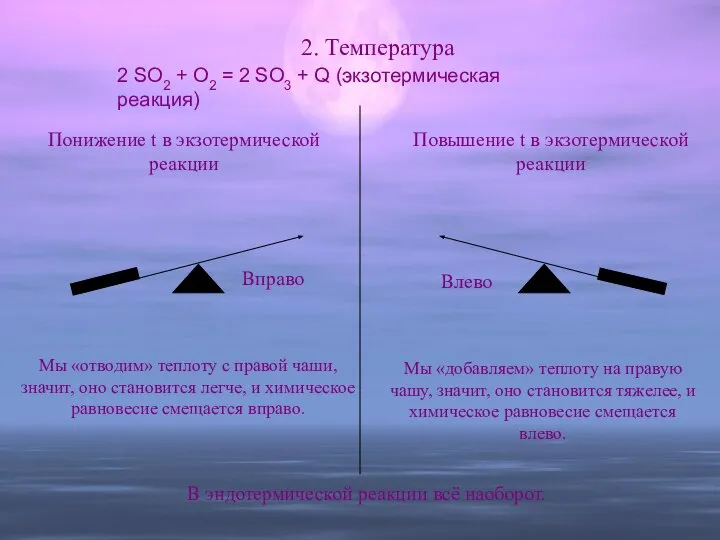
- 15. 2. Температура 2 SO2 + O2 = 2 SO3 + Q (экзотермическая реакция) Понижение t в
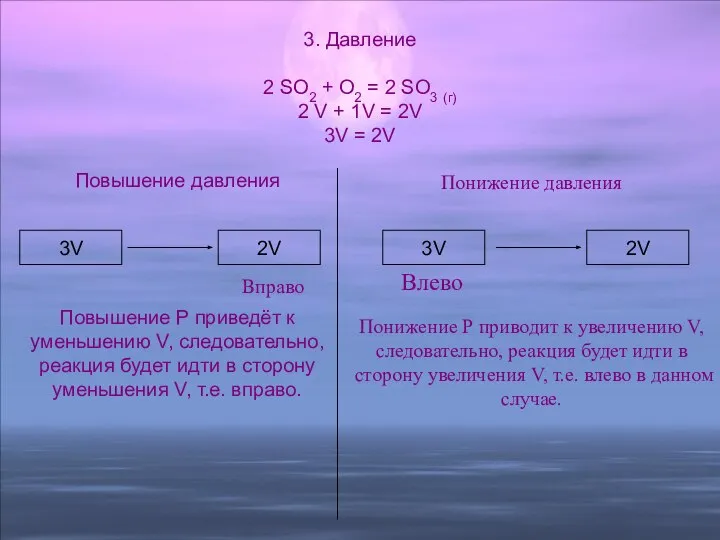
- 16. Понижение давления Понижение Р приводит к увеличению V, следовательно, реакция будет идти в сторону увеличения V,
- 17. Беседа с классом по вопросам: 1. Что из того, что вы прочитали, вам уже было знакомо?
- 18. Стадия «Размышление»
- 19. Химик толкает реакцию в спину: «Давай-ка тебя я немного подвину!» Она отвечает: «Ты знаешь меня: Ни
- 20. Самостоятельная работа I вариант Как сместится равновесие реакции: 2 NOг + O2 = 2 NO2 Г
- 21. Оценки за урок
- 23. Скачать презентацию














 Зародження періодичної системи елементів Менделєєва
Зародження періодичної системи елементів Менделєєва Презентация по Химии "Колообіг Оксигену, Нітрогену, Карбону в природі" - скачать смотреть бесплатно
Презентация по Химии "Колообіг Оксигену, Нітрогену, Карбону в природі" - скачать смотреть бесплатно Классификация топлива. Показатели качества топлива (Лекция 1)
Классификация топлива. Показатели качества топлива (Лекция 1) Состояние электронов в атоме
Состояние электронов в атоме Каменный уголь
Каменный уголь Металлы в природе, общие способы получения металлов
Металлы в природе, общие способы получения металлов Задачи на сплавы и смеси
Задачи на сплавы и смеси Laboratorní sklo a nářadí
Laboratorní sklo a nářadí Природні джерела вуглеводнів Підготувала: Савчук Ірина
Природні джерела вуглеводнів Підготувала: Савчук Ірина  Мыло. Синтетические моющие средства
Мыло. Синтетические моющие средства Алмази
Алмази  Тему «Соли». Нитрат серебра(I) AgNO3
Тему «Соли». Нитрат серебра(I) AgNO3 Хроматография. Физико-химические методы анализа биологических систем
Хроматография. Физико-химические методы анализа биологических систем Арены. Бензол
Арены. Бензол Классификация моторных масел
Классификация моторных масел Небезпечні хімічні речовини Підготувала: учениця 8 – А класу Кіровоградського НВК №34 Подколзіна Анна
Небезпечні хімічні речовини Підготувала: учениця 8 – А класу Кіровоградського НВК №34 Подколзіна Анна  Общая характеристика нефти и газа
Общая характеристика нефти и газа Chimie anorganica
Chimie anorganica Презентация по Химии "Шкода запаху гуми і її токсичність. Які хвороби характерні для працівників шинних заводів?" - скачать см
Презентация по Химии "Шкода запаху гуми і її токсичність. Які хвороби характерні для працівників шинних заводів?" - скачать см Тема урока: СЕРНАЯ КИСЛОТА И ЕЁ СВОЙСТВА
Тема урока: СЕРНАЯ КИСЛОТА И ЕЁ СВОЙСТВА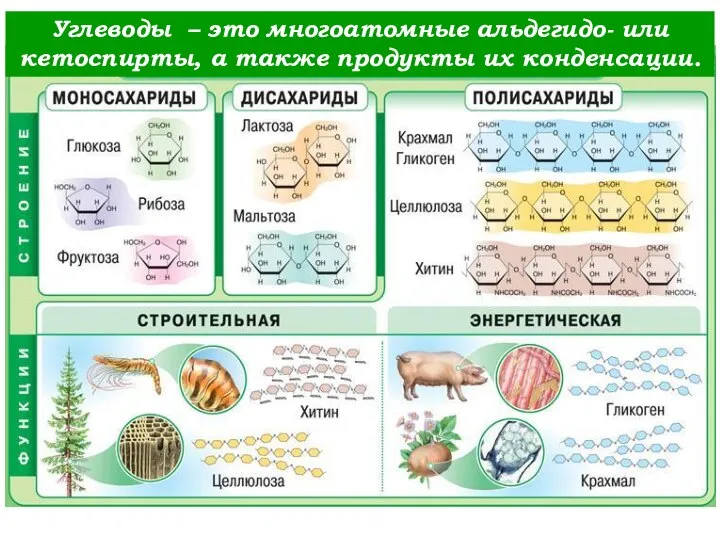 Углеводы. Классификация углеводов. Явление мутаротации. (Лекция 4)
Углеводы. Классификация углеводов. Явление мутаротации. (Лекция 4) Степень окисления
Степень окисления Кислород- история открытия, роль в природе
Кислород- история открытия, роль в природе Химия ғажайыптары
Химия ғажайыптары Бүйрек зәр түзе отырып, қаннан шығатын бөлінділерді сүзетін
Бүйрек зәр түзе отырып, қаннан шығатын бөлінділерді сүзетін Хроматографические методы анализа
Хроматографические методы анализа Биологически важные химические элементы. Неорганические соединения
Биологически важные химические элементы. Неорганические соединения Аттестационная работа. Программа элективного курса «Исследовательская проектная деятельность при изучении химии»
Аттестационная работа. Программа элективного курса «Исследовательская проектная деятельность при изучении химии»