Содержание
- 2. N2O – несолеобразующий NO – несолеобразующий N2O3 – кислый NO2 – несолеобразующий N2O5 – кислый Однако!
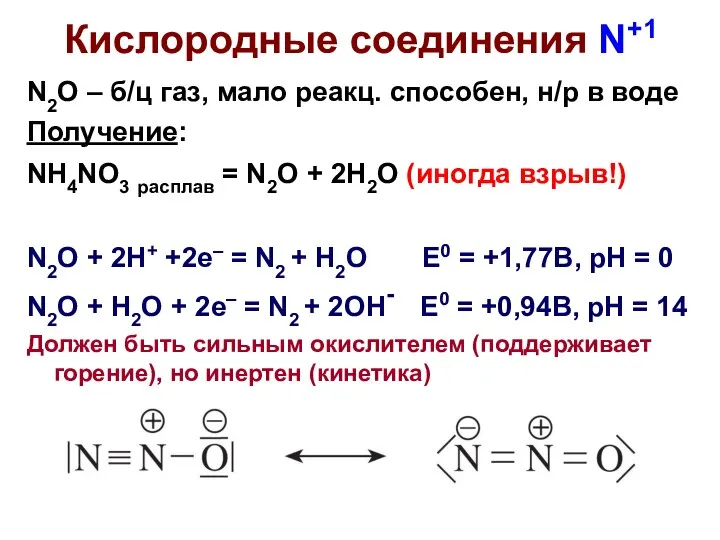
- 3. Кислородные соединения N+1 N2O – б/ц газ, мало реакц. способен, н/р в воде Получение: NH4NO3 расплав
- 4. Кислородные соединения N+2 NO – б/ц газ, реакц. способен, н/р в воде Получение: 3Cu + 8HNO3
- 5. ДВОЙСВЕННОСТЬ Ox-Red СВОЙСТВ: HNO2 – сильный (и быстрый) окислитель HNO2 + H+ + e– = NO
- 6. Кислородные соединения N+4 NO2 – бурый, реакционноспособный, газ, ядовит N2O4 – бесцветный, Тпл. = –11 оС
- 7. Кислородные соединения N+4 Диспропорционирование: 2NO2 + H2O = HNO3 + HNO2 (на холоду) 3NO2 + H2O
- 8. Кислородные соединения N+5 N2O5 – б/ц тв., неустойчив, [NO2]+[NO3]–, в газе O2N–O–NO2, сильный окислитель Получение оксида:
- 9. NO3– в нейтральной среде не обладает окислительными свойствами! NO3– + 2H2О + 3e– = NO +
- 10. Азотная кислота Производство: В XX веке и до… : 4NH3 + 5O2 (Pt) → 4NO +
- 11. Применение в производстве минеральных удобрений; в производстве красителей и лекарств (нитроглицерин) в военной промышленности (дымящая –
- 12. Азотная кислота Различные азотсодержащие продукты при взаимодействии азотной кислоты с различными веществами: увеличение концентрации кислоты увеличение
- 13. Азотная кислота Различные азотсодержащие продукты при взаимодействии азотной кислоты с различными веществами: увеличение концентрации кислоты увеличение
- 14. Почему азот в реакциях с разбавленной HNO3 восстанавливается «глубже», чем с концентрированной? NO + 2HNO3 ⮀
- 15. «Царская водка»: HNO3(к) + HCl(к) (1:3 по объему) 3HCl + HNO3 ⮀ NOCl + 2[Cl0] +
- 16. Разложение нитратов при T NH4NO3 = N2O + 2H2O NaNO3 = NaNO2 + 1/2O2 Щелочные и
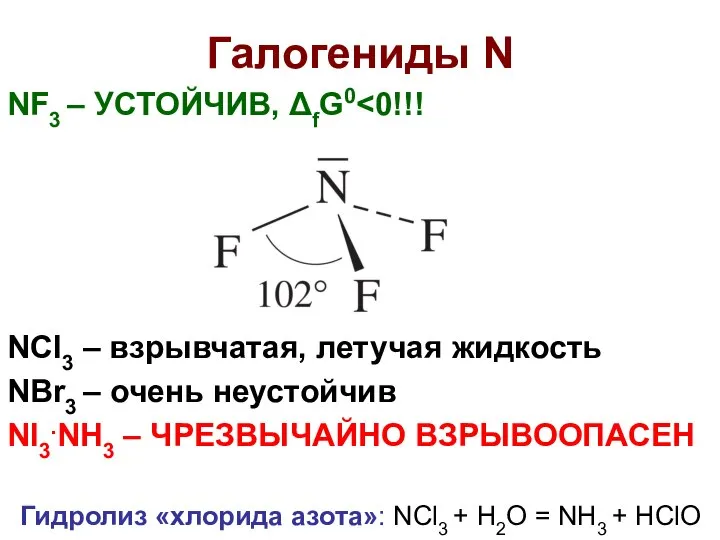
- 17. Галогениды N NF3 – УСТОЙЧИВ, ΔfG0 NCl3 – взрывчатая, летучая жидкость NBr3 – очень неустойчив NI3.NH3
- 18. N и P Химия N и P резко отличаются N в высших степенях окисления – сильные
- 19. Э = P, As, Sb, Bi Возрастание металлических свойств Увеличение окислительных свойств P5+ → Bi5+; соединения
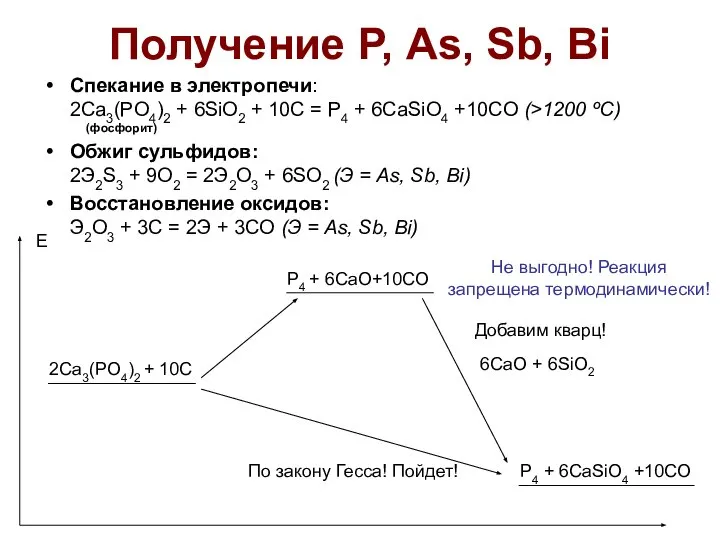
- 20. Получение Р, As, Sb, Bi Спекание в электропечи: 2Ca3(PO4)2 + 6SiO2 + 10C = P4 +
- 21. Свойства Р, As, Sb, Bi Реакции с кислородом: P образует P4O6 и P4O10, остальные Э2О3 (в
- 22. Реакции с кислотами окислителями: Э + 5HNO3 конц. = H3ЭO4 + 5NO2 + H2O (Э =
- 23. Соединения с водородом PH3 – фосфин, Получение через фосфиды – Ca3P2 2Э + 3Ca = Ca3Э2
- 24. Криминалистика As2O3 + 6Zn + 6H2SO4 = 6ZnSO4 + 2AsH3 + 3H2O “H” 2AsH3 = 3H2
- 28. Кислородные соединения Э+1 Известны кислота и соли только для Р H3PO2 – гипофосфористая (фосфорноватистая) к-та, одноосновная,
- 29. Кислородные соединения Э+1 Получение: 2P4 + 3Ba(OH)2 + 6H2O = 2PH3 + 3Ba(H2PO2)2 Ba(H2PO2)2 + H2SO4
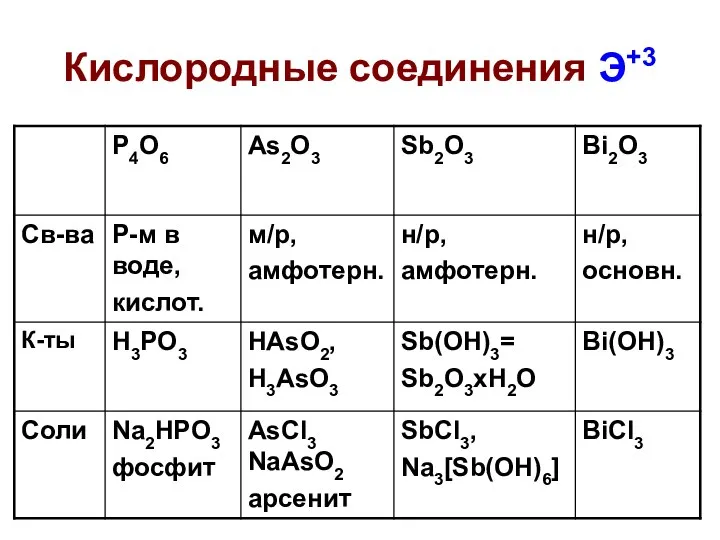
- 30. Кислородные соединения Э+3
- 31. Кислородные соединения Э+3 H3PO3 – фосфористая кислота, ДВУХОСНОВНАЯ, средняя соль Na2HPO3 (фосфит натрия) pKa1 = 2,
- 32. Реакции ЭГ3 (Г = галогенид ион) ЭCl3 + 3H2O = H3ЭO3 + 3HCl (Э = P,
- 33. Ox/red св-ва кислородных соединений P+3 Диспропорционирование H3PO3 4H3PO3(безводная) = 3H3PO4 + PH3 (при Т) H3PO3 –
- 34. В щелочной среде Bi3+ может быть окислен или восстановлен Bi(OH)3 + Cl2 +3KOH = KBiO3 +
- 35. Кислородные соединения Э+5
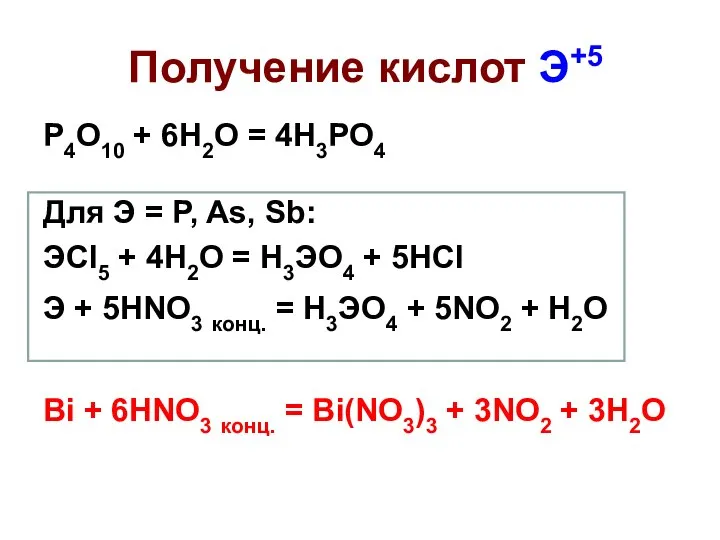
- 36. Получение кислот Э+5 P4O10 + 6H2O = 4H3PO4 Для Э = P, As, Sb: ЭCl5 +
- 37. Ox свойства Э+5 Соли BiO3– можно получить только в сильнощелочной среде в кислой среде BiO3– ОЧЕНЬ
- 38. As5+ и Sb5+ слабые окислители и только в кислой среде: H3AsO4 + 2HI = I2 +
- 40. Скачать презентацию





![Кислородные соединения N+5 N2O5 – б/ц тв., неустойчив, [NO2]+[NO3]–, в газе](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1393640/slide-7.jpg)


























 ПРЕЗЕНТАЦІЯ НА ТЕМУ “МІНЕРАЛЬНІ ДОБРИВА”
ПРЕЗЕНТАЦІЯ НА ТЕМУ “МІНЕРАЛЬНІ ДОБРИВА”  Изомерия. (11 класс)
Изомерия. (11 класс) Презентация Палладий
Презентация Палладий  Строение и электрический заряд коллоидных частиц. Электрокинетические явления
Строение и электрический заряд коллоидных частиц. Электрокинетические явления Серная кислота. Физические свойства
Серная кислота. Физические свойства Удобрения. 9 класс
Удобрения. 9 класс Химия Кислотные дожди.
Химия Кислотные дожди.  Циклические углеводороды
Циклические углеводороды Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционир
Общие закономерности реакционной способности органических соединений как химическая основа их биологического функционир лекарства Урок-защита проектов Разработала учитель химии МОУ «Гимназия №1» г. Саратова Шишкина И.Ю.
лекарства Урок-защита проектов Разработала учитель химии МОУ «Гимназия №1» г. Саратова Шишкина И.Ю.  Цветные реакции белков Качественные реакции на остатки аминокислот
Цветные реакции белков Качественные реакции на остатки аминокислот  Все о лаках для волос
Все о лаках для волос Praktická cvičení z biochemie
Praktická cvičení z biochemie Презентация по Химии "Проблеми використання відходів видобутку та переробки" - скачать смотреть бесплатно
Презентация по Химии "Проблеми використання відходів видобутку та переробки" - скачать смотреть бесплатно Презентация по Химии "Вплив побутової хімії на здоров'я людини" - скачать смотреть бесплатно
Презентация по Химии "Вплив побутової хімії на здоров'я людини" - скачать смотреть бесплатно Гибридизация атомных орбиталей
Гибридизация атомных орбиталей Фазовые превращения в однокомпонентных системах
Фазовые превращения в однокомпонентных системах Sm-Nd метод
Sm-Nd метод Нержавеющая сталь
Нержавеющая сталь Петрография магматических пород
Петрография магматических пород Сократительная функция всех типов мышц
Сократительная функция всех типов мышц Натуральный яблочный уксус
Натуральный яблочный уксус Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы
Қышқылды-сілтілі тепетеңдік бұзылысының клиникалық биохимиясы Альтернативні види палива
Альтернативні види палива  Хроматографія. Мікрогетерогенні дисперсні системи
Хроматографія. Мікрогетерогенні дисперсні системи Изготовление натурального мыла в домашних условиях
Изготовление натурального мыла в домашних условиях Химическое производство и химический процесс. (Тема 1)
Химическое производство и химический процесс. (Тема 1) Неорганические соединения. Вода. Роль воды в клетке
Неорганические соединения. Вода. Роль воды в клетке