Содержание
- 2. Цель: Познакомить с научными химическими достижениями во время Первой Мировой Войны и их последствиями. Расширить и
- 3. Историческая справка Эта история произошла во время I мировой войны. Ещё было далеко до рассвета, но
- 4. Проблема Химия и Первая Мировая Война. Что связывает эти слова?
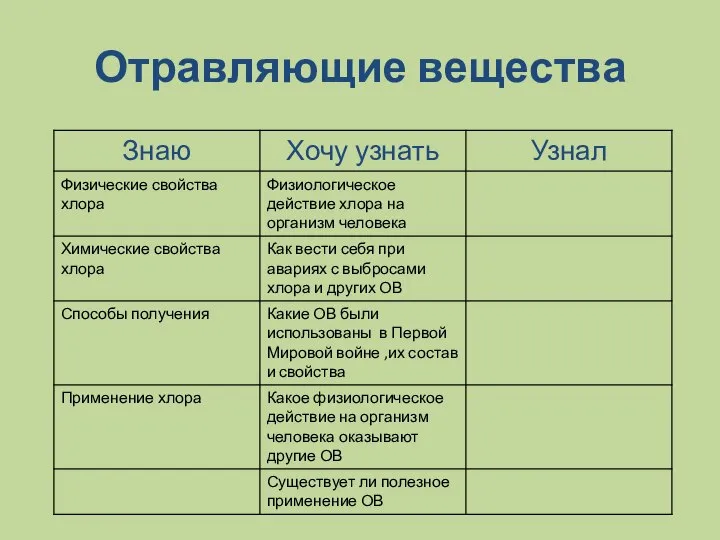
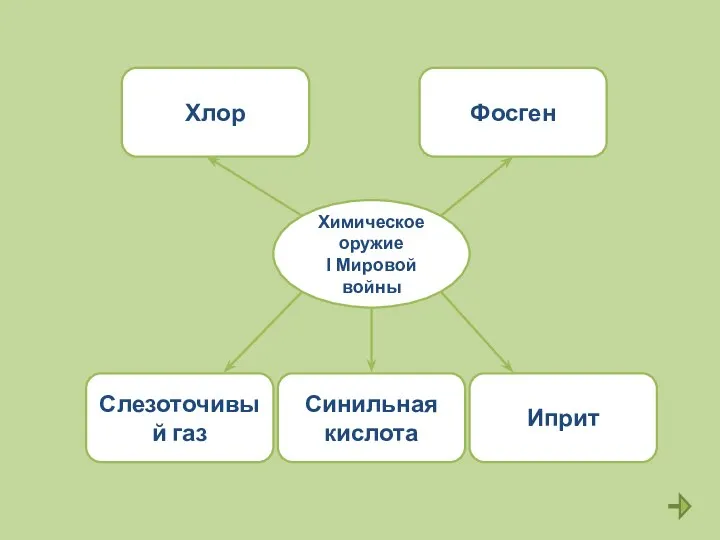
- 5. Отравляющие вещества
- 6. Хлор Физиологическое действие хлора на организм человека По физиологическому действию на организм хлор относится к группе
- 7. Нейтрализация хлора Основной способ нейтрализации – это взаимодействие с водой: Cl2 + H2O = HCl +
- 8. Слезоточивый газ
- 9. Фосген Физические свойства Фосген (СG) при обычных условиях бесцветный газ, тяжелее воздуха в 3,5 раза, с
- 10. Химические свойства фосгена - фосген хорошо гидролизуется, особенно в щелочной среде СОСl2 + 4NaOH → Na2CO3
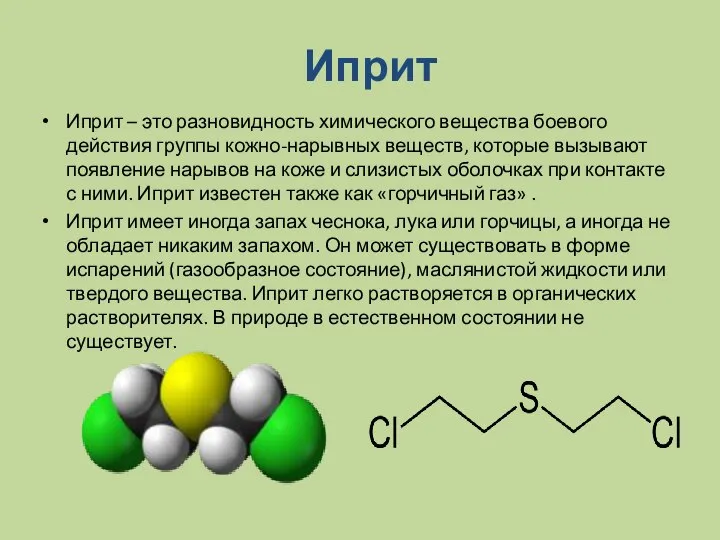
- 11. Иприт Иприт – это разновидность химического вещества боевого действия группы кожно-нарывных веществ, которые вызывают появление нарывов
- 12. Химические свойства иприта При обычной температуре иприт представляет собой устойчивое соединение. При нагревании выше 170 °C
- 13. Физиологическое действие на организм Иприт воздействует на организм, разрушая клеточные мембраны, нарушая обмен углеводов. Иприт поражает
- 14. Синильная кислота Физические свойства бесцветная, прозрачная, очень подвижная жидкость с запахом горького миндаля (при малых концентрациях),смешивается
- 15. Получение СН4 + NH3 +1,5 O2 → HCN + 4H2O в присутствии катализаторов Физиологическое действие на
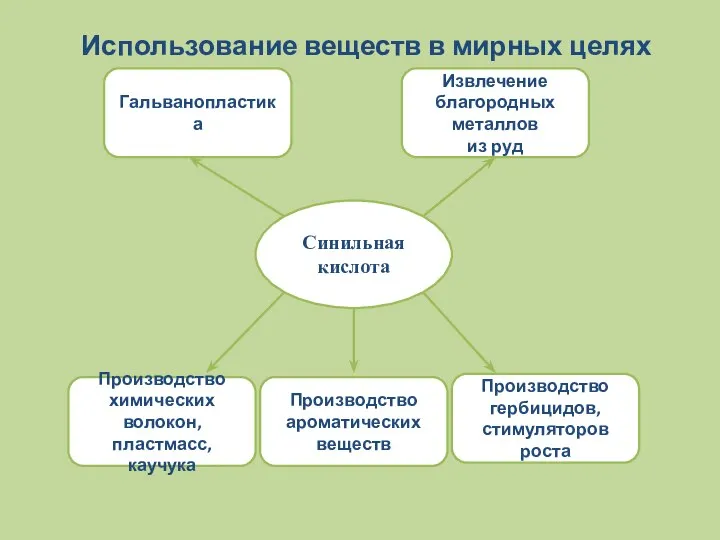
- 16. Использование веществ в мирных целях
- 17. Самостоятельная работа 1.Это произошло в солнечный день 22 апреля 1915 года. Солдаты увидели желтый туман, от
- 18. Соотнесите исторические события с используемыми ОВ Отравляющие вещества Фосген Хлор Синильная кислота Слезоточивый газ Иприт Историческое
- 19. Применение знаний в новых ситуациях Решите задачу: При аварии на химическом заводе произошла утечка 400 кг.
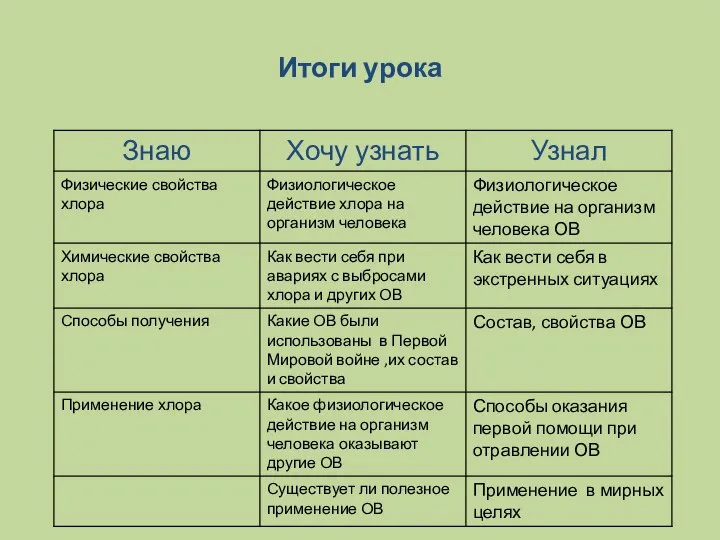
- 20. Итоги урока
- 21. Проблема уничтожения химического оружия Использование химического оружия в наши дни запрещено. Уничтожение арсеналов отравляющих веществ -
- 23. Скачать презентацию















 Открытие водорода
Открытие водорода Ионизирующее излучение и окружающая среда
Ионизирующее излучение и окружающая среда Углеводороды: изомерия
Углеводороды: изомерия Уравнения химической реакции
Уравнения химической реакции Поняття про номенклатуру Органічних сполук
Поняття про номенклатуру Органічних сполук  Фосфорное сырье. Применение и обогащение фосфорного сырья
Фосфорное сырье. Применение и обогащение фосфорного сырья Графическое представление газовых процессов. (10 класс)
Графическое представление газовых процессов. (10 класс) Мінерально-сировинні ресурси корисні копалини, які видобувають із надр Землі і використовують у різних галузях виробництва
Мінерально-сировинні ресурси корисні копалини, які видобувають із надр Землі і використовують у різних галузях виробництва  Презентация Предельные углеводороды
Презентация Предельные углеводороды  Неорганические вещества, входящие в состав клетки
Неорганические вещества, входящие в состав клетки Chemical reactions. (Chapter 5)
Chemical reactions. (Chapter 5) Синтез наночастиц неорганических веществ. (Лекция 7)
Синтез наночастиц неорганических веществ. (Лекция 7) Общая и неорганическая химия. Лекция 20 Особенности химии серы. Водородные и кислородные соединения
Общая и неорганическая химия. Лекция 20 Особенности химии серы. Водородные и кислородные соединения Неметаллы. Обобщение. Открытый урок
Неметаллы. Обобщение. Открытый урок Раздел: химия Научно-исследовательская работа Влияние тепловой кулинарной обработки овощей и хранения их в горячем состоянии н
Раздел: химия Научно-исследовательская работа Влияние тепловой кулинарной обработки овощей и хранения их в горячем состоянии н Неоднородные системы, их классификация, методы разделения. Лекция 4
Неоднородные системы, их классификация, методы разделения. Лекция 4 Биоактивные пептиды
Биоактивные пептиды Бордос сұйықтығын дайындау және оның сапасын тексеру
Бордос сұйықтығын дайындау және оның сапасын тексеру Растительные жиры. Пальмовое масло
Растительные жиры. Пальмовое масло Программа дополнительного образования «Химия, здоровье и окружающая среда»
Программа дополнительного образования «Химия, здоровье и окружающая среда» Комплексные соединения. Химическая связь. (Лекция 9)
Комплексные соединения. Химическая связь. (Лекция 9) Point defects. Line defects. Surface Imperfections
Point defects. Line defects. Surface Imperfections Строение атома водорода
Строение атома водорода Хромопротеиды. Патология пигментного обмена. Взаимосвязь обменов
Хромопротеиды. Патология пигментного обмена. Взаимосвязь обменов Медицинские резины
Медицинские резины Методы получения нафтиридинов (всех изомеров)
Методы получения нафтиридинов (всех изомеров) Распределение химических веществ по классам
Распределение химических веществ по классам Химическая промышленность Беларуси
Химическая промышленность Беларуси