Содержание
- 2. Хроматография - наука о межмолекулярных взаимодействиях и переносе молекул или частиц в системе несмешивающихся и движущихся
- 3. Элюент – жидкость или газ, используемые в качестве подвижной фазы. Элюат - выходящий из колонки поток
- 4. Колонка произвольно разделена на 18 теоретических тарелок. На колонку нанесено 512 молекул. Из них 256 (жирный
- 5. Теоретическая и практическая хроматограммы Идеальный вариант разделения смеси двух веществ Более реальный вариант разделения смеси тех
- 6. Основные параметры хроматограммы t0 – нулевое время tR1 – время удерживания для первого пика t’R1 –
- 7. Нормальное (Гауссово) распределение где H - высота, эквивалентная теоретической тарелке; L – длина колонки H =
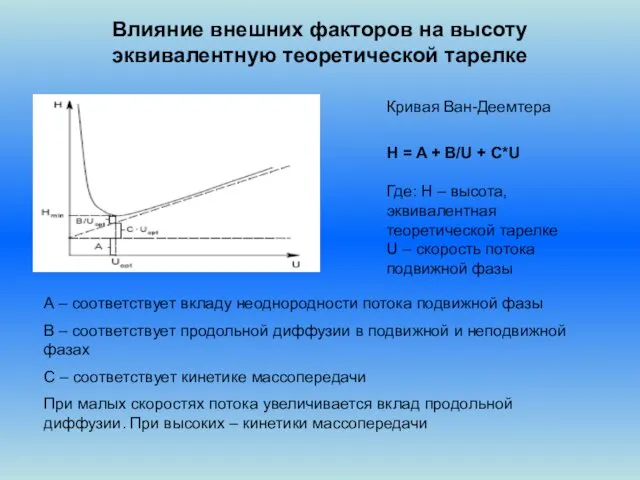
- 8. Влияние внешних факторов на высоту эквивалентную теоретической тарелке Кривая Ван-Деемтера H = A + B/U +
- 9. По агрегатному состоянию фаз Газовая хроматография Газо-жидкостная хроматография Газо-твёрдофазная хроматография Жидкостная хроматография Жидкостно-жидкостная хроматография Жидкостно-твёрдофазная хроматография
- 10. Ионообменная хроматография Ионообменная хроматография позволяет разделить молекулы, основываясь на ионных взаимодействиях. Неподвижная фаза имеет заряженные функциональные
- 11. Катионная ионообменная хроматография задерживает положительно заряженные катионы, так как неподвижная фаза имеет отрицательно заряженные функциональные группы,
- 12. Адсорбционная хроматография Вид хроматографии основанный на способности твёрдого вещества — неподвижной фазы — сорбировать примеси, находящиеся
- 13. Принципиальная схема В качестве лиганда могут выступать: Антитела Хелатирующие агенты Комплексообразующие агенты и т. д.
- 14. Эксклюзионная хроматография В эксклюзионной (ситовой, гель-проникающей, гель-фильтрационной) хроматографии молекулы веществ разделяются по размеру за счёт их
- 15. Принципиальная схема Наиболее распространенные сорбенты: Сефадекс Сефакрил Агарозные частицы (Биогели)
- 16. Осадочная хроматография Метод хроматографии, основанный на способности разделяемых веществ образовывать малорастворимые соединения с различными произведениями растворимости.
- 17. Распределительная хроматография В распределительной ВЭЖХ разделение происходит за счет разной растворимости разделяемых веществ в неподвижной фазе,
- 18. Принципиальная схема
- 19. ВЭЖХ высокоэффективная жидкостная хроматография HPLC/ВЭЖХ HPLC high-performance liquid chromatography high-pressure liquid chromatography По агрегатному состоянию фаз
- 20. Блок-схема жидкостного хроматографа
- 21. Принцип работы помпы Одноплунжерная помпа Двуплунжерная помпа
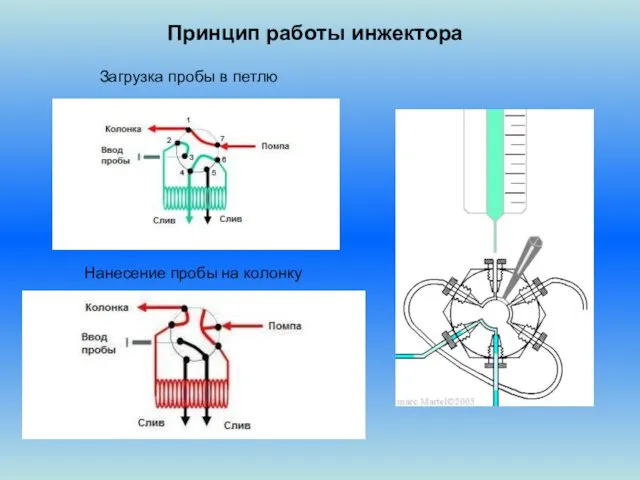
- 22. Принцип работы инжектора Загрузка пробы в петлю Нанесение пробы на колонку
- 23. Принцип работы UV-VIS детектора
- 24. Силикагель Матрицы ОФ-ВЭЖХ Полистирол, сшитый дивинилбензолом Оксиды алюминия, титана, циркония
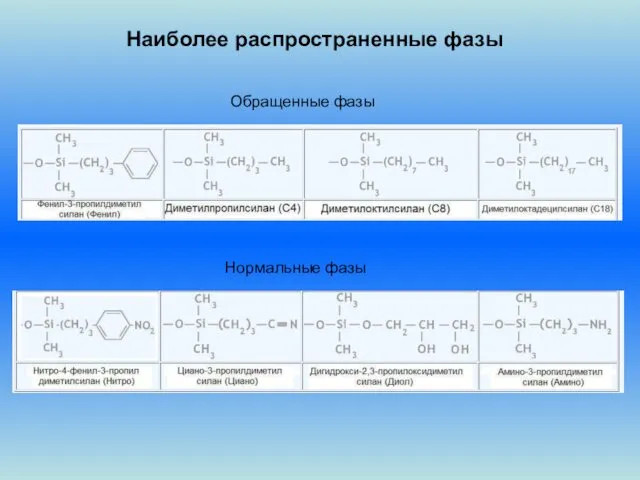
- 25. Наиболее распространенные фазы Обращенные фазы Нормальные фазы
- 26. Параметры и методы оценки сорбентов для обращенно-фазной хроматографии Параметр Метод оценки Эффективность N Число теоретических тарелок
- 27. Характеристики коммерческих сорбентов С18 для обращенно-фазной хроматографии Название Фирма КАБ аСН2 аТ/0 аК/Ф аБ/Ф N pH
- 28. Специализированные колонки в ВЭЖХ Сорбент Назначение колонок Hypersil Green Env Для анализа загрязнений окружающей среды (фенолов,
- 29. Сорбенты для обращенно-фазной хроматографии, приготовленные по нетрадиционной технологии или на несиликагелевой основе Сорбент Характеристики Diamond Band
- 30. Сорбент Характеристики Fluophase RP Перфторированные алкильные цепи Thermo Hypersil Fluophase WP Перфторированные алкильные цепи на силикагеле
- 31. Свойства растворителей для ВЭЖХ Адсорбционная сила растворителя ε0 – относительная энергия взаимодействия молекул подвижной фазы с
- 32. Классификация растворителей по Снайдеру Кругами выделены области, в которых группируются растворители по селективности: Xe – способность
- 33. Противоионы ион-парной хроматографии Анионы Катионы
- 34. Анионы: - Муравьиная кислота - Трифторуксусная кислота - Гептафтормасляная кислота Классические противоионы ОФ-ВЭЖХ хроматографии Катионы: -
- 35. Регенерация обращённо-фазовых колонок с внутренним диаметром 4.6 мм Подсоедините колонку к хроматографу в противоположном направлении. Промойте
- 37. Скачать презентацию































 Эта удивительная вода Эта удивительная вода
Эта удивительная вода Эта удивительная вода Кислород. 8 класс
Кислород. 8 класс Кислородсодержащие органические вещества. Фенолы
Кислородсодержащие органические вещества. Фенолы Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания
Бораты и силикаты как матрицы лазеров. Свойства и методы выращивания Отбор проб товаров для анализа. Химико-аналитический контроль
Отбор проб товаров для анализа. Химико-аналитический контроль Методы химического анализа. Классификации методов анализа
Методы химического анализа. Классификации методов анализа Природные и попутные нефтяные газы
Природные и попутные нефтяные газы Явление аллотропии
Явление аллотропии Теория растворов. Диффузия в растворах. Коллигативные свойства растворов
Теория растворов. Диффузия в растворах. Коллигативные свойства растворов Обмен простых белков. Пути обмена аминокислот. (Тема 5)
Обмен простых белков. Пути обмена аминокислот. (Тема 5) Сера. Положение серы в периодической системе химических элементов Д.И. Менделеева
Сера. Положение серы в периодической системе химических элементов Д.И. Менделеева Подготовка к контрольной работе по химии
Подготовка к контрольной работе по химии Виды контроля коррозии
Виды контроля коррозии Біологічна хімія з основами фізичної і колоїдної хімії
Біологічна хімія з основами фізичної і колоїдної хімії Презентация по Химии "Углеводы" - скачать смотреть
Презентация по Химии "Углеводы" - скачать смотреть  Лабораторное оборудование, посуда и средства защиты Разработка для проведения практических работ по химии подготовила Нерев
Лабораторное оборудование, посуда и средства защиты Разработка для проведения практических работ по химии подготовила Нерев Состав воздуха и его загрязненность Отдел образования администрации Тальменского района Алтайского края
Состав воздуха и его загрязненность Отдел образования администрации Тальменского района Алтайского края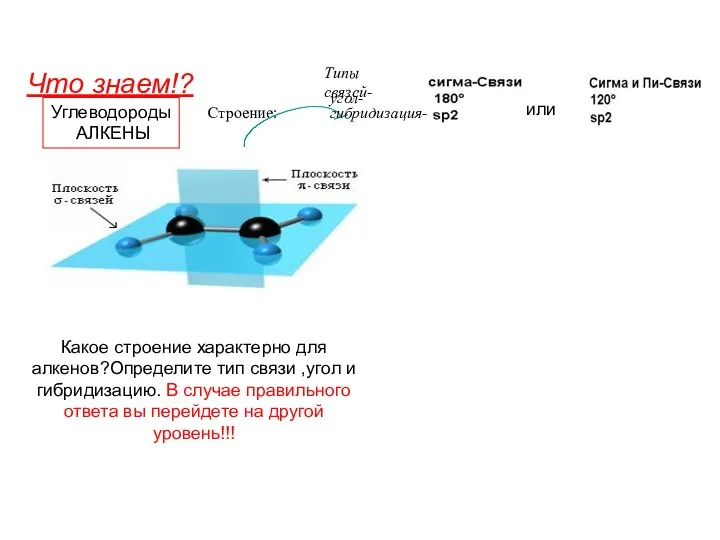 Углеводороды. Алкены
Углеводороды. Алкены Жиры – биологически важные органические соединения Работа ученицы 11а класса МБОУ СОШ № 26 Ногинского района Московской облас
Жиры – биологически важные органические соединения Работа ученицы 11а класса МБОУ СОШ № 26 Ногинского района Московской облас Стратегия успеха 2 (ЕГЭ). Органическая химия
Стратегия успеха 2 (ЕГЭ). Органическая химия Чистые вещества и смеси. Способы разделения смесей
Чистые вещества и смеси. Способы разделения смесей Фосфор и его соединения
Фосфор и его соединения Виды топлива и их характеристика
Виды топлива и их характеристика Технология получения гидропероксида изопропилбензола
Технология получения гидропероксида изопропилбензола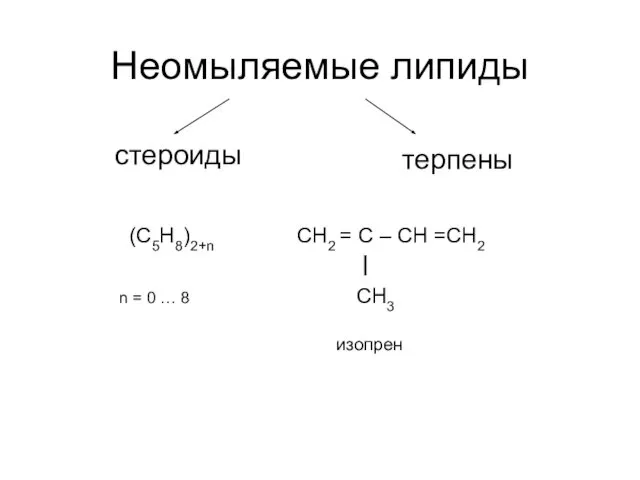 Неомыляемые липиды. Стероиды
Неомыляемые липиды. Стероиды Адсорбция. Поглощение газов или паров из газовых смесей или растворов твердым веществом
Адсорбция. Поглощение газов или паров из газовых смесей или растворов твердым веществом Презентация Простые вещества химия 8 класс
Презентация Простые вещества химия 8 класс Химия вокруг нас
Химия вокруг нас