Содержание
- 3. Точки пересечения прямых Е-lg и E-lg для каждой из двух ОВР (5) и (6) дают значения
- 4. В реальном коррозионном биэлектроде ( М в растворе, содержащем Мn+ , Ох и R) рЕМn+/М и
- 5. C учетом (8) и (9) переходит в (12), j ≡ipM. j ≡ipM = iвR (12) Если
- 6. Если условия (12) и (13) не соблюдаются, потенциал под током не стационарен. Кривые E-lg iк и
- 7. В ы х о д п о т о к у В ы х о д
- 8. Если между катодным и анодным участками существует омическое падение напряжения. Графически уравнение закона Ома описывается прямой
- 9. пересечения дает один Екор и максимальную скорость коррозии jмах. Для учета омического фактора следует перестроить одну
- 11. Виды контроля коррозии При стационарном Екор растворение металла и катодная деполяризация являются сопряженными реакциями, изменение скорости
- 13. Рис. а,б иллюстрируют роль i0. Если , процесс протекает с катодным контролем (рис. а) и изменение
- 14. На рис. в,г показана роль крутизны поляризационных кривых. При bк ≈ ∞, что имеет место в
- 15. Сложные коррозионные системы Короткозамкнутая система ( R≈0), у которой поверхность всех металлов, находящихся в электрическом контакте,
- 16. Суммарные кривые E-Ja, E-Jк .
- 17. Кривая ( ) (при заданном Е) начинается от и до совпадает с кривой т.к. при этих
- 18. при М1 и М2 являются анодами, причем > , а М3 – катод. При этом |
- 19. Используя J вместо i , получаем JpM = Jа + JвR () JвR = Jк +
- 20. Парциальные кривые
- 21. Эти кривые идут от равновесного потенциала, а не от Екор. Аналогично проводится суммирование. Кривая начинается от
- 23. Скачать презентацию




















 Термический анализ
Термический анализ Презентация по Химии "«Чайная презентация»" - скачать смотреть бесплатно
Презентация по Химии "«Чайная презентация»" - скачать смотреть бесплатно Растворы электролитов
Растворы электролитов Углеводороды: изомерия
Углеводороды: изомерия Հիալուրոնաթթվի անջատումը ձվի կեղևից և դրա նույնականացումը բարձրարդյունավետ. Հեղուկային քրոմատոգրաֆիայի եղանակով
Հիալուրոնաթթվի անջատումը ձվի կեղևից և դրա նույնականացումը բարձրարդյունավետ. Հեղուկային քրոմատոգրաֆիայի եղանակով ЙОД ( I ) Презентація Учениці 10-В Сухарської Ольги
ЙОД ( I ) Презентація Учениці 10-В Сухарської Ольги  Аминокислоты. Белки. Пептиды
Аминокислоты. Белки. Пептиды Круговорот химических веществ в природе Выполнила: Подсыпанина Наташа Ученица: 10 «А» класса Учитель: Макарова Е. И.
Круговорот химических веществ в природе Выполнила: Подсыпанина Наташа Ученица: 10 «А» класса Учитель: Макарова Е. И. Лабораторная посуда и оборудование
Лабораторная посуда и оборудование Выполнил ученик 11-б класса МОУ СОШ №41 Гандилян Армен Руководитель: Изместьева Н.Д. Красноярск
Выполнил ученик 11-б класса МОУ СОШ №41 Гандилян Армен Руководитель: Изместьева Н.Д. Красноярск  Презентация по Химии "Органическая химия. история развития" - скачать смотреть
Презентация по Химии "Органическая химия. история развития" - скачать смотреть  Общая характеристика элементов VII А группы
Общая характеристика элементов VII А группы Коллоидная химия
Коллоидная химия Структура и свойства чистого титана
Структура и свойства чистого титана Биологически важные гетероциклы
Биологически важные гетероциклы Состав тонких покрытий
Состав тонких покрытий Презентация по Химии "Презентация Коррозия металлов" - скачать смотреть
Презентация по Химии "Презентация Коррозия металлов" - скачать смотреть 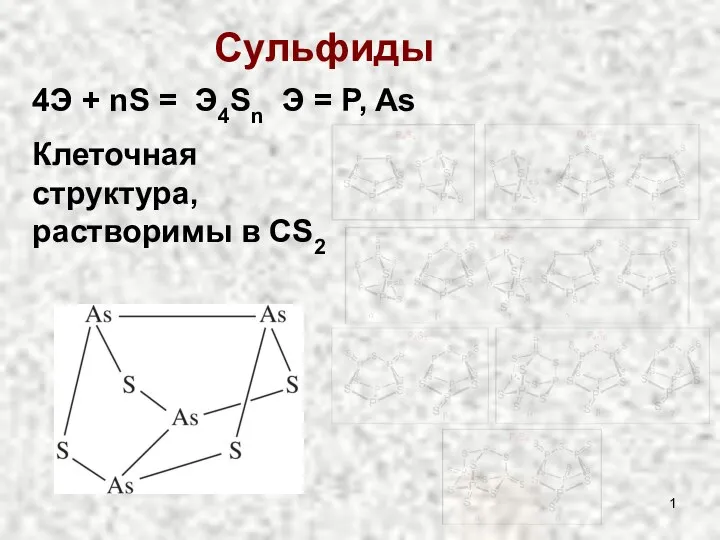 Сульфиды и оксиды
Сульфиды и оксиды Методы диффузионной металлизации
Методы диффузионной металлизации Виды коррозии
Виды коррозии Презентация по Химии "«Атомы химических элементов»." - скачать смотреть бесплатно
Презентация по Химии "«Атомы химических элементов»." - скачать смотреть бесплатно Характеристика химического элемента S
Характеристика химического элемента S Сапалық талдау. Сапалық аналитикалық реакциялар
Сапалық талдау. Сапалық аналитикалық реакциялар Классификация химических реакций в неорганической химии
Классификация химических реакций в неорганической химии Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще
Даны буквы: Р, З, И, О, А, П, Т, М. В этих буквах спрятано название элемента, про который известно: - воздух на 78% состоит из простого веще Гомологи бензола
Гомологи бензола Механизм реакции в органической химии
Механизм реакции в органической химии Состав и строение металлических кристаллов в титаномагнетитовой руде при медленном росте
Состав и строение металлических кристаллов в титаномагнетитовой руде при медленном росте