Содержание
- 2. "Если бы в результате какой-то мировой катастрофы все накопленные научные знания оказались бы уни- чтоженными, и
- 3. В 1869 году Д.И.Менделеев обнародовал периоди-ческий закон и его следствие - таблицу элементов. В 1870 году
- 4. "Короткая" форма таблицы, 2000-й год
- 5. Объяснение периодической системы элементов – одна из важнейших задач атомной физики. Сформулируем прежде всего те принципы,
- 6. 2) Принцип Паули: В атоме может существо-вать только один электрон в состоянии, характеризуемом данными значениями четырех
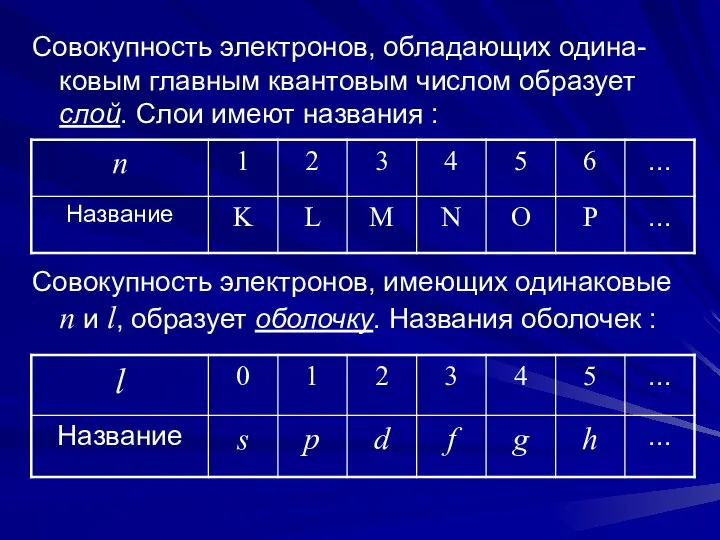
- 7. Совокупность электронов, обладающих одина-ковым главным квантовым числом образует слой. Слои имеют названия : Совокупность электронов, имеющих
- 8. Принцип Паули ограничивает число электронов на той или иной электронной оболочке. Дейст-вительно, электроны в невозбужденном атоме
- 9. Установим теперь, сколько электронов может находится на оболочке и в атоме. Т.к. число ms может иметь
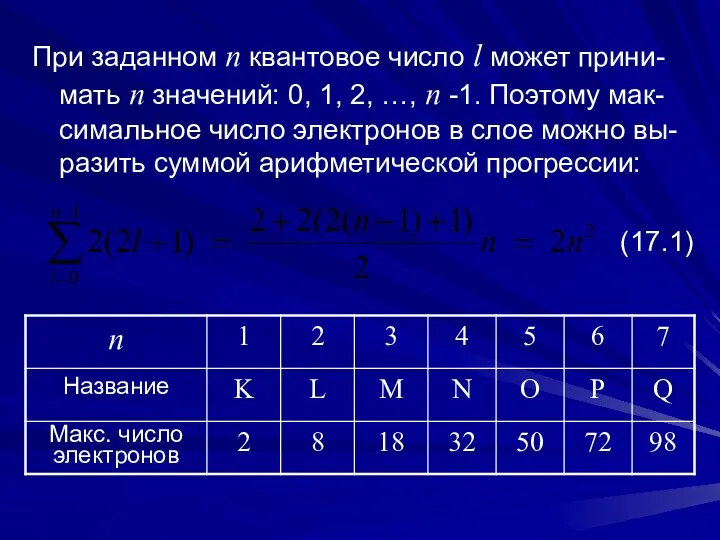
- 10. При заданном n квантовое число l может прини-мать n значений: 0, 1, 2, …, n -1.
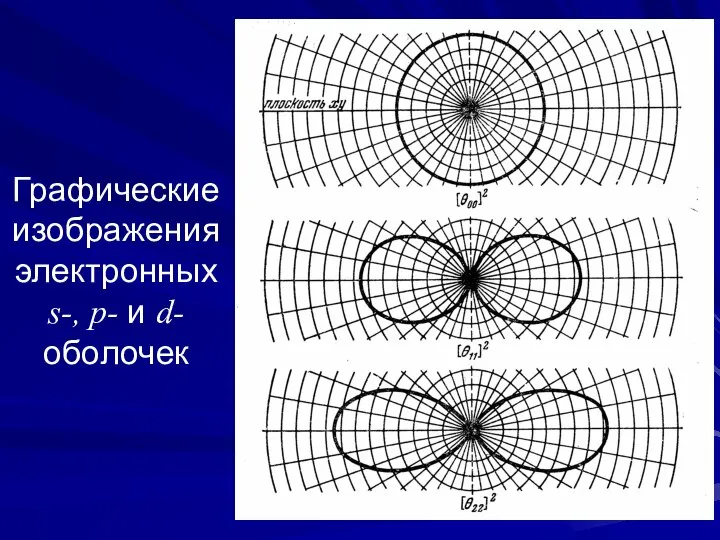
- 11. Графические изображения электронных s-, p- и d-оболочек
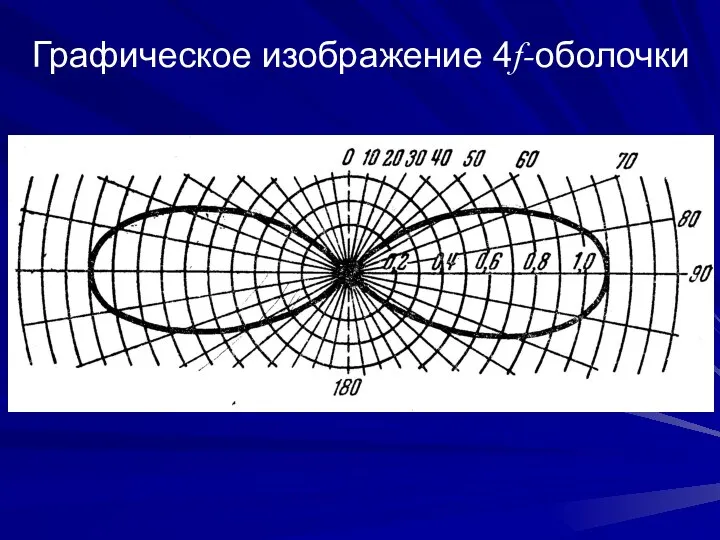
- 12. Графическое изображение 4f-оболочки
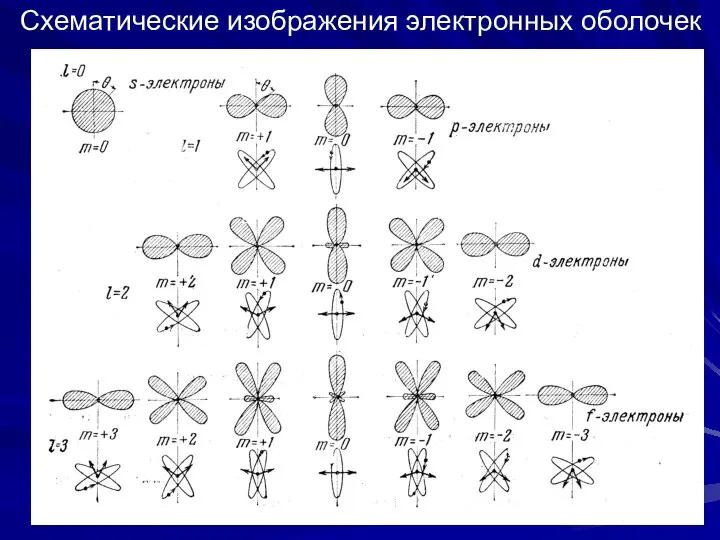
- 13. Схематические изображения электронных оболочек
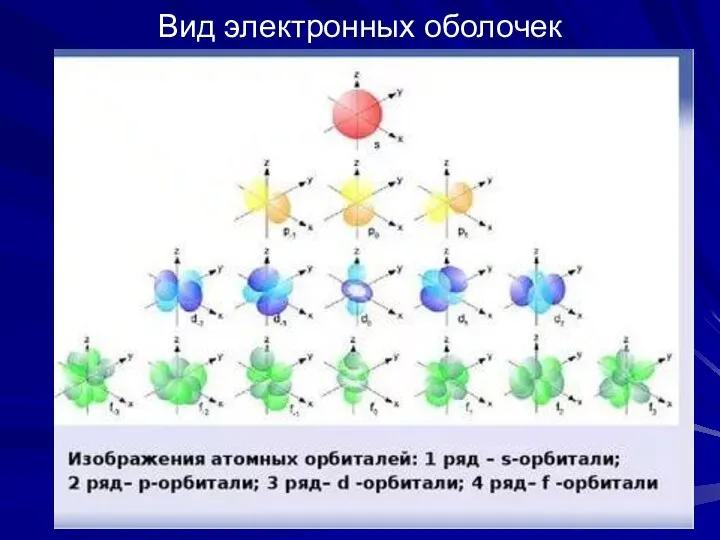
- 14. Вид электронных оболочек
- 15. Конфигурация электронных оболочек атомов за-писывается с помощью следующих обозначе-ний. Каждая оболочка обозначается соответст-вующим n и буквой,
- 16. Итак, принцип Паули дает следующую картину пост-роения электронной оболочки атомов. Каждый вновь присоединяемый электрон связывается в
- 17. Например, 19-ый электрон калия должен (соглас-но идеальной схеме) находиться в 3d-оболоч-ке. Однако химические и спектроскопические данные
- 18. По этой же причине 20-ый электрон кальция тоже присоединяется в 4s-состояние, а нормальное за- полнение 3d-оболочки
- 19. Еще несколько примеров конфигураций электрон-ных оболочек атомов: 19 Калий 1s22s22p63s23p64s1 = [Ar]4s1 20 Кальций [Ar]4s2 36
- 20. Таким образом, атомная физика полностью объяс- нила периодическую таблицу элементов. Причем теория не только объяснила, но
- 21. Недостатки короткой формы таблицы Из-за того, что короткая таблица ограничена 8-ю столбцами, приходится подразделять 4-й и
- 22. Длинная форма таблицы В 1989 году Международный союз теоретической и прикладной химии (International Union of Pure
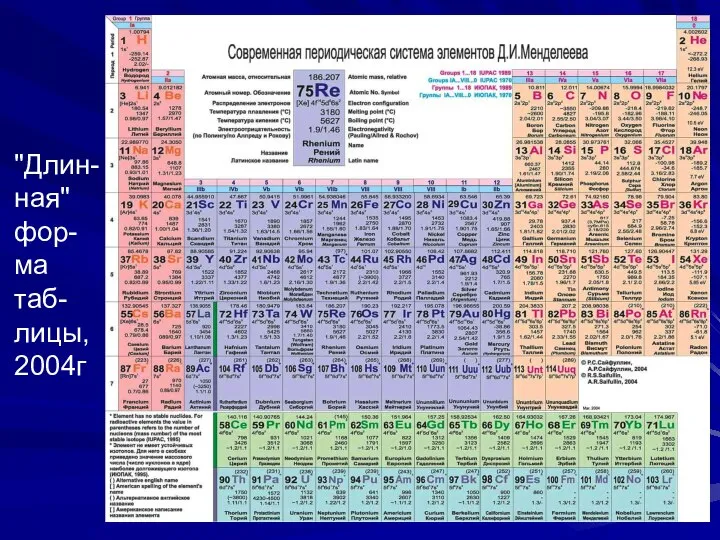
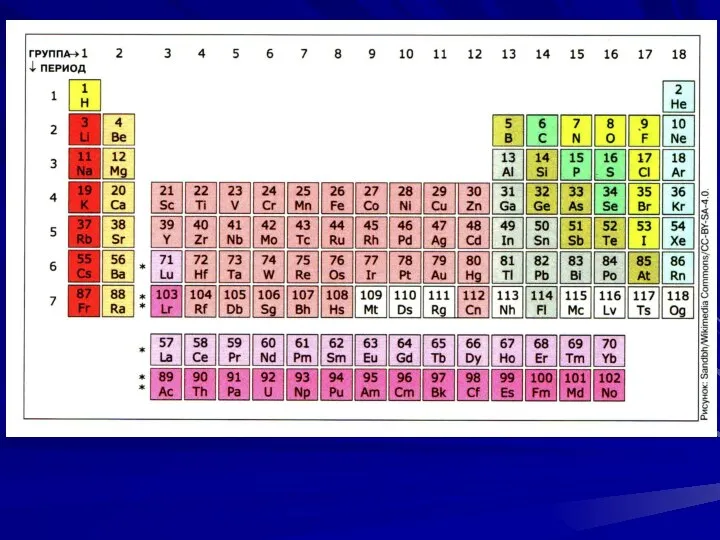
- 23. "Длин-ная" фор-ма таб-лицы, 2004г
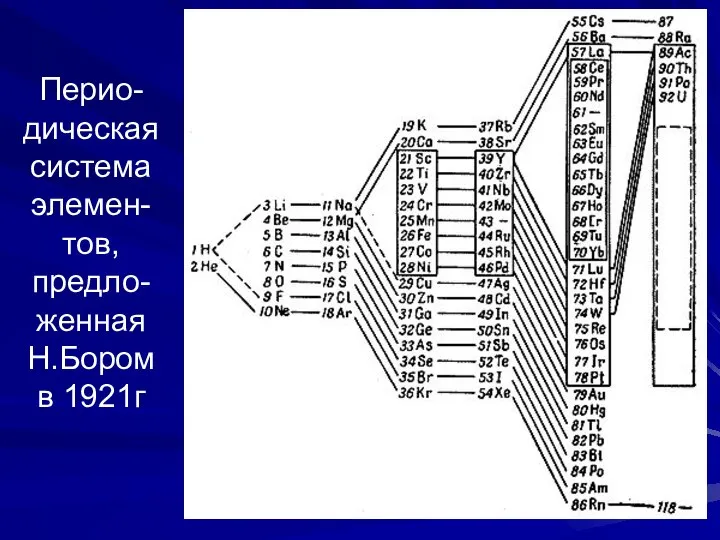
- 24. Перио-дическая система элемен-тов, предло-женная Н.Бором в 1921г
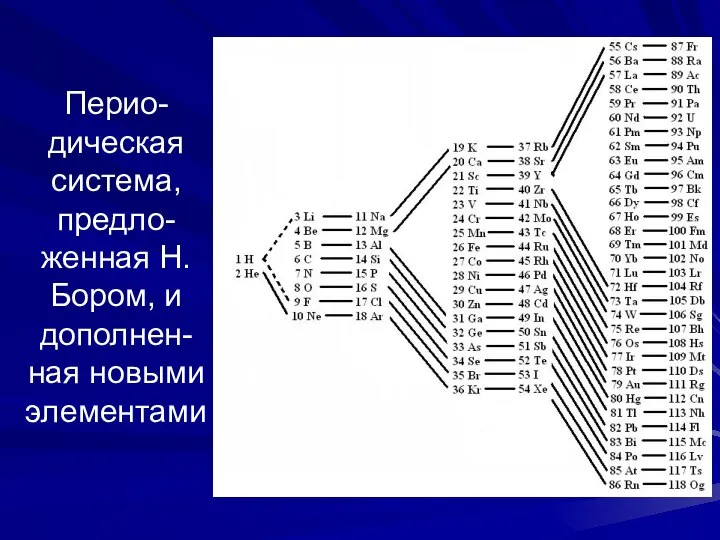
- 25. Перио-дическая система, предло-женная Н.Бором, и дополнен-ная новыми элементами
- 26. Состав атомных ядер Ядра состоят из протонов и нейтронов. Электричес-кий заряд протона e = 1.6·10-19 Кл,
- 27. В настоящее время известно (существуют в природе или получены искусственно) ок. 3000 ядер с раз-личными значениями
- 28. Большинство элементов имеют по несколько ста-бильных изотопов, рекорд принадлежит олову (Z=50), у которого 10 стабильных изотопов.
- 29. Другие примеры изотопов: Гелий имеет 2 стабильных изотопа (они также есть в природе): 4He2 (обычный гелий)
- 30. Искусственные химические элементы До 1937г оставались неизвестными 4 элемента до урана: с номерами Z = 43,
- 31. Технеций (Technetium, Tc) В настоящее время известно 16 изотопов технеция с массовыми числами от 92 до
- 32. Франций Элемент №87 был обнаружен в 1939 году французс- ким радиохимиком Маргаритой Перей (Marguerite Perey) в
- 33. Франций Франций - первый элемент 7-го периода таблицы Д.И.Менделеева и самый химически активный ще-лочной металл. Формула
- 34. Астат (Astatium, At) Элемент №85 был получен в 1940 году (Д.Корсон, К.Р.Маккензи, Э.Сегре, Калифорнийский универси-тет в
- 35. Применение астата Изотоп астат-211 считается перспективным для при-менения в медицине. Это чистый (т.е. без сопро-вождающего гамма-
- 36. Прометий (Prometium, Pm) В 1945г американские химики Д.Маринский (J.Marins-ky), Л.Гленденин (L.Glendenin) и Ч.Кориэлл (C.Co-ryell) с помощью
- 37. Применение прометия Металлический прометий имеет гексагональную кри-сталлическую структуру, плотность 7.3г/см3, тем-пература плавления ок.1100оС, кипения ок.3000оС. Наибольшее
- 38. Первые трансурановые элементы: нептуний и плутоний Эти элементы получают в результате реакции радиационного захвата нейтрона ядрами
- 39. Нептуний и плутоний получили свои названия по аналогии с названиями планет Солнечной систе-мы: Нептун и Плутон,
- 40. В настоящее время известно 15 изотопов нептуния, наиболее долгоживущий среди них изотоп 237Np93 (T1/2 =2.14·106 лет).
- 41. Америций После того, как было накоплено достаточное коли-чество плутония-239, появилась возможность по-лучения следующих трансурановых элементов. 95-й
- 42. Назван в честь страны открытия, латинское назва-ние Americium (Am). В настоящее время известно 11 изотопов америция,
- 43. Кюрий 96-й элемент также был получен в 1944 г в той же лаборатории в США той
- 44. Берклий После накопления достаточного количества амери-ция, в 1949 году в той же лаборатории в США под
- 45. Калифорний После накопления достаточного количества кюрия, в 1950 году в США под рук. Г.Сиборга был получен
- 46. Эйнштейний и Фермий 99-й и 100-й элементы открыли американские физи-ки А.Гиорсо (A.Ghiorso), С.Томпсон (S.G.Thomp-son) и Г.Хиггинс
- 47. Позднее эти элементы были также получены по тра-диционной схеме, облучением ядер берклия и ка-лифорния альфа-частицами. В
- 48. Менделевий После того, как было накоплено достаточное количе-ство атомов эйнштейния, в 1955 году в той же
- 49. Нобелий, Nobelium (No) Впервые о синтезе 102-го элемента сообщила в 1957 г международная группа физиков, работав-ших
- 50. Ускоритель тяжелых ионов Дубненский циклотрон У-400
- 51. Ускоритель тяжелых ионов Дубненский циклотрон У-400
- 52. 102-й элемент был получен в 3-х реакциях: В настоящее время известно 10 изотопов нобелия, наиболее долгоживущий
- 53. Лоуренсий, Lawrencium (Lr) Впервые о синтезе ядер 103-го элемента в 1961 г со-общил А.Гиорсо (лаборатория в
- 54. Резерфордий (Rf) С 60-х гг прошлого века, после того, как был постро- ен У-400, дубненская лаборатория
- 55. 105-й элемент Дубний (Db) впервые получен в 1970 г в Дубне в реакции Сейчас известно 4
- 56. 108-й элемент Хассий (Hs) синтезирован в 1984 г в лаборатории г. Дармштадт (Германия) в реакции: Назван
- 57. 111-й элемент Рентгений (Rg) синтезирован в 1994 г в лаборатории г. Дармштадт в реакции: Наиболее долгоживущий
- 58. 114-й элемент Флеровий (Fl) синтезирован в России в ОИЯИ (г. Дубна) в 1999 г в реакции:
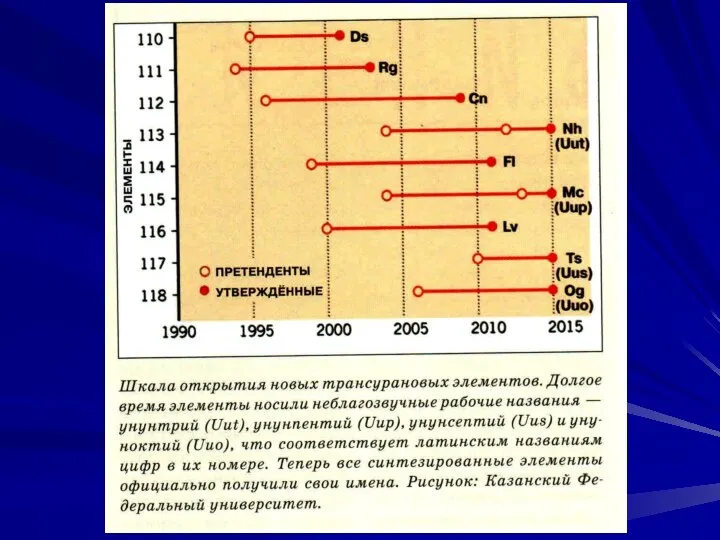
- 59. 117-й элемент Теннесин (Ts) синтезирован в США в 2010 г в реакции: Назван в честь штата
- 62. Зависимость энергии связи ядра от параметра деформации Пунктирная кривая соот- ветствует Z2/A > 49, т.е. Z
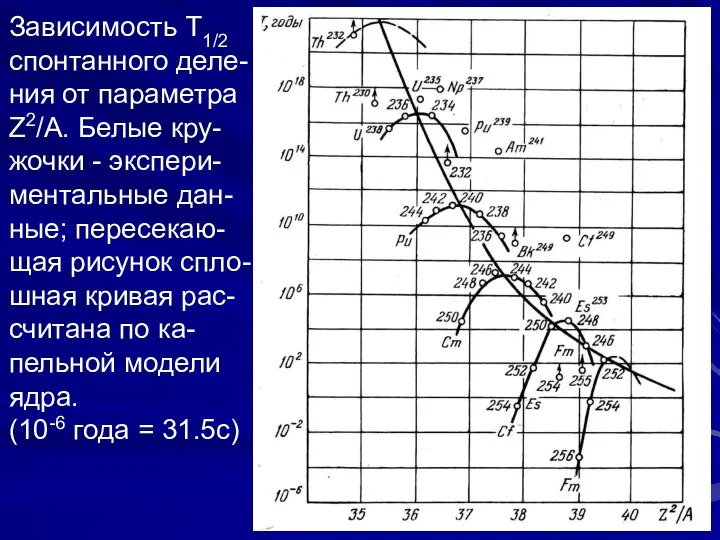
- 63. Зависимость T1/2 спонтанного деле- ния от параметра Z2/A. Белые кру- жочки - экспери- ментальные дан- ные;
- 65. Скачать презентацию


















































 Биосинтез заменимых аминокислот. Деградация нуклеиновых кислот. (Лекция 4)
Биосинтез заменимых аминокислот. Деградация нуклеиновых кислот. (Лекция 4) Выдающиеся ученые - химики и их заслуги
Выдающиеся ученые - химики и их заслуги Альбітит-грейзенові родовища
Альбітит-грейзенові родовища Синтетические лекарственные средства
Синтетические лекарственные средства Презентация по химии на тему: «Применение кислорода»
Презентация по химии на тему: «Применение кислорода» Титриметрический анализ. Сущность титриметрического анализа
Титриметрический анализ. Сущность титриметрического анализа Химическая посуда и ее назначения (5)
Химическая посуда и ее назначения (5) Вчені - хіміки
Вчені - хіміки  Кинетика химических реакций. Основные понятия и законы химической кинетики
Кинетика химических реакций. Основные понятия и законы химической кинетики Роль женщин в химическом образовании и науке
Роль женщин в химическом образовании и науке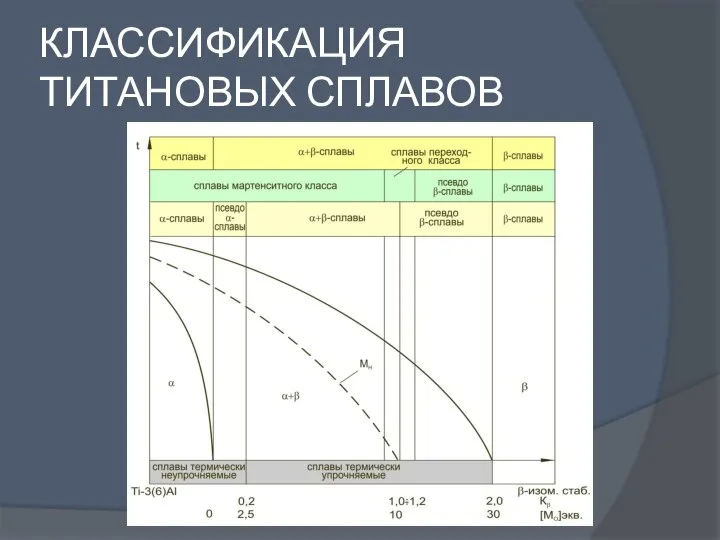 Классификация титановых сплавов
Классификация титановых сплавов Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота
Сероводород, Сульфиды. Оксид серы (IV). Сернистая кислота Бета-окисление жирных кислот
Бета-окисление жирных кислот Органічні сполуки Жири, білки, вуглеводи, вітаміни як компоненти їжі, їх роль в організмі.
Органічні сполуки Жири, білки, вуглеводи, вітаміни як компоненти їжі, їх роль в організмі.  Электрохимические методы анализа
Электрохимические методы анализа Превращение веществ в одной среде
Превращение веществ в одной среде Атомы и молекулы
Атомы и молекулы Дослід Ознайомлення зі змістом етикеток харчових продуктів
Дослід Ознайомлення зі змістом етикеток харчових продуктів  Адсорбционные равновесия. Межмолекулярные взаимодействия при адсорбции
Адсорбционные равновесия. Межмолекулярные взаимодействия при адсорбции Арены. 10 класс
Арены. 10 класс Горение вещества и способы его прекращения
Горение вещества и способы его прекращения Противомикробное средство растительного происхождения, хлорофиллипт
Противомикробное средство растительного происхождения, хлорофиллипт Химические свойства оксидов
Химические свойства оксидов Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон
Выполнила: Ученица 11 «Б» класса Урывкова Анастасия Кон Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.
Металлы ГОУ СОШ № 661 УЧИТЕЛЬ ХИМИИ Ефремова С.А.  Явище ізомерії. Структурна ізомерія Близнюки органічного світу
Явище ізомерії. Структурна ізомерія Близнюки органічного світу  Типы изомерии
Типы изомерии Тест по теме Алкины
Тест по теме Алкины