Содержание
- 2. Титриметрический анализ основан на точном измерении количества реактива, израсходованного на реакцию с определяемым веществом. Титр (от
- 3. Титрованный, или стандартный, раствор - раствор, концентрация которого известна с высокой точностью. Титрование - прибавление титрованного
- 4. В титриметрическом анализе может быть использована не любая химическая реакция. Реакции, применяемые в титриметрии, должны удовлетворять
- 5. Объемный анализ - метод количественного анализа, где искомое вещество определяют по объему реактива с точно известной
- 10. Классификация методов титриметрического анализа В соответствии с характером используемых реакций различают следующие методы титриметрического анализа. 1.
- 11. В зависимости от применяемого реактива различают следующие методы: перманганатометрию, где используется реакция окисления перманганатом калия; иодометрию
- 12. 3. Методы осаждения и комплексообразования. В эти группы объединены методы, основанные на осаждении определенного иона в
- 13. аргентометрию, в которой используют реакцию иона серебра с галогенид-ионами; роданометрию, в которой используют реакцию иона серебра
- 14. Индикаторы и принцип их выбора Одним из важнейших условий выполнения объемного определения является фиксирование точки эквивалентности
- 16. Цвет индикатора будет зависеть от соотношения концентраций различно окрашенных ионов Ind- и молекул HInd. Если среда
- 17. Например, малиновая окраска фенолфталеина появляется в щелочной среде при рН 8,9-9,8. Этот интервал называется интервалом перехода
- 19. Таким образом, приступая к определению содержания кислот или оснований в растворе, следует заранее знать, какая реакция
- 20. Для правильного выбора индикатора сначала изучают, как меняется рН раствора в процессе титрования. К раствору кислоты
- 22. Основные приемы титрования Титрование щелочи кислотой является типичным примером прямого титрования. В методах прямого титрования определяемое
- 23. В методах обратного титрования (или, как их еще называют, методах титрования по остатку) используются два титрованных
- 24. Не вступившее в реакцию избыточное количество вещества оттитровывают вторым раствором (вспомогательным рабочим раствором). Содержание искомого компонента
- 25. Третьим основным видом титриметрических определений является титрование заместителя, или титрование по замещению (косвенное титрование). В этом
- 26. Метод нейтрализации включает все аналитические реакции между ионом водорода и гидроксид-ионом. Различают АЦИДИМЕТРИЧЕСКОЕ титрование (от acidium
- 27. При титровании сильной кислоты сильной щелочью снижается концентрация ионов водорода Н+. Допустим в колбе для титрования
- 28. По мере титрования концентрация ионов водорода [Н+] будет снижаться, изменится соответственно и рН раствора. Когда к
- 29. Когда будет прибавлено 99% щелочи (1/=19,8 мл), концентрация НСI cнижается до 0,001г-экв/л, [Н+] = 0,001 и
- 30. При прибавлении 20 мл 0,1н. раствора NaOH в раствор введено эквивалентное кислоте количество щелочи – достигнута
- 31. Если после достижения точки эквивалентности добавить к раствору еще 0,02 мл 01н. раствора NaOH (перетитровать раствор),
- 32. Метод оксидиметрии В объемном анализе методом оксидиметрии используют реакции, связанные с изменением степени окисления анализируемого вещества,
- 33. Если титруют раствором окислителя восстановленную форму анализируемого вещества, то по мере титрования она переходит в окисленную
- 34. Существуют различные способы определения точки эквивалентности при окислительно-восстановительном титровании. Скачок потенциала можно измерить с помощью специальных
- 35. ПЕРМАНГАНАТОМЕТРИЯ – метод объемного (титриметрического) химического анализа, основанный на применении стандартного (имеющего строго определенную концентрацию) раствора
- 36. В этом методе анализа рабочим раствором служит раствор перманганата калия КМnС4. Это соединение является сильным окислителем.
- 37. Последняя реакция имеет наибольшее значение в количественном анализе. Большая часть анализов методом перманганатометрии проводится в кислой
- 38. Титрование ведут постепенным прибавлением раствора перманганата калия к подкисленному раствору анализируемого вещества, обладающего свойствами восстановителя. Раствор,
- 39. Когда определяемый восстановитель полностью прореагирует, следующая капля раствора перманганата окрасит раствор в розовый цвет. По появлению
- 40. Методом перманганатометрии можно анализировать и восстановители и окислители. Восстановители определяют прямым титрованием, окислители – обратным: сначала
- 41. В основе метода иодометрии лежит реакция восстановления элементного иода до иодид-ионов и окисления иодид-ионов в элементный
- 42. Основным рабочим раствором в иодометрии служит раствор иода. Поскольку иод мало растворим в воде, его растворяют
- 43. При титровании этим соединением раствора, содержащего восстановитель, по мере прибавления иод восстанавливается в иодид-ионы. В точке
- 44. Многие аналитические иодометрические реакции протекают с невысокой скоростью, и определение ведут обратным титрованием. К анализируемому раствору
- 45. При анализе окислителей используют следующий прием обратного титрования. К анализируемому раствору добавляют заведомый избыток иодида калия.
- 46. Титрование ведут с индикатором, в качестве которого используют крахмал, образующий в присутствии иода интенсивно окрашенное синее
- 47. МЕТОДЫ ОСАЖДЕНИЯ В объемном анализе используются некоторые реакции, приводящие к образованию осадка. К этим реакциям предъявляются
- 48. Принципиальное отличие объемного анализа методом осаждения от гравиметрического состоит в том, что о количестве вещества судят
- 50. Скачать презентацию


























![По мере титрования концентрация ионов водорода [Н+] будет снижаться, изменится соответственно](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404459/slide-27.jpg)




















 Полимеры
Полимеры Презентация по Химии "Белки" - скачать смотреть _
Презентация по Химии "Белки" - скачать смотреть _ Окислительно-восстановительные реакции в органической химии
Окислительно-восстановительные реакции в органической химии Значення білків, жирів та вуглеводів у харчуванні людини
Значення білків, жирів та вуглеводів у харчуванні людини  Химические элементы. Викторина
Химические элементы. Викторина Вещества, действующие на мембрану клетки и клеточную стенку. Занятие 5
Вещества, действующие на мембрану клетки и клеточную стенку. Занятие 5 Вода Самое удивительное вещество
Вода Самое удивительное вещество Обобщение знаний об углеводородах Автор Акимова Ольга Васильевна учитель химии, высшая квалификационная категория МАОУ Барыби
Обобщение знаний об углеводородах Автор Акимова Ольга Васильевна учитель химии, высшая квалификационная категория МАОУ Барыби Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов
Химическая связь. Валентность элементов в ковалентных соединениях. Степень окисления элементов «Мінеральні добрива»
«Мінеральні добрива»  Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)
Электролитическая диссоциация(ЭД). Теория электролитической диссоциации (ТЭД)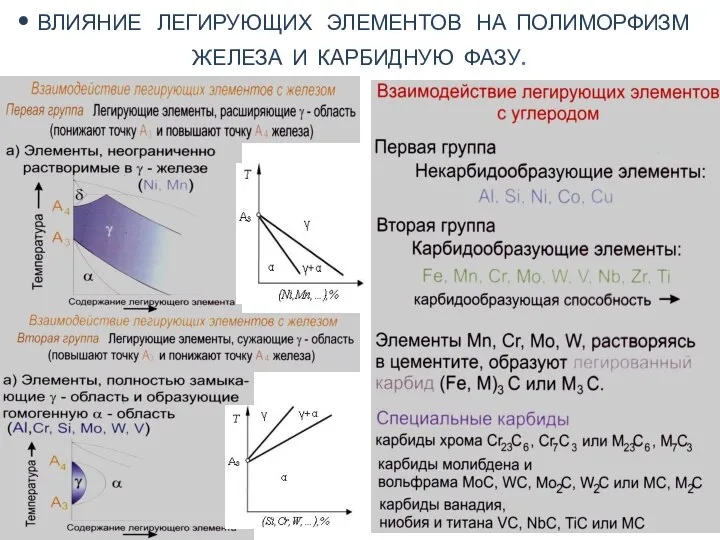 Влияние легирующих элементов на полиморфизм железа и карбидную фазу
Влияние легирующих элементов на полиморфизм железа и карбидную фазу Проектная деятельность школьников в процессе обучения химии
Проектная деятельность школьников в процессе обучения химии Dzeramā ūdens sagatavošanas shēma
Dzeramā ūdens sagatavošanas shēma Сульфаниламидные препараты. (Тема 5)
Сульфаниламидные препараты. (Тема 5) Презентация по Химии "«Кристаллические решетки»" - скачать смотреть
Презентация по Химии "«Кристаллические решетки»" - скачать смотреть  Щелочные металлы
Щелочные металлы Коррозия металлов
Коррозия металлов Хром. Роль хрома в организме человека
Хром. Роль хрома в организме человека  Аминокислоты. Номенклатура аминокислот
Аминокислоты. Номенклатура аминокислот Сложные эфиры. Жиры. Мыло
Сложные эфиры. Жиры. Мыло Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть
Презентация по Химии "Химия. Щелочные металлы" - скачать смотреть  Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.
Типы изомерии 1.Историческая справка 2.Изомерия. Изомеры. 3.Типы изомерии. Классификация изомеров.  Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Хімічний склад синтетичних миючих засобів та їх основні нормативно-технічні показники
Хімічний склад синтетичних миючих засобів та їх основні нормативно-технічні показники Свойства серной кислоты и солей
Свойства серной кислоты и солей Кислоты: состав, строение, классификация
Кислоты: состав, строение, классификация Системный анализ и моделирование процессов. Горение паро-газо-воздушного облака
Системный анализ и моделирование процессов. Горение паро-газо-воздушного облака