Содержание
- 2. Признаки объектов коллоидной химии Коллоидную химию иногда называют физикохимией дисперсных систем
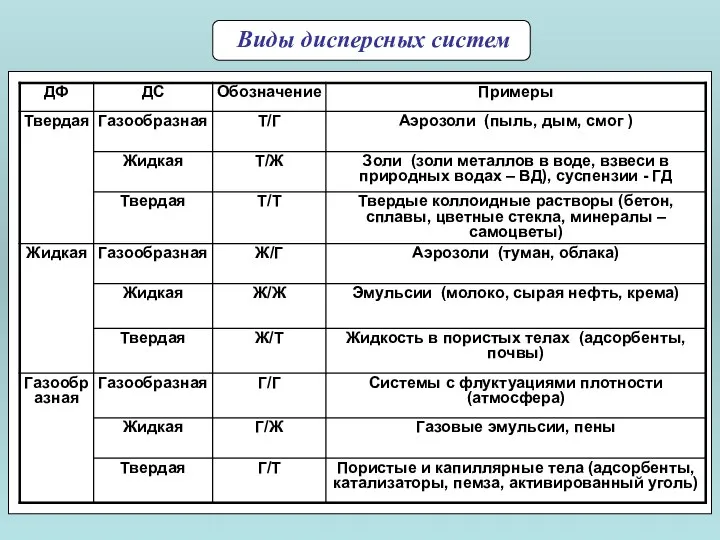
- 3. Виды дисперсных систем
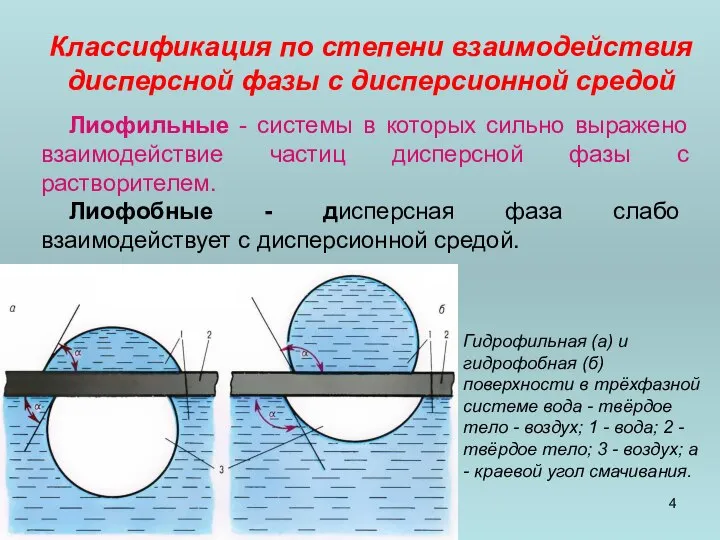
- 4. Классификация по степени взаимодействия дисперсной фазы с дисперсионной средой Лиофильные - системы в которых сильно выражено
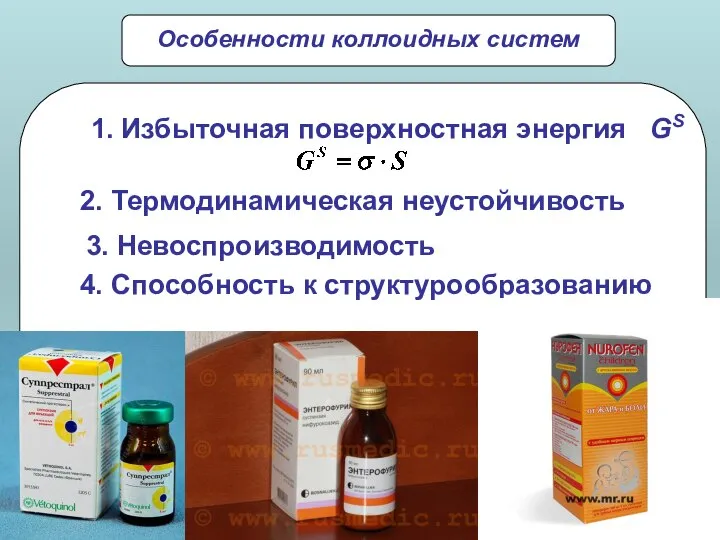
- 5. Особенности коллоидных систем 2. Термодинамическая неустойчивость 3. Невоспроизводимость 4. Способность к структурообразованию
- 6. Получение дисперсных систем -измельчение крупных образцов вещества до частиц дисперсных размеров;
- 7. Позволяют достигать более тонкого измельчения Коллоидные мельницы
- 8. ИНТЕНСИФИКАЦИЯ ПРОЦЕССОВ ДИСПЕРГИРОВАНИЯ ВВЕДЕНИЕМ ПОВЕРХНОСТНО-АКТИВНЫХ ВЕЩЕСТВ И ИОНОВ ЭЛЕКТРОЛИТОВ ИСПОЛЬЗУЕТСЯ, ТАКЖЕ, ДЛЯ ПОЛУЧЕНИЯ БОЛЕЕ УСТОЙЧИВЫХ ДИСПЕРСНЫХ
- 9. основаны на ассоциации молекул в агрегаты из истинных растворов; используют для получения высокодисперсных систем; не требуют
- 10. Стадии конденсации 2. Рост зародышей. 3. Формирование слоя стабилизатора (ДЭС).
- 11. Физические конденсационные методы
- 12. СТРОЕНИЕ КОЛЛОИДНОЙ МИЦЕЛЛЫ Согласно общепринятой мицеллярной теории золь состоит из 2-х частей: Мицелла – структурная коллоидная
- 13. СТРОЕНИЕ КОЛЛОИДНОЙ МИЦЕЛЛЫ Строение мицеллы может быть рассмотрено лишь в первом приближении, т.к. она не имеет
- 14. Некоторая часть противоионов адсорбируется на поверхности ядра, образуя т.н. адсорбционный слой противоионов; ядро вместе с адсорбированными
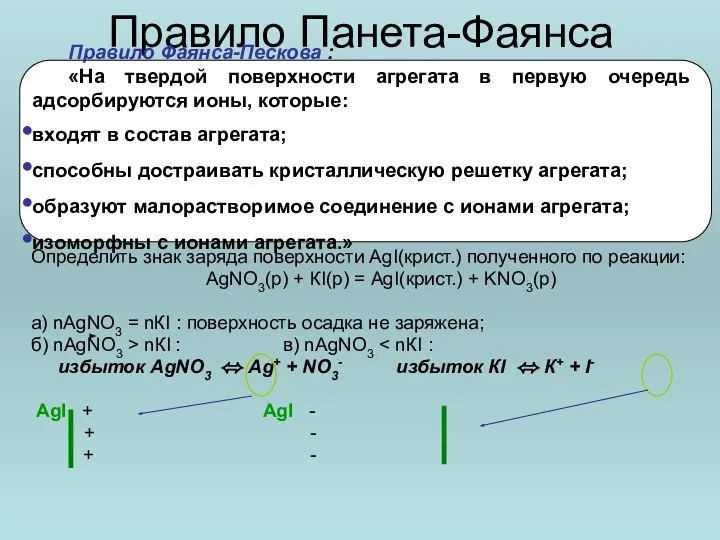
- 15. Правило Панета-Фаянса Определить знак заряда поверхности AgI(крист.) полученного по реакции: АgNО3(р) + КI(р) = АgI(крист.) +
- 16. Химические конденсационные методы
- 17. {[mFe4[Fe(CN)6]3·n[Fe(CN)6]4-]4n-·4 (n-х)K+}4x-·4xK+ {[m Fe4[Fe(CN)6]3·nFe3+] 3n+·3(n-х)Сl-}3x+·3xCl-
- 19. 3. Реакции окисления Образование золя серы. 2H2Sр-р + O2 = 2S ↓+ 2H2O Строение мицеллы:
- 20. 4. Реакции гидролиза Получение золя гидроксида железа. FeCl3 + 3H2O = Fe(OH)3 ↓ + 3HCl Cтроение
- 21. Метод пептизации
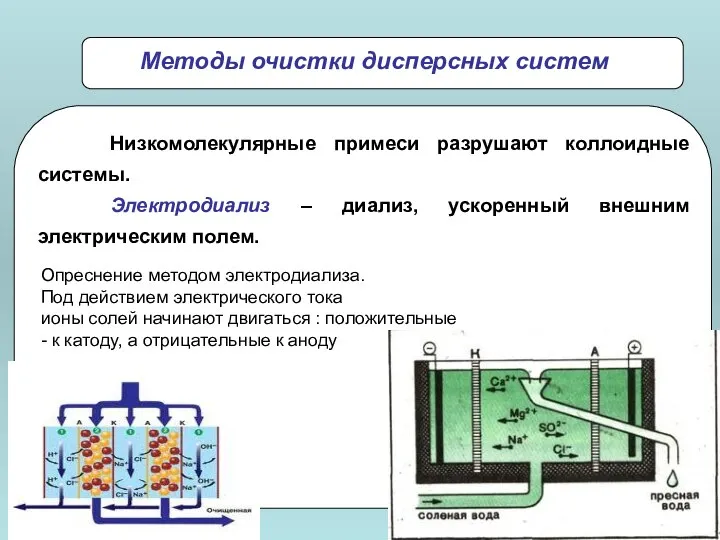
- 22. Низкомолекулярные примеси разрушают коллоидные системы. Диализ – отделение золей от низкомолекулярных примесей с помощью полупроницаемой мембраны.
- 23. Опреснение методом электродиализа. Под действием электрического тока ионы солей начинают двигаться : положительные - к катоду,
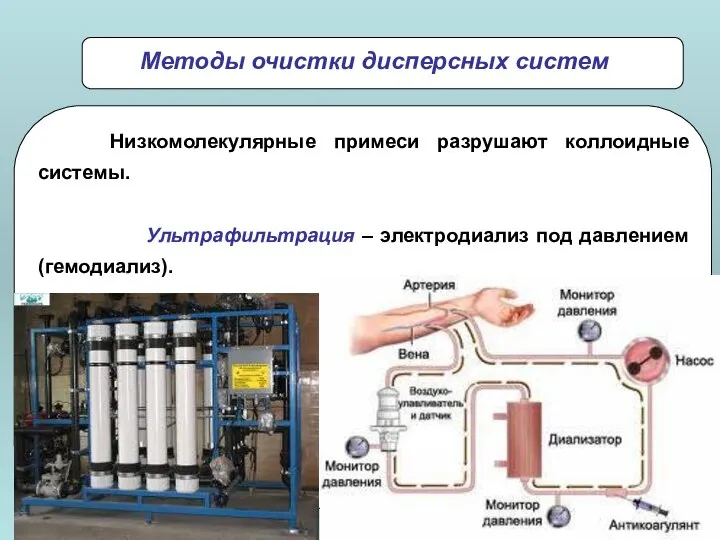
- 24. Низкомолекулярные примеси разрушают коллоидные системы. Ультрафильтрация – электродиализ под давлением (гемодиализ). Методы очистки дисперсных систем
- 25. Молекулярно-кинетические свойства дисперсных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
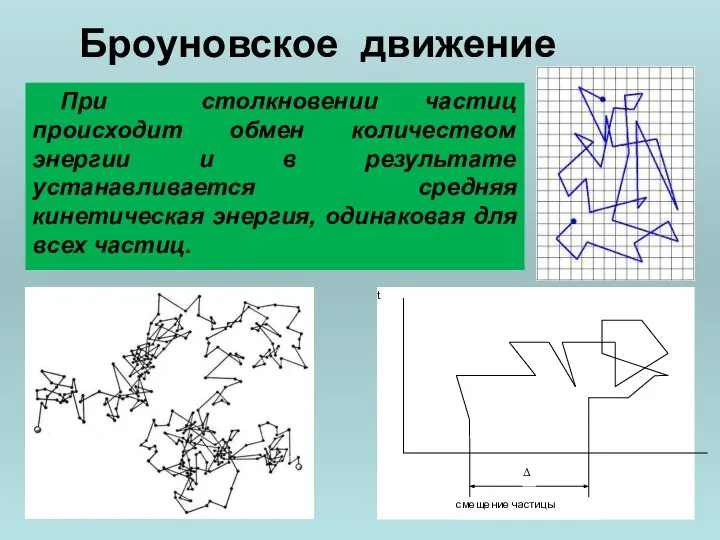
- 26. Броуновское движение Коллоидные частицы по молекулярно-кинетическим свойствам принципиально не отличаются от истинных растворов. Взвешенные в растворе
- 27. Броуновское движение При столкновении частиц происходит обмен количеством энергии и в результате устанавливается средняя кинетическая энергия,
- 28. Диффузия Диффузия – самопроизвольный процесс выравнивания концентрации частиц по всему объему раствора или газа под влиянием
- 29. Осмотическое давление Осмотическое давление в коллоидных системах составляет очень малую величину, трудно воспроизводимую в опытах. Осмотическое
- 30. Седиментация Седиментацией (от лат. sedimentum – осадок) называют процесс оседания частиц дисперсной фазы в жидкой или
- 31. Седиментационный анализ Для проведения седиментационного анализа кинетически устойчивых систем с целью определения размеров и массы их
- 32. Ультрацентрифуги Современные ультрацентрифуги дают возможность получить центробежную силу, превышающую ускорение силы тяжести в 105 раз. Современная
- 33. Оптические свойства дисперсных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
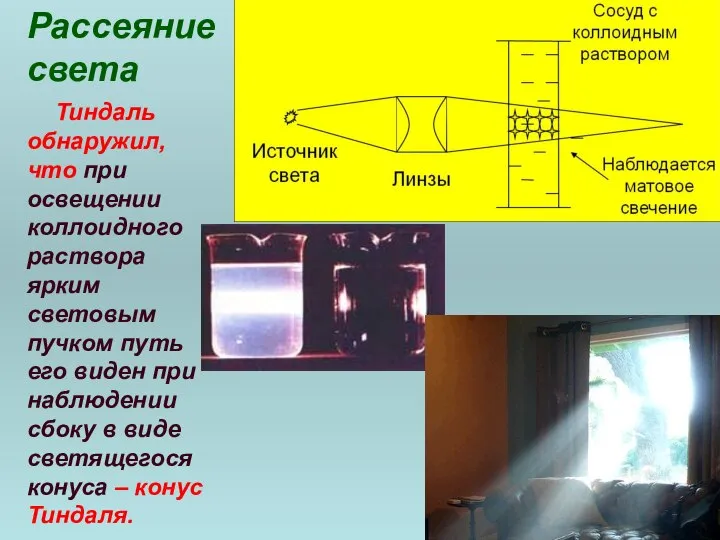
- 34. Рассеяние света Это наиболее характерное оптическое свойство для коллоидных систем. Свет рассеивается во всех направлениях. Это
- 35. Рассеяние света Тиндаль обнаружил, что при освещении коллоидного раствора ярким световым пучком путь его виден при
- 36. Электрические свойства дисперсных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
- 37. ДЭС. Образование двойного электрического слоя Существование ДЭС ионов и скачка потенциала на границе раздела двух фаз
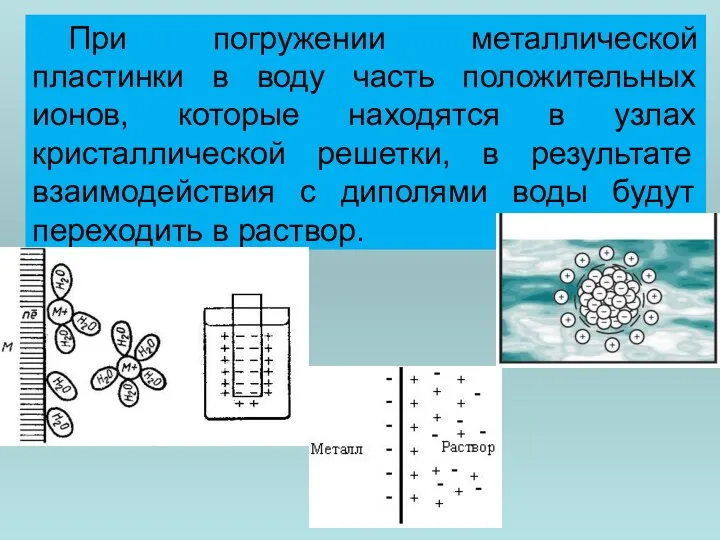
- 38. При погружении металлической пластинки в воду часть положительных ионов, которые находятся в узлах кристаллической решетки, в
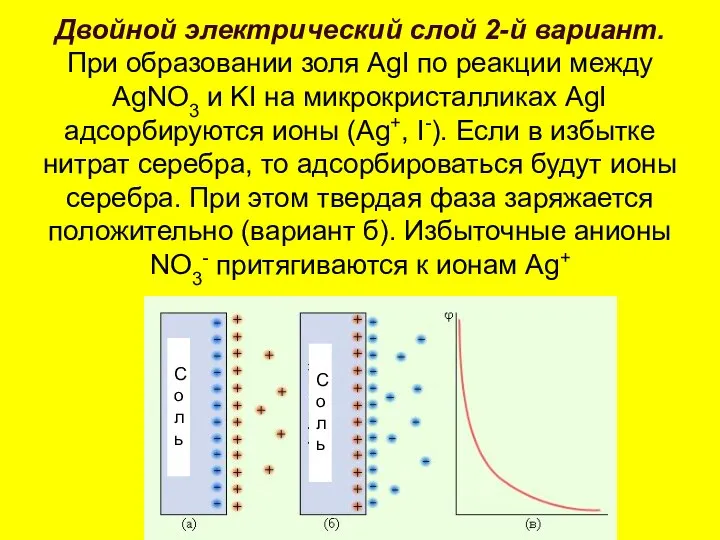
- 39. Двойной электрический слой 2-й вариант. При образовании золя AgI по реакции между AgNO3 и KI на
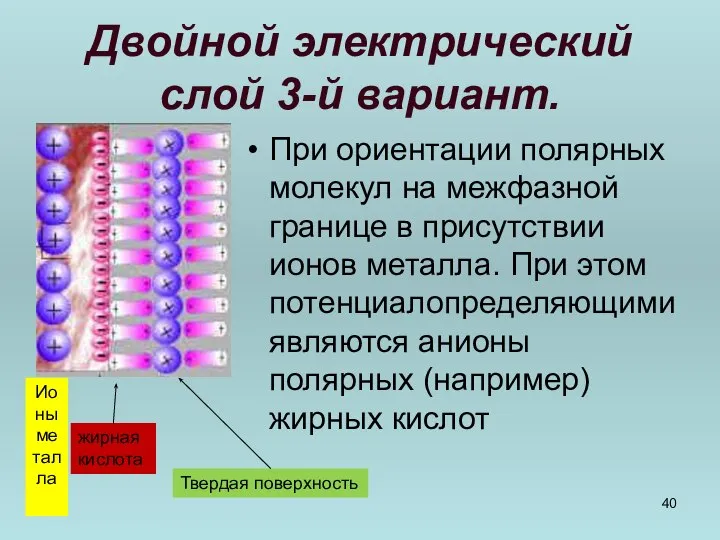
- 40. Двойной электрический слой 3-й вариант. При ориентации полярных молекул на межфазной границе в присутствии ионов металла.
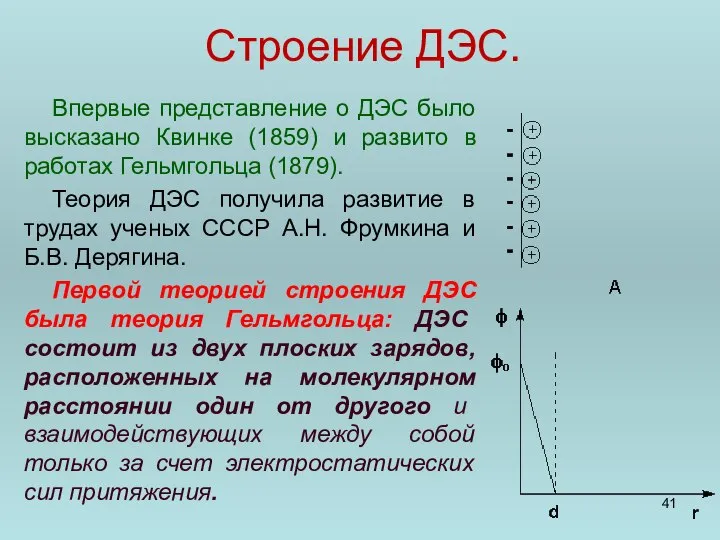
- 41. Строение ДЭС. Впервые представление о ДЭС было высказано Квинке (1859) и развито в работах Гельмгольца (1879).
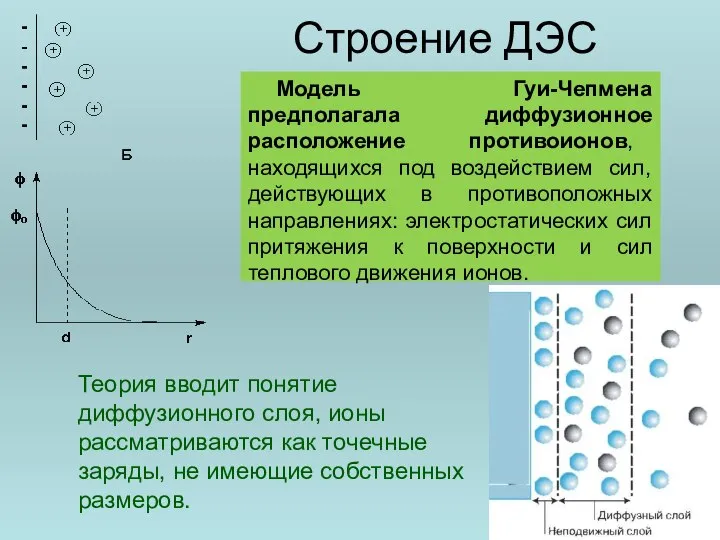
- 42. Строение ДЭС Модель Гуи-Чепмена предполагала диффузионное расположение противоионов, находящихся под воздействием сил, действующих в противоположных направлениях:
- 43. Строение ДЭС По современным представлениям (теория Штерна) строение ДЭС: ионы входящие в состав твердой фазы, образуют
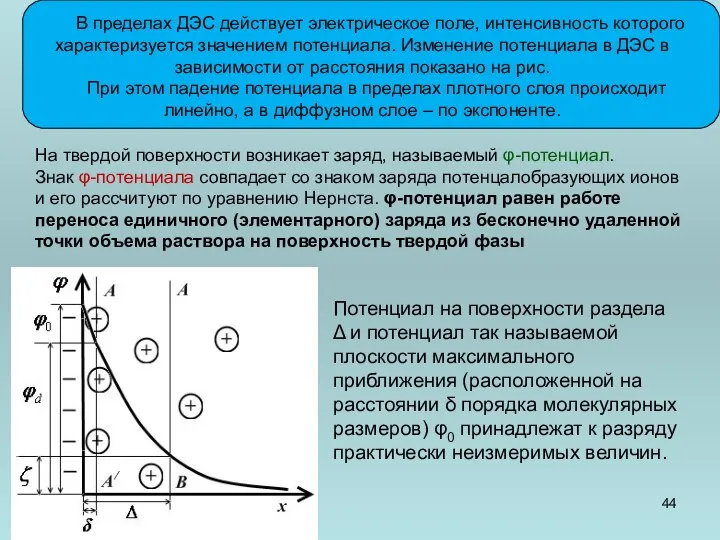
- 44. В пределах ДЭС действует электрическое поле, интенсивность которого характеризуется значением потенциала. Изменение потенциала в ДЭС в
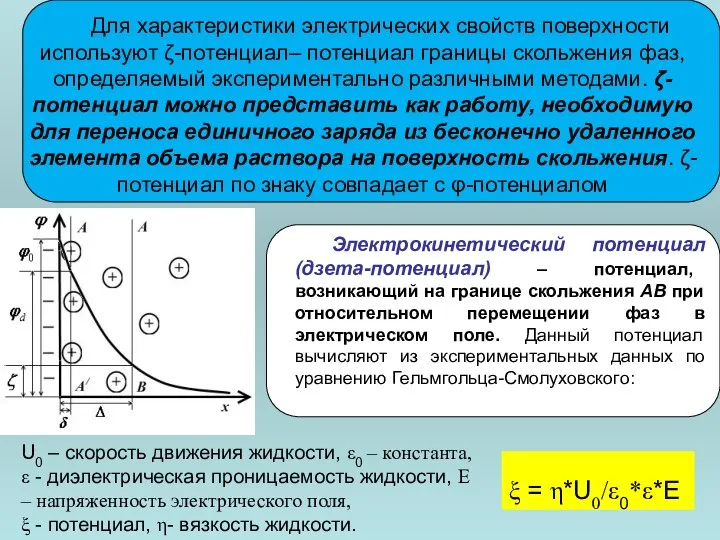
- 45. Для характеристики электрических свойств поверхности используют ζ-потенциал– потенциал границы скольжения фаз, определяемый экспериментально различными методами. ζ-потенциал
- 46. Электрокинетические явления. Классификация. Электрокинетические явления 1-го рода – относительное перемещение фаз под действием разности потенциалов Электрокинетические
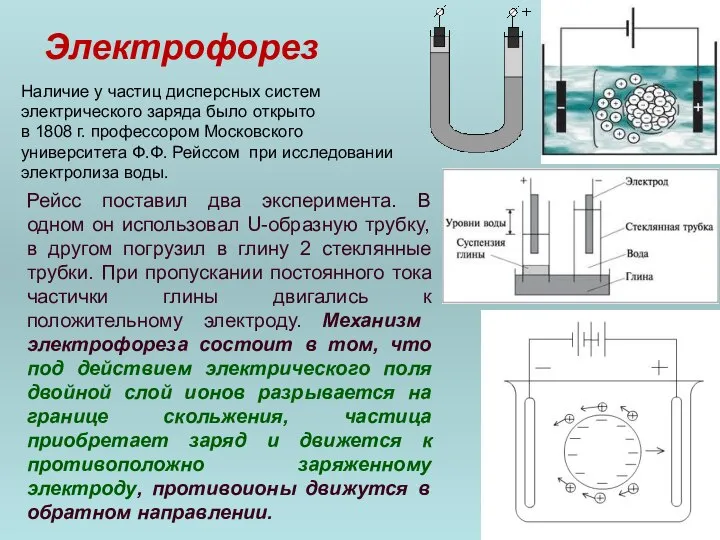
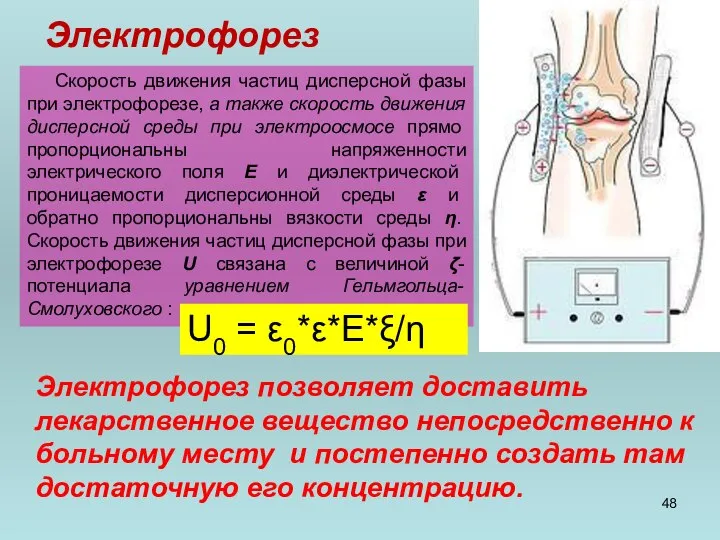
- 47. Электрофорез Наличие у частиц дисперсных систем электрического заряда было открыто в 1808 г. профессором Московского университета
- 48. Электрофорез Скорость движения частиц дисперсной фазы при электрофорезе, а также скорость движения дисперсной среды при электроосмосе
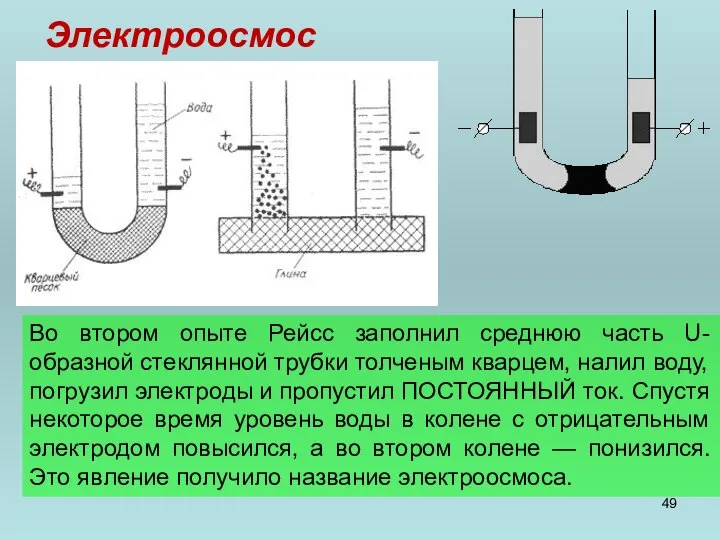
- 49. Электроосмос Во втором опыте Рейсс заполнил среднюю часть U- образной стеклянной трубки толченым кварцем, налил воду,
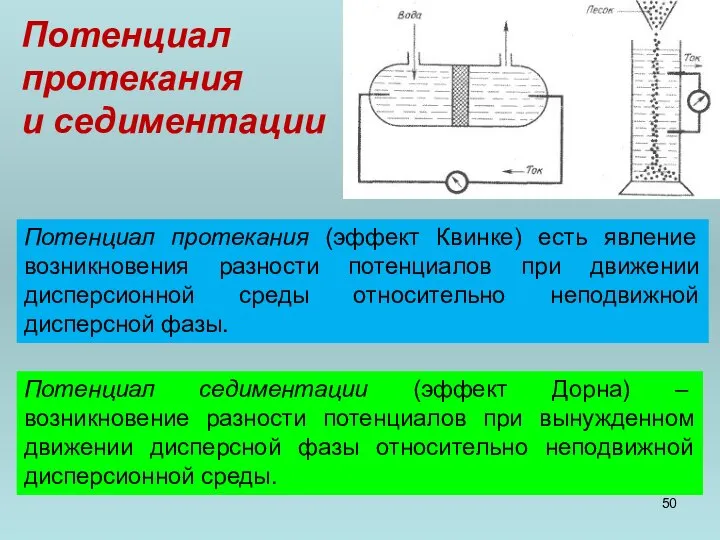
- 50. Потенциал протекания и седиментации Потенциал протекания (эффект Квинке) есть явление возникновения разности потенциалов при движении дисперсионной
- 51. Устойчивость и коагуляция коллоидных систем Запорожский государственный медицинский университет Кафедра физической и коллоидной химии
- 52. Устойчивость дисперсных систем По предложению Н.П. Пескова (1920г) устойчивость дисперсных систем подразделяют на два вида: Кинетическая
- 53. Коагуляция процесс слипания коллоидных частиц с образованием более крупных агрегатов с последующей потерей кинетической устойчивости. может
- 54. Коагуляция золей электролитами Все электролиты при определенной концентрации могут вызвать коагуляцию золя. Правило знака заряда: коагуляцию
- 56. Скачать презентацию











![{[mFe4[Fe(CN)6]3·n[Fe(CN)6]4-]4n-·4 (n-х)K+}4x-·4xK+ {[m Fe4[Fe(CN)6]3·nFe3+] 3n+·3(n-х)Сl-}3x+·3xCl-](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1404226/slide-16.jpg)





















 Серная кислота и её соли, применение
Серная кислота и её соли, применение Штучні і синтетичні волокна
Штучні і синтетичні волокна  Основные понятия и законы химии
Основные понятия и законы химии Натрій - найважливіший представник лужних металів
Натрій - найважливіший представник лужних металів Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ»
Выполнили: обучающиеся 10 класса Плотникова А. и Вартанян О. МОУ «Новопоселеновская СОШ» Химические свойства кислот
Химические свойства кислот Нефть и способы её переработки
Нефть и способы её переработки The molecular basis of inheritance. (Chapter 16)
The molecular basis of inheritance. (Chapter 16) Презентация по Химии "Законы газового состояния вещества" - скачать смотреть
Презентация по Химии "Законы газового состояния вещества" - скачать смотреть  Попова Ольга Викторовна учитель химии ГБОУ школа 634 города Санкт-Петербург «Мониторинг продуктов питания»
Попова Ольга Викторовна учитель химии ГБОУ школа 634 города Санкт-Петербург «Мониторинг продуктов питания» Первоначальная периодическая таблица Д.И.Менделеева
Первоначальная периодическая таблица Д.И.Менделеева Уравнения химических реакций
Уравнения химических реакций Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6)
Применение закона действующих масс к окислительно-восстановительным равновесиям. (Лекция 6) Введение в биохимию. Строение и функции белков (часть 1)
Введение в биохимию. Строение и функции белков (часть 1) Металлы. XV раздел Недрагоценные металлы и изделия из них. Перемещение через таможенную границу
Металлы. XV раздел Недрагоценные металлы и изделия из них. Перемещение через таможенную границу Резина и каучук
Резина и каучук Хлор и его соединения
Хлор и его соединения Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7)
Регуляция активности ферментов. Множественные формы ферментов. Введение в клиническую энзимологию. (Лекция 7) Комплексные соединения
Комплексные соединения Електричний струм у газах та його використання
Електричний струм у газах та його використання ЦУКОР
ЦУКОР  Обзор свойств неметаллов.. Окислительно-восстановительные свойства типичных неметаллов
Обзор свойств неметаллов.. Окислительно-восстановительные свойства типичных неметаллов Аттестационная работа. Программа элективного курса Химия в задачах
Аттестационная работа. Программа элективного курса Химия в задачах Химический элемент цинк
Химический элемент цинк Гидролиз солей
Гидролиз солей Крахмал. Строение вещества
Крахмал. Строение вещества Формирование химического состава, структуры и свойств поверхностных слоев систем Ме-С при ионно-лучевых воздействиях
Формирование химического состава, структуры и свойств поверхностных слоев систем Ме-С при ионно-лучевых воздействиях Презентация по Химии "Определение геометрических размеров молекул изомеров октана" - скачать смотреть
Презентация по Химии "Определение геометрических размеров молекул изомеров октана" - скачать смотреть