Содержание
- 2. Введение Особое историческое значение квантовой механики определяется тем, что она радикально преобразовала систему химического знания, подняла
- 3. Квантовая химия - это область современной химии, в которой принципы и понятия квантовой механики и статистической
- 4. Основные понятия и объекты химии Атом - наименьшая частица химического элемента, являющаяся носителем его свойств. Химический
- 5. Химическая связь - это та связь между атомами, которая приводит к образованию молекул
- 6. Два основных типа химических связей Ионная связь образуется за счет переноса электронов с одного атома на
- 7. Металлическая связь Она реализуется за счет большой концентрации в кристаллах свободных электронов («электронный газ»), которые удерживают
- 8. Основная задача квантовой химии Решение уравнение Шредингера и его релятивистского варианта (уравнение Дирака) для атомов и
- 9. Приближения, используемые в квантовой химии
- 10. Приближение Борна — Оппенгеймера движение электронов и движение ядер разделено (ядра движутся настолько медленно, что при
- 11. Одноэлектронное приближение считается, что движение электрона не зависит от движения других электронов системы. В связи с
- 12. Приближение МО ЛКАО в данном подходе волновая функция молекулы представляется как сумма атомных орбиталей с коэффициентами.
- 13. Межмолекулярное взаимодействие - это электромагнитное взаимодействие электронов и ядер одной молекулы с электронами и ядрами другой
- 14. Заключение В последние десятилетия квантовые подходы в химии позволили решить еще более сложные задачи, прежде всего
- 16. Скачать презентацию













 Обмен триацилглицеролов и жирных кислот
Обмен триацилглицеролов и жирных кислот Различные способы решения задач на смеси, сплавы, растворы
Различные способы решения задач на смеси, сплавы, растворы Природные источники углеводородов
Природные источники углеводородов Презентацию выполнил ученик 8 класса «В» ЦО 1428. Пугачёв Александр 2009.
Презентацию выполнил ученик 8 класса «В» ЦО 1428. Пугачёв Александр 2009.  Лабораторная посуда и оборудование
Лабораторная посуда и оборудование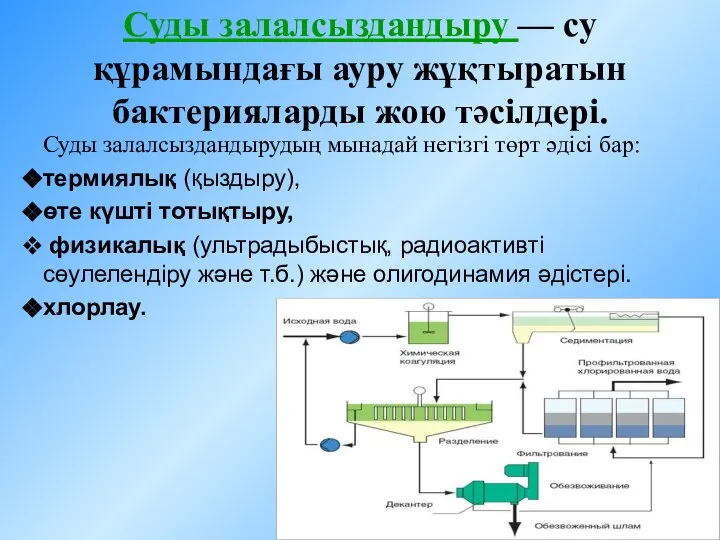 Суды залалсыздандыру - су құрамындағы ауру жұқтыратын бактерияларды жою тәсілдері
Суды залалсыздандыру - су құрамындағы ауру жұқтыратын бактерияларды жою тәсілдері Спирты, они же – алкоголи. В средние века люди считали этиловый спирт одним из сильнейших лекарственных средств и поэтому назвали
Спирты, они же – алкоголи. В средние века люди считали этиловый спирт одним из сильнейших лекарственных средств и поэтому назвали  Теория химического строения Бутлерова. Второе положение теории Бутлерова. Изомерия. Структурная изомерия
Теория химического строения Бутлерова. Второе положение теории Бутлерова. Изомерия. Структурная изомерия Производные пролина (каптоприл, эналаприл) и фенилаланина (мелфалан). Требования к качеству и методы анализа
Производные пролина (каптоприл, эналаприл) и фенилаланина (мелфалан). Требования к качеству и методы анализа Каучук. Строение и применение
Каучук. Строение и применение Область применения карбоновых кислот
Область применения карбоновых кислот Обмен белков, жиров и углеводов
Обмен белков, жиров и углеводов Материя и цвет. Свет
Материя и цвет. Свет Высокомолекулярные соединения полимеры
Высокомолекулярные соединения полимеры Неорганические полимеры
Неорганические полимеры Индикаторы на кухне
Индикаторы на кухне Галогены. Способы получения, применение
Галогены. Способы получения, применение Строение сплавов
Строение сплавов Углеводы (10 класс) - Презентация по Химии_
Углеводы (10 класс) - Презентация по Химии_ Маслянокислые бактерии
Маслянокислые бактерии Обмен липидов. (Часть 1)
Обмен липидов. (Часть 1) Органічні розчинники. 11 клас
Органічні розчинники. 11 клас Классификации в аналитической химии
Классификации в аналитической химии Адсорбционные взаимодействия
Адсорбционные взаимодействия Химическая связь в твердых телах. Классификация твердых тел по типу химической связи
Химическая связь в твердых телах. Классификация твердых тел по типу химической связи Дәрілік препараттардың синтезі мен олардың классификациясы
Дәрілік препараттардың синтезі мен олардың классификациясы Основы коррозии и защиты металлов
Основы коррозии и защиты металлов Матчворк Підготувала учениця 11-А класу Шведюк Людмила
Матчворк Підготувала учениця 11-А класу Шведюк Людмила