Содержание
- 2. Учебники Цирельсон В.Г. Квантовая химия. Молекулы, молекулярные системы и твердые тела "БИНОМ. Лаборатория знаний" 2012. –
- 3. Рейтинг курса Экзамен – 40 баллов (20 б. – миним. к допуску) Практические работы – 30
- 4. Основные понятия Квантовая механика – т. раздел физики, описывающий движение и свойства микрочастиц (электронов, атомов, молекул).
- 5. Возникновение атомной физики V-IV в до н. э – Демокрит, Левкипп: понятие неделимой частицы (впоследствии «атом»)
- 6. Радиоактивность 1896 г. Антуан Анри Беккерель – для солей урана Радиоактивность – самопроизвольное превращение неустойчивых ядер
- 7. Изотопы (U, Th, Ac) 1899 - 1907г. Эрнест Резерфорд, Фредерик Содди Изотопы – разновидности одного и
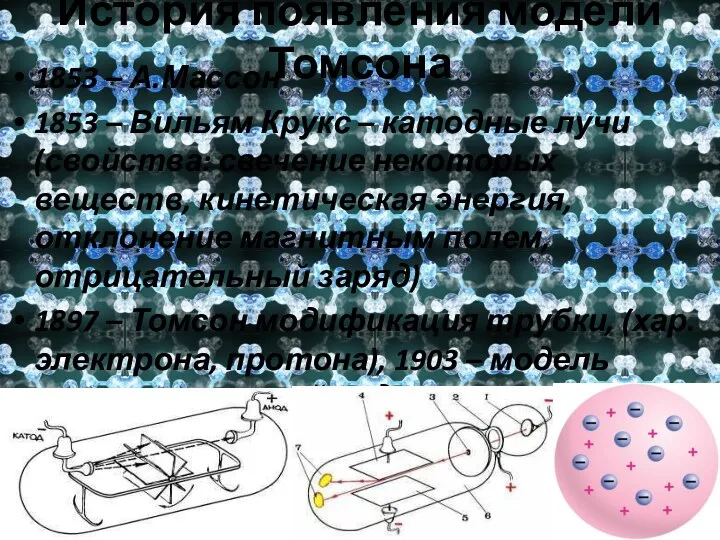
- 8. История появления модели Томсона 1853 – А.Массон 1853 – Вильям Крукс – катодные лучи (свойства: свечение
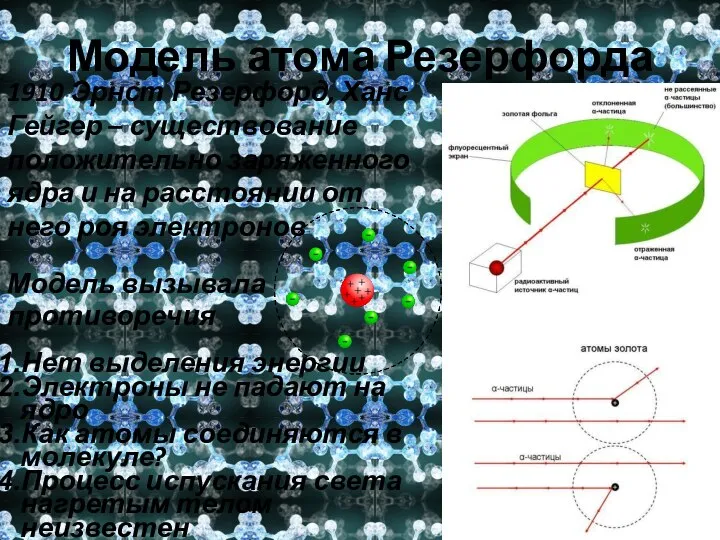
- 9. Модель атома Резерфорда 1910 Эрнст Резерфорд, Ханс Гейгер – существование положительно заряженного ядра и на расстоянии
- 10. Квантовая модель атома Бора 1913 – Нильс Бор на основе двух постулатов: В атоме существует несколько
- 11. Предпосылки квантовой теории атома 1910 г. Макс Планк связал элементарный квант (порцию света) с частотой электромагнитной
- 12. Квантовая модель атома Бора Уровни – электронные орбиты Подуровни составляют уровень Орбитали составляют подуровень Расположение электронов
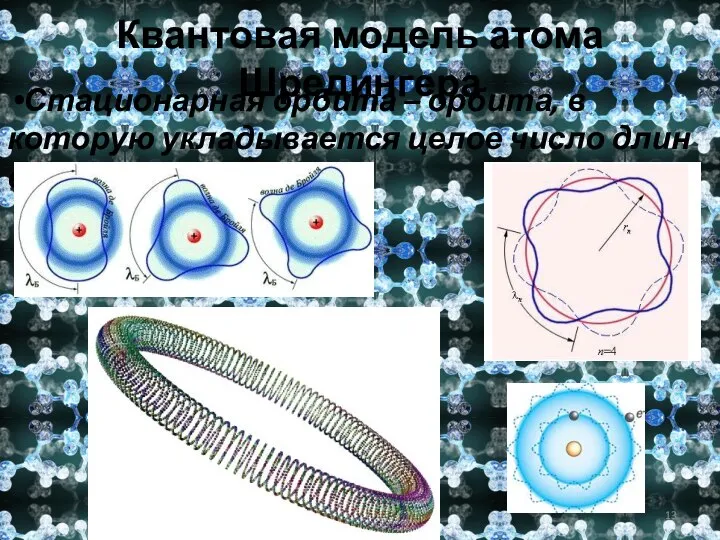
- 13. Квантовая модель атома Шредингера Стационарная орбита – орбита, в которую укладывается целое число длин волн электрона
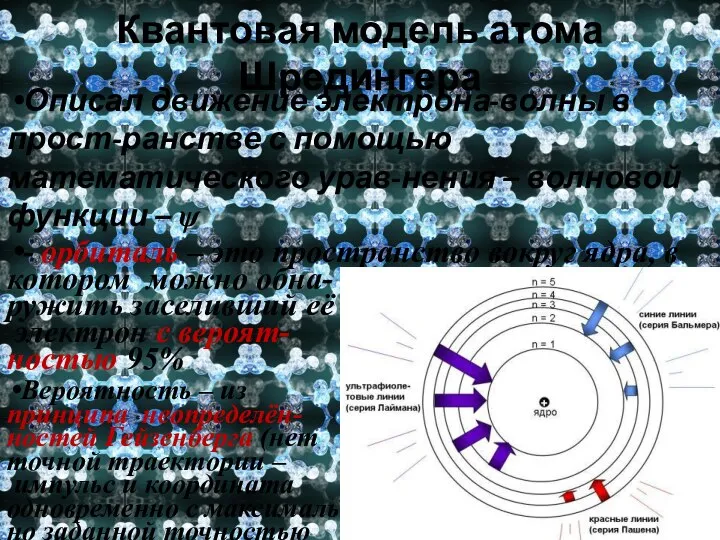
- 14. Квантовая модель атома Шредингера Описал движение электрона-волны в прост-ранстве с помощью математического урав-нения – волновой функции
- 15. Квантовая модель атома Шредингера Существование уровней, орбиталей различной формы
- 17. Скачать презентацию










 Скорость реакции и температура. (Лекция 10)
Скорость реакции и температура. (Лекция 10) Химия биогенных элементов
Химия биогенных элементов Химические элементы в быту
Химические элементы в быту Углеводороды. Структура и функции биолекул
Углеводороды. Структура и функции биолекул Полисилоксаны. Классификация полимеров
Полисилоксаны. Классификация полимеров Методы познания химии
Методы познания химии Высокомолекулярные соединения (ВМС) или полимеры
Высокомолекулярные соединения (ВМС) или полимеры Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения: Используя оксид ртути (II) напишит
Используя оксид ртути (II) напишите уравнения реакций при которых возможны следующие превращения: Используя оксид ртути (II) напишит Ювелирное дело. Империя самоцветов
Ювелирное дело. Империя самоцветов Алкандар. (қаныққан көмірсутектер. Парафиндер.)
Алкандар. (қаныққан көмірсутектер. Парафиндер.) Определение подлинности лекарственных веществ
Определение подлинности лекарственных веществ Пестициды. Применение пестицидов
Пестициды. Применение пестицидов Строение твердого вещества
Строение твердого вещества Золото. Свойство золота
Золото. Свойство золота Сверхразветвленные полимеры: типы, получение, применение
Сверхразветвленные полимеры: типы, получение, применение Арены. Бензол
Арены. Бензол В гостях у Хозяйки Медной горы. Покровская сельская библиотека
В гостях у Хозяйки Медной горы. Покровская сельская библиотека Рождающий воду
Рождающий воду Химическая связь
Химическая связь Газообразные вещества
Газообразные вещества Ртуть. Нахождение в природе. Применение
Ртуть. Нахождение в природе. Применение Изомерия комплексных соединений
Изомерия комплексных соединений Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Вспомогательные вещества. Флюсы и их применение. Кислоты, соли, щёлочи применяемые в ювелирном деле. (Лекция 3)
Вспомогательные вещества. Флюсы и их применение. Кислоты, соли, щёлочи применяемые в ювелирном деле. (Лекция 3) Производство синтетических моющих средств
Производство синтетических моющих средств Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду
Поверхностно-активные вещества (ПАВ). Классификация ПАВ по степени влияния на окружающую среду Твердофазное восстановление металлов и образование карбидов из хромовых концентратов Аганозерского месторождения
Твердофазное восстановление металлов и образование карбидов из хромовых концентратов Аганозерского месторождения Простейшие операции с веществом (химический практикум)
Простейшие операции с веществом (химический практикум)