Содержание
- 2. Проверка ДЗ
- 3. С имеет массу 12 а.е.м. Давайте посчитаем, какая масса у Н и О в а.е.м. Мн=
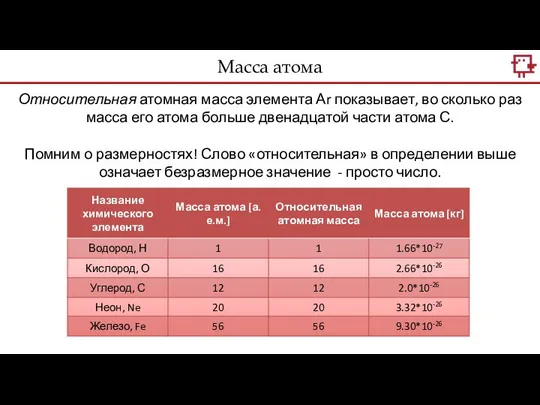
- 4. Относительная атомная масса элемента Аr показывает, во сколько раз масса его атома больше двенадцатой части атома
- 5. 2H2 + O2 = 2H2O Массы водорода и кислорода должны относиться как 1:8 для задействование всего
- 6. H2O Эта формула означает, что на 1 атом кислорода приходится 2 атома кислорода. Относительная атомная масса
- 7. Получается, что в каких пропорциях ни возьми H и О образуется вода (Н2О). А значит химический
- 9. Скачать презентацию
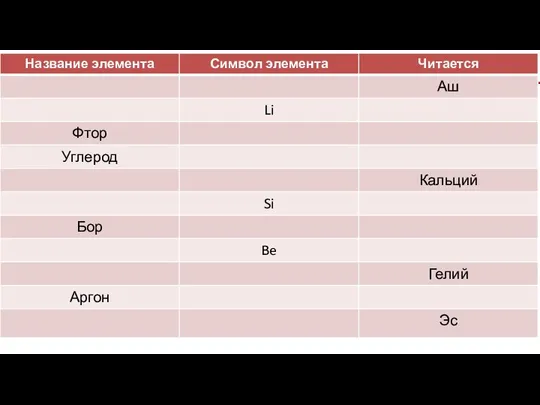




 Смоги и их влияние на человека
Смоги и их влияние на человека Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно
Презентация по Химии "Патофизиология аритмий сердца ПАТОФИЗИОЛОГИЯ АРИТМИЙ СЕРДЦА" - скачать смотреть бесплатно Введение в геологию и минералогию
Введение в геологию и минералогию Подготовка воды к количественному химическому анализу. Количественное определение азота, аммиака, нитритов, нитратов
Подготовка воды к количественному химическому анализу. Количественное определение азота, аммиака, нитритов, нитратов Проект по химии. Минералы на нашей коже
Проект по химии. Минералы на нашей коже Органические вещества клетки. Углеводы и липиды
Органические вещества клетки. Углеводы и липиды Аминокислоты. Белки. Пептиды
Аминокислоты. Белки. Пептиды Подкласс Иносиликаты (цепочечные/ленточные силикаты)
Подкласс Иносиликаты (цепочечные/ленточные силикаты) Химия переходных элементов IV – V группы
Химия переходных элементов IV – V группы Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія
Пластмаси, синтетичні каучуки Підготували учениці 11-б класу Оренбургська Марина та Козаренко Таїсія  Тема урока ОСНОВАНИЯ
Тема урока ОСНОВАНИЯ Галогены. Химические свойства галогенов
Галогены. Химические свойства галогенов Изотопная геохимия. U-Pb метод
Изотопная геохимия. U-Pb метод Алканы. Определение. Общая формула класса углеводородов
Алканы. Определение. Общая формула класса углеводородов Синтез в неводных средах
Синтез в неводных средах Презентация по Химии "Химия и сельское хозяйство. Пестициды" - скачать смотреть
Презентация по Химии "Химия и сельское хозяйство. Пестициды" - скачать смотреть  Электролиз
Электролиз Радикальная полимеризация (Лекция 5)
Радикальная полимеризация (Лекция 5) Основы составления балансов
Основы составления балансов Изучение растворимости веществ. Приготовление растворов и анализ состава растворов путем выпаривания
Изучение растворимости веществ. Приготовление растворов и анализ состава растворов путем выпаривания Арбузный снег. Предположения
Арбузный снег. Предположения Презентация по Химии "Изотопы" - скачать смотреть
Презентация по Химии "Изотопы" - скачать смотреть  Кислоты. Определение, состав, классификация, номенклатура
Кислоты. Определение, состав, классификация, номенклатура Оксид серы IV. Сернистая кислота
Оксид серы IV. Сернистая кислота Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9
Карбон қышқылдар, түрлері қасиеттері, түындылары. Лекция № 8. Гетерофункционалды қосылыстар. Лекция № 9 Atomic number, Mass number and Isotopes
Atomic number, Mass number and Isotopes Нефть и газ. Выполнила Кириллова Анастасия.
Нефть и газ. Выполнила Кириллова Анастасия.  Гидрокрекинг нефтяного сырья
Гидрокрекинг нефтяного сырья