Методические рекомендации по подготовке учащихся к выполнению заданий повышенного и высокого уровней сложности ЕГЭ по химии
Содержание
- 2. Демоверсия КИМ ЕГЭ 2018 г. по химии www.fipi.ru Структура части 1 варианта принципиально не изменилась. Задания,
- 3. Тематический блок «Неорганическая химия» Задание 5. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
- 4. Задание 6. Характерные химические свойства простых веществ (металлов и неметаллов). Характерные химические свойства оксидов: оснóвных,амфотерных, кислотных.
- 5. Задание 6. Характерные химические свойства простых веществ (металлов и неметаллов). Характерные химические свойства оксидов: оснóвных,амфотерных, кислотных.
- 6. Задание 7. Характерные химические свойства оснований, амфотерных гидроксидов, кислот, солей: средних, кислых, оснóвных; комплексных (на примере
- 7. Задание 8. Характерные химические свойства неорганических веществ (4512) Тематический блок «Неорганическая химия»
- 8. Задание 9. Характерные химические свойства неорганических веществ Пример 1 Тематический блок «Неорганическая химия»
- 9. Задание 9. Характерные химические свойства неорганических веществ Пример 2 Тематический блок «Неорганическая химия»
- 10. Задание 10. Взаимосвязь неорганических веществ Тематический блок «Неорганическая химия»
- 11. Задания 30 и 31. Реакции окислительно-восстановительные. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты.
- 12. Критерии оценивания задания 30
- 13. Задание 30 Содержание условий заданий с развернутым ответом во многих случаях может ориентировать экзаменуемых на использование
- 14. Важнейшие окислители: O2, Cl2, Br2, HNO3, H2SO4(конц.), KMnO4, MnO2, K2Cr2O7, K2CrO4, KClO, KClO3, H2O2, (соединения Fe(III))
- 15. Подготовка к выполнению задания 30 Важнейшие окислители: азотная кислота
- 16. Подготовка к выполнению задания 30 Важнейшие окислители Азотная кислота – примеры реакций:
- 17. Подготовка к выполнению задания 30 Важнейшие окислители: концентрированная серная кислота При использовании сильных восстановителей (активных металлов,
- 18. Подготовка к выполнению задания 30 Перманганат калия и оксид марганца(IV) 2KMnO4 + 3KNO2 + H2O =
- 19. Хроматы и дихроматы чаще используют в кислой среде, восстановление протекает до соединений Cr(III): При использовании кислородсодержащих
- 20. Важнейшие восстановители и продукты их окисления Cложные вещества, содержащие атом в низшей степени окисления: HI, KI,
- 21. Сложные вещества, содержащие катионы металлов, заряд которых может возрасти, например, Fe2+, соединения меди(I), соединения хрома(III): 2Cr(OH)3
- 22. K2Cr2O7 + KBr + H2SO4 → Cr2(SO4)3 + Br2 + … 2Cr+6 + 6ē → 2Cr+3
- 23. Такие обозначения степеней окисления как N5+ и N4+ (сначала цифра, затем знак) считаются неверными. Исключение: у
- 24. Оценка: 1 балл, верно составлено уравнение реакции, запись электронного баланса содержит ошибку Пример 3 Задание выполнено
- 25. Задание 31
- 26. Ионные уравнения реакций отражают суть тех изменений, которые происходят при взаимодействии веществ − электролитов. . Реакции
- 27. Если в качестве одного из исходных веществ выбрана соль, то она должна быть растворима в воде
- 28. Реакции образования гидроксокомплексов при взаимодействии растворов щелочей и растворимых солей цинка и алюминия также можно отнести
- 29. Оценка: 1 балл Пример 10 Задание 31
- 30. Пример заданий 30 и 31 Для выполнения заданий 30, 31 используйте следующий перечень веществ: нитрат аммония,
- 31. Задание 32 Хлорид алюминия нагрели с калием. Полученный в результате металл поместили в раствор гидроксида калия.
- 32. Задание 32 Доля выпускников, получивших определенное количество баллов
- 33. Элементы содержания, проверяемые заданием 32 (см. кодификатор):
- 34. Необходимо проявить умение составлять уравнения реакций, соответствующих всем типам взаимодействия неорганических веществ: кислотно-основное взаимодействие; реакции ионного
- 35. ЗАДАЧИ Оксид цинка массой 16,2 г нагрели в присутствии угарного газа объёмом 1,12 л (н.у.). При
- 36. При нагревании образца гидрокарбоната натрия часть вещества разложилась. При этом выделилось 4,48 л газа (н.у.) и
- 37. 2. Смешали 58,8 г 20 %-ного раствора бромида аммония и 328 г 5 %-ного раствора дигидрофосфата
- 38. Рекомендации по подготовке обучающихся к государственной итоговой аттестации в форме ЕГЭ Успешность выполнения заданий во многом
- 39. Рекомендуемые учебные пособия
- 40. «Я сдам ЕГЭ! Курс самоподготовки» Пособие содержит весь необходимый теоретический и фактологический материал, изучение которого является
- 41. «Я сдам ЕГЭ! Курс самоподготовки»
- 42. «Я сдам ЕГЭ! Курс самоподготовки»
- 43. «Я сдам ЕГЭ! Курс самоподготовки»
- 44. «Я сдам ЕГЭ! Курс самоподготовки»
- 45. Пособие «Я сдам ЕГЭ!»
- 46. «Я сдам ЕГЭ! Курс самоподготовки»
- 47. Пособие «Я сдам ЕГЭ!»
- 48. Пособие «Я сдам ЕГЭ!» Тематическое планирование курса:
- 49. Пособие «Я сдам ЕГЭ!»
- 50. Пособие «Я сдам ЕГЭ!»
- 51. Пособие «Я сдам ЕГЭ!»
- 52. Пособие «Я сдам ЕГЭ!»
- 53. «Я сдам ЕГЭ! Типовые задания» К заданиям для самопроверки приведены ответы и приведены подробные решения. Предложена
- 54. Тренировочные задания
- 55. Тренировочные задания
- 56. Тренировочные задания
- 57. Задания для самопроверки
- 58. Задания для самопроверки
- 59. Задания для самопроверки
- 60. Задания для самопроверки
- 61. Ответы и решения
- 62. Ответы и решения
- 63. Ответы и решения
- 64. Другие рекомендуемые пособия: 1. Каверина А.А., Молчанова Г.Н., Свириденкова Н.В., Стаханова С.В. Химия. Решение заданий повышенного
- 66. Скачать презентацию































































 Органическая химия
Органическая химия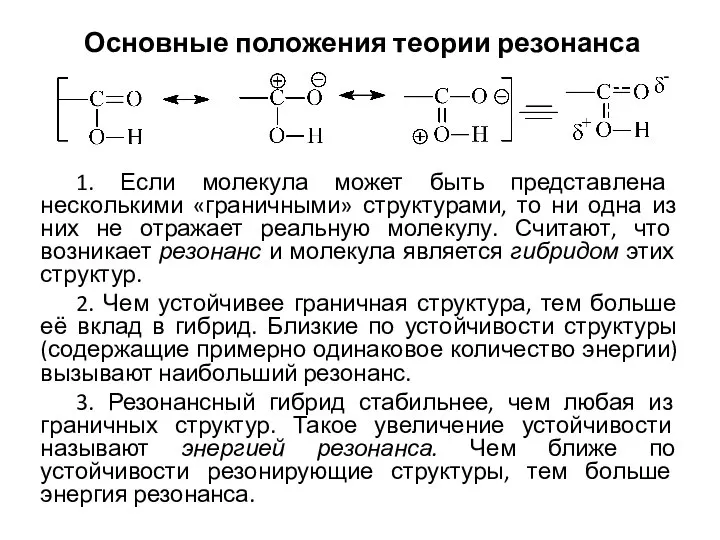 Основные положения теории резонанса
Основные положения теории резонанса Дисперсные системы. Способы получения и очистки коллоидных систем. (Лекция 5)
Дисперсные системы. Способы получения и очистки коллоидных систем. (Лекция 5) Презентация по химии тема: «Химия в жизни общества» выполняли ученики 1
Презентация по химии тема: «Химия в жизни общества» выполняли ученики 1 Презентация по Химии "Соли, их состав и названия" - скачать смотреть
Презентация по Химии "Соли, их состав и названия" - скачать смотреть  Общие свойства металлов
Общие свойства металлов Cтроение и спектры молекул
Cтроение и спектры молекул Антибиотики как ЛС
Антибиотики как ЛС Мінеральні добрива
Мінеральні добрива Химия элементов VIA группы. SO2
Химия элементов VIA группы. SO2 Коррозия металлов в контакте
Коррозия металлов в контакте Личная жизнь и научная деятельность Михаила Васильевича Ломоносова Работу выполнил: ученик 8-го «А» класса лицея № 1571 г.Москвы Ани
Личная жизнь и научная деятельность Михаила Васильевича Ломоносова Работу выполнил: ученик 8-го «А» класса лицея № 1571 г.Москвы Ани Полиэтилентерефталат. Свойства. Получение
Полиэтилентерефталат. Свойства. Получение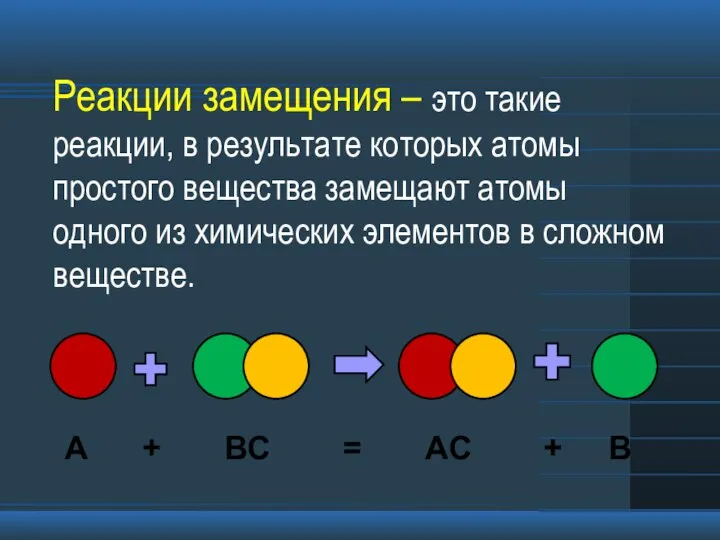 Реакции замещения
Реакции замещения ОЗОНОВАЯ ДЫРА
ОЗОНОВАЯ ДЫРА  Виды присадок к моторным топливам
Виды присадок к моторным топливам Бионеорганическая химия. Комплексообразование в организме. (Лекция 3)
Бионеорганическая химия. Комплексообразование в организме. (Лекция 3) Карбоновые кислоты
Карбоновые кислоты Очистка поверхности медного сплава
Очистка поверхности медного сплава Взаимосвязь неорганических веществ
Взаимосвязь неорганических веществ Физические и химические явления Учитель химии «Чажемтовской СОШ» Косова Е.М.
Физические и химические явления Учитель химии «Чажемтовской СОШ» Косова Е.М. Твердість води Мета: ознайомлення з поняттям “твердість води”, вивчення видів твердості води та методів її усунення
Твердість води Мета: ознайомлення з поняттям “твердість води”, вивчення видів твердості води та методів її усунення  Натуральный каучук
Натуральный каучук Кислоты Начальные сведения
Кислоты Начальные сведения Типы и механизмы органических реакций
Типы и механизмы органических реакций Классификация металлов
Классификация металлов Альдегидная функциональная группа
Альдегидная функциональная группа Alkynes
Alkynes