Содержание
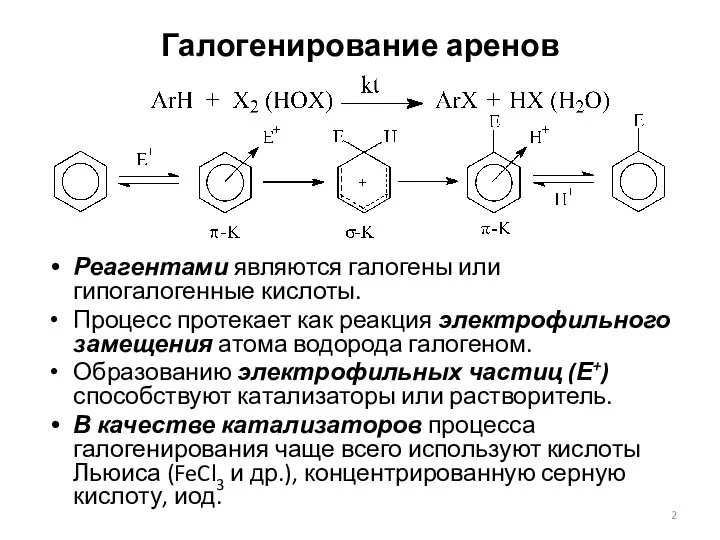
- 2. Галогенирование аренов Реагентами являются галогены или гипогалогенные кислоты. Процесс протекает как реакция электрофильного замещения атома водорода
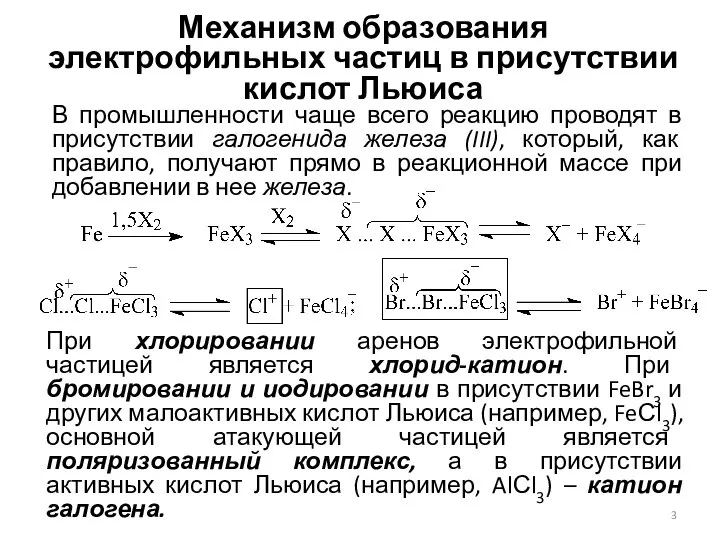
- 3. Механизм образования электрофильных частиц в присутствии кислот Льюиса В промышленности чаще всего реакцию проводят в присутствии
- 4. Механизм образования электрофильных частиц в присутствии H2SO4 и I2 Катализ серной кислотой: Катализ иодом: арены хлорируются
- 5. Каталитическое влияние растворителя В связи с этим галогенирование активных субстратов (ароматических аминов, фенолов, полиалкилбензолов типа мезитилена,
- 6. Направление и скорость реакции галогенирования аренов а также выход целевого продукта зависят от (см.лекции): строения субстрата
- 7. Влияние строения субстрата (устойчивости σ-комплекса) и кислотности среды В реакциях SE скорость уменьшается: фуран > нафталин
- 8. Активность электрофильной частицы - очень зависит от галогена и катализатора. Природа галогена настолько сильно влияет, что
- 9. Влияние технологических факторов Удачный подбор катализатора может обеспечить не только высокую скорость, но и селективность процесса.
- 10. Технология хлорирования аренов в безводной среде Подготовка хлора – обезвоживание (H2SO4). Подготовка жидкого сырья - обезвоживание
- 11. Технология бромирования аренов Подготовка брома – используют товарный бром или после перегонки Подготовка субстрата (арена) –
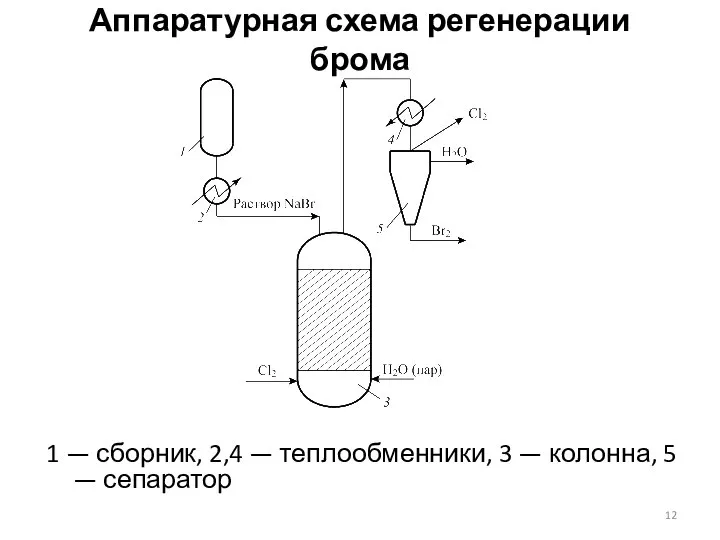
- 12. Аппаратурная схема регенерации брома 1 — сборник, 2,4 — теплообменники, 3 — колонна, 5 — сепаратор
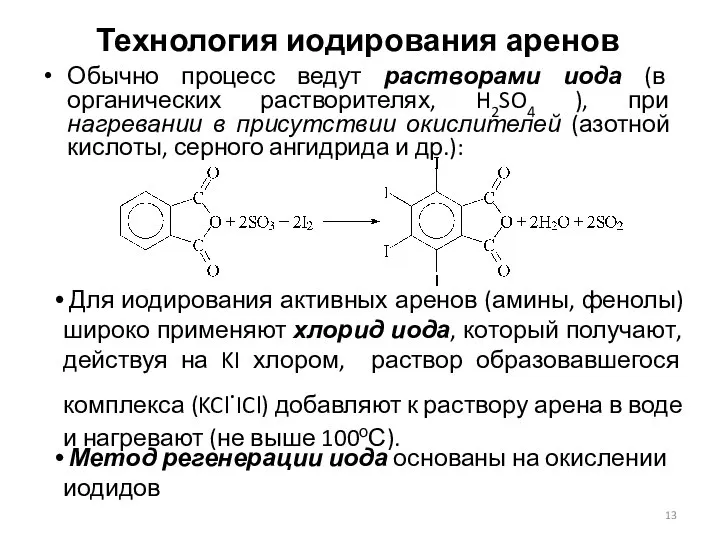
- 13. Технология иодирования аренов Обычно процесс ведут растворами иода (в органических растворителях, H2SO4 ), при нагревании в
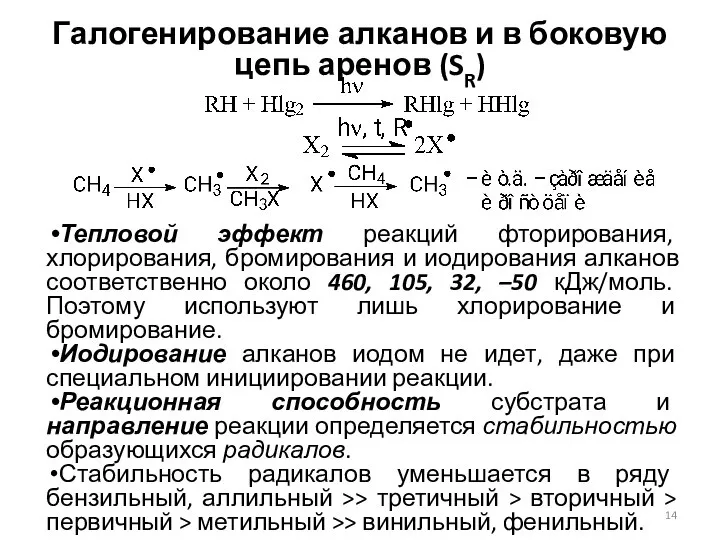
- 14. Галогенирование алканов и в боковую цепь аренов (SR) Тепловой эффект реакций фторирования, хлорирования, бромирования и иодирования
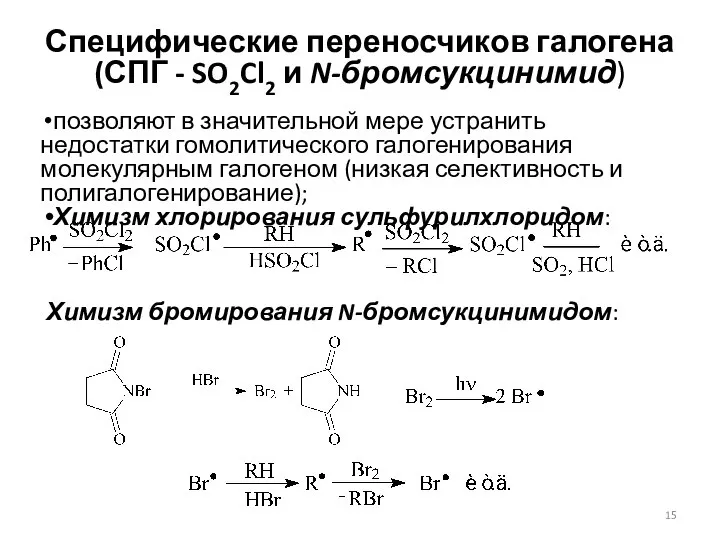
- 15. Специфические переносчиков галогена (СПГ - SO2Cl2 и N-бромсукцинимид) позволяют в значительной мере устранить недостатки гомолитического галогенирования
- 16. Особенности технологии гомолитического галогенирования Гомолитическое галогенирование идет в газовой и в жидкой фазе. При этом необходимо
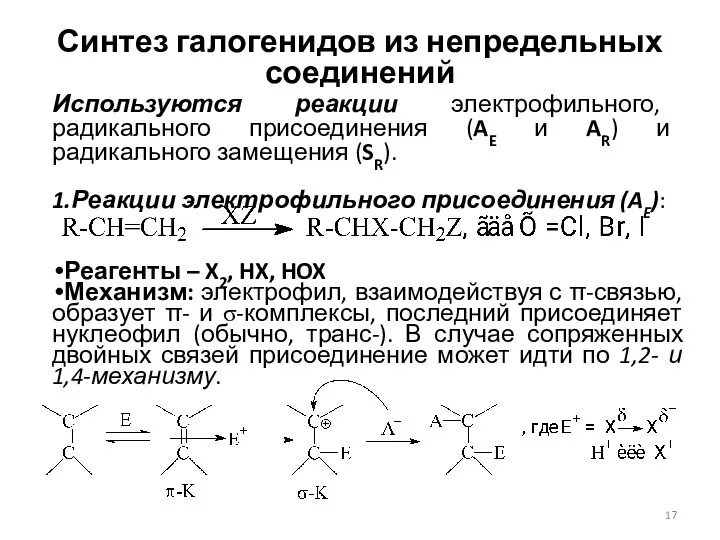
- 17. Синтез галогенидов из непредельных соединений Реагенты – X2, HX, HOX Механизм: электрофил, взаимодействуя с π-связью, образует
- 18. Присоединение галогена по π-связям электрофилом (Е+) является поляризованная молекула галогена. реакционная способность увеличивается в ряду: F2
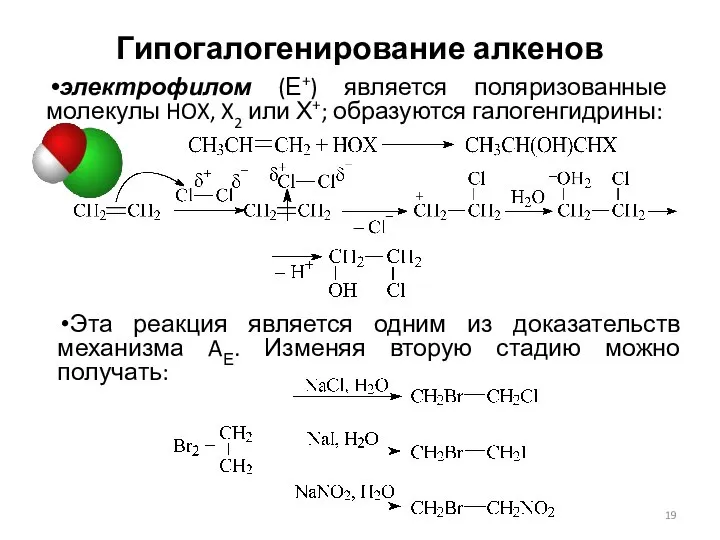
- 19. Гипогалогенирование алкенов электрофилом (Е+) является поляризованные молекулы HOX, X2 или Х+; образуются галогенгидрины: Эта реакция является
- 20. Реакционная способность субстрата и направление реакции - в наибольшей степени зависят от стабильности катиона (σ-комплекса), которая
- 21. 2.Гомолитическое присоединение (AR) галогенов и галогеноводорода - Идет при соответствующем инициировании (свет, нагрев, пероксиды) протекает по
- 22. Гетеролитическое галогенирование алифатических альдегидов и кетонов - Галогенирование альдегидов и кетонов (кроме фторирования) в присутствии кислот
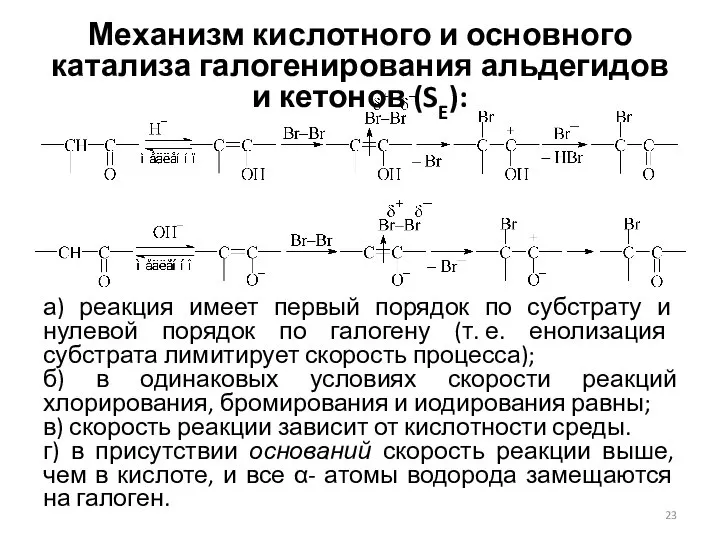
- 23. Механизм кислотного и основного катализа галогенирования альдегидов и кетонов (SE): а) реакция имеет первый порядок по
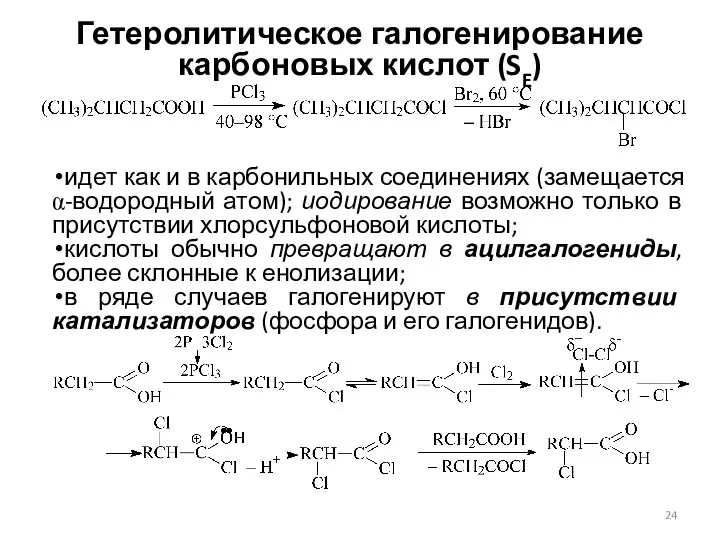
- 24. Гетеролитическое галогенирование карбоновых кислот (SE) идет как и в карбонильных соединениях (замещается α-водородный атом); иодирование возможно
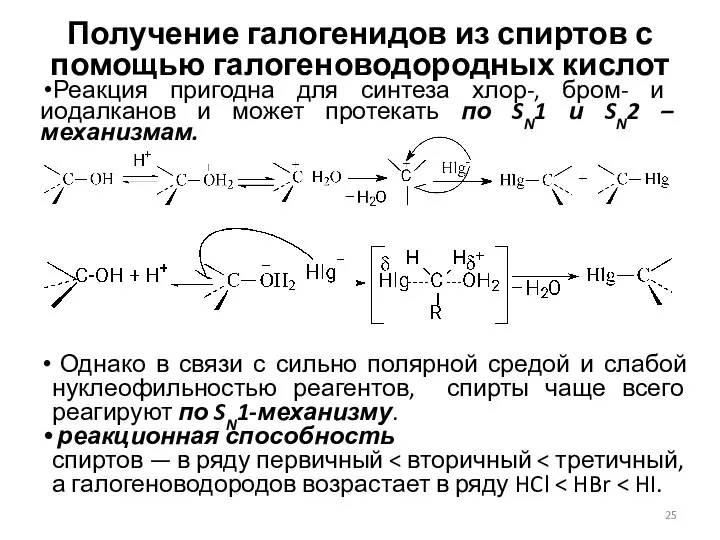
- 25. Получение галогенидов из спиртов с помощью галогеноводородных кислот Реакция пригодна для синтеза хлор-, бром- и иодалканов
- 26. Реакция спиртов с галогеноводородами С избытком концентрированного раствора HI легко реагируют все спирты, с бромоводородной кислотой
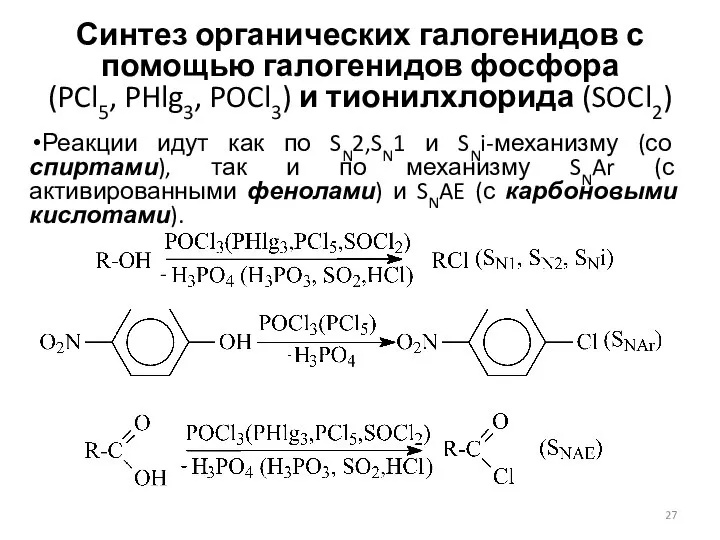
- 27. Синтез органических галогенидов с помощью галогенидов фосфора (PCl5, PHlg3, POCl3) и тионилхлорида (SOCl2) Реакции идут как
- 28. Синтез органических галогенидов с помощью PCl5, PHlg3, POCl3 Во всех случаях гидроксил предварительно ацилируется с образованием
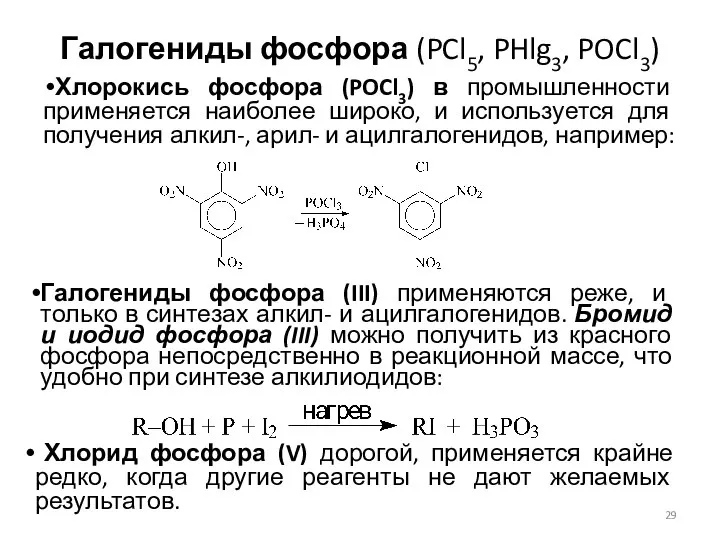
- 29. Галогениды фосфора (PCl5, PHlg3, POCl3) Хлорокись фосфора (POCl3) в промышленности применяется наиболее широко, и используется для
- 31. Скачать презентацию















 Глюкоза Презентацію виконали учениці 11-Б класу Христинівської спеціалізованої школи І – ІІІ ступенів № 1 ім. О. Є. Корнійчука В
Глюкоза Презентацію виконали учениці 11-Б класу Христинівської спеціалізованої школи І – ІІІ ступенів № 1 ім. О. Є. Корнійчука В Аминокислоты ароматического ряда и их производные
Аминокислоты ароматического ряда и их производные Кинетика сложных реакций
Кинетика сложных реакций Морфология почв. (Лекция 7)
Морфология почв. (Лекция 7) Кислород Общая характеристика, получение и свойства
Кислород Общая характеристика, получение и свойства Презентация по Химии "Задания на соответствие" - скачать смотреть
Презентация по Химии "Задания на соответствие" - скачать смотреть  Алюминий, его физические и химические свойства
Алюминий, его физические и химические свойства Основные характеристики ковалентной связи
Основные характеристики ковалентной связи Классификация кислот, химические свойства кислот
Классификация кислот, химические свойства кислот Свойства морской воды
Свойства морской воды Химия элементов - неметаллов Сера Автор: Цуркан Лилия Фёдоровна учитель химии МОУ « ТСШ № 17» г. Тирасполь
Химия элементов - неметаллов Сера Автор: Цуркан Лилия Фёдоровна учитель химии МОУ « ТСШ № 17» г. Тирасполь Натуральний каучук Підготувала учениця 11-Б класу ЗОШ І-ІІІст. №11 Відняк Людмила
Натуральний каучук Підготувала учениця 11-Б класу ЗОШ І-ІІІст. №11 Відняк Людмила  Хімічний склад і використання мінералів
Хімічний склад і використання мінералів Предмет химии. Вещества и их физические свойства
Предмет химии. Вещества и их физические свойства Диссоциация кислот, щелочей и солей (9 класс)
Диссоциация кислот, щелочей и солей (9 класс) Адсорбция. Поглощение газов или паров из газовых смесей или растворов твердым веществом
Адсорбция. Поглощение газов или паров из газовых смесей или растворов твердым веществом Классификация магматических пород
Классификация магматических пород Пример практического тура. Всероссийская олимпиада школьников по химии
Пример практического тура. Всероссийская олимпиада школьников по химии Генетическая связь между классами органических веществ МБОУ «Арбузовская СОШ» Муравьева Н.А. – учитель химии
Генетическая связь между классами органических веществ МБОУ «Арбузовская СОШ» Муравьева Н.А. – учитель химии  Презентация по Химии "Медь и ее соединения" - скачать смотреть
Презентация по Химии "Медь и ее соединения" - скачать смотреть  Хроматографические методы анализа. Метод газовой хроматографии
Хроматографические методы анализа. Метод газовой хроматографии Атмосферный цикл соединений азота
Атмосферный цикл соединений азота Получение этилена и опыты с ним. (Практическая работа 2)
Получение этилена и опыты с ним. (Практическая работа 2) Свойства простых веществ 8 класс
Свойства простых веществ 8 класс  Презентация по Химии "Устранение дефектов при росте кристалла медного купороса" - скачать смотреть
Презентация по Химии "Устранение дефектов при росте кристалла медного купороса" - скачать смотреть  Нафта та її переробка
Нафта та її переробка  Периодическая система химических элементов Д.И.Менделеева и строение атомов. (8 класс)
Периодическая система химических элементов Д.И.Менделеева и строение атомов. (8 класс)  Ультраосновные породы щелочные и умереннощелочные
Ультраосновные породы щелочные и умереннощелочные