Содержание
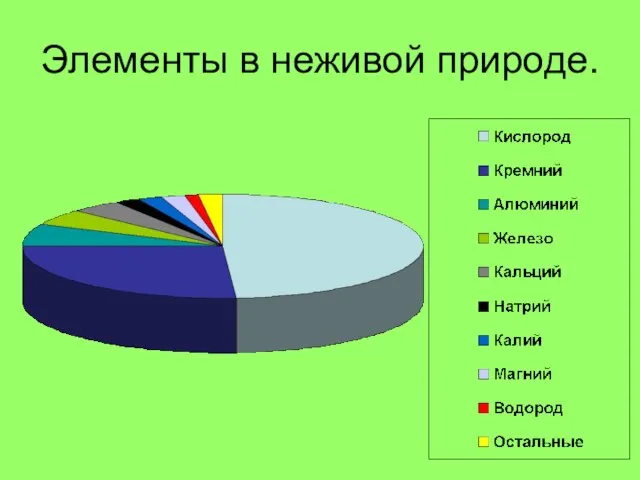
- 2. Элементы в неживой природе.
- 3. Нахождение в природе. Самородные элементы Сера Графит С Алмаз С Азот и кислород, инертные газы в
- 4. Нахождение в природе ← Апатиты Р Галит NaCl → ← FeS2 пирит Кварц SiO2 →
- 5. Неметаллы - это химические элементы, которые могут проявлять свойства как окислителя ( принимают электроны), так и
- 6. Соединения неметаллов. Оксиды – только кислотные SO3, SO2, CO2 и другие. (кроме NO и CO –безразличные)
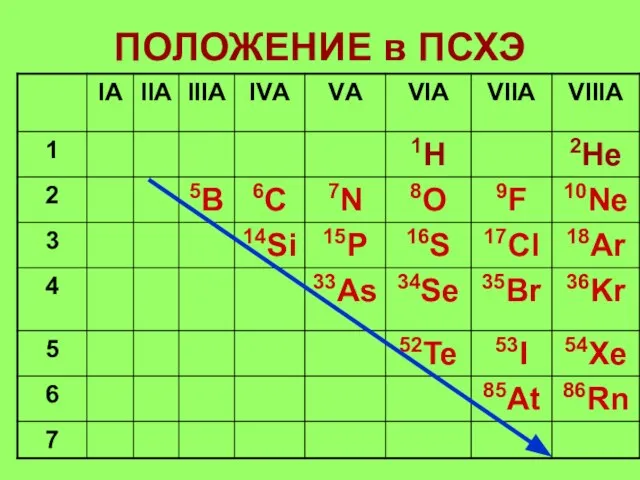
- 7. ПОЛОЖЕНИЕ в ПСХЭ
- 8. ЭЛЕМЕНТЫ - IA,IIIA,IVA Н
- 9. ХАЛЬКОГЕНЫ -VIA
- 11. ГАЛОГЕНЫ -VIIA
- 12. ИНЕРТНЫЕ ГАЗЫ-VIIIA
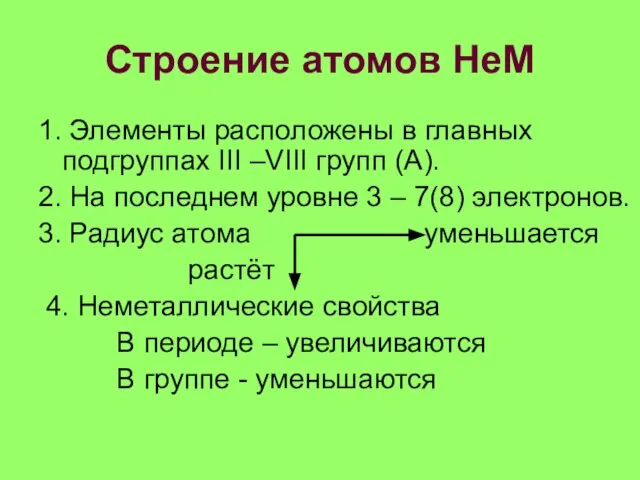
- 13. Строение атомов НеМ 1. Элементы расположены в главных подгруппах III –VIII групп (А). 2. На последнем
- 14. Строение атомов НеМ 5. Высокая электроотрицательность. 6. Принимают электроны и отдают. 7. НеМ → кислотный оксид→кислота
- 15. Физические свойства Агрегатное состояние. Газообразные – азот, кислород, хлор, инертные газы, водород. Жидкий – бром, Твёрдые
- 16. Кислород, водород – пример газообразных бесцветных неметаллов
- 17. Хлор (как и фтор) – окрашенные газообразные неметаллы. При растворении хлора в воде получается хлорная вода
- 18. Бром – жидкость красно-бурого цвета При растворении брома в воде получается бромная вода
- 19. При растворении брома в воде получается бромная вода
- 20. Большинство неметаллов имеют твёрдое агрегатное состояние Сера – кристаллическое вещество жёлтого цвета Красный фосфор Углерод (уголь)
- 21. Неметаллы малорастворимы в воде Уголь Фосфор Сера не смачивается водой
- 24. Скачать презентацию


















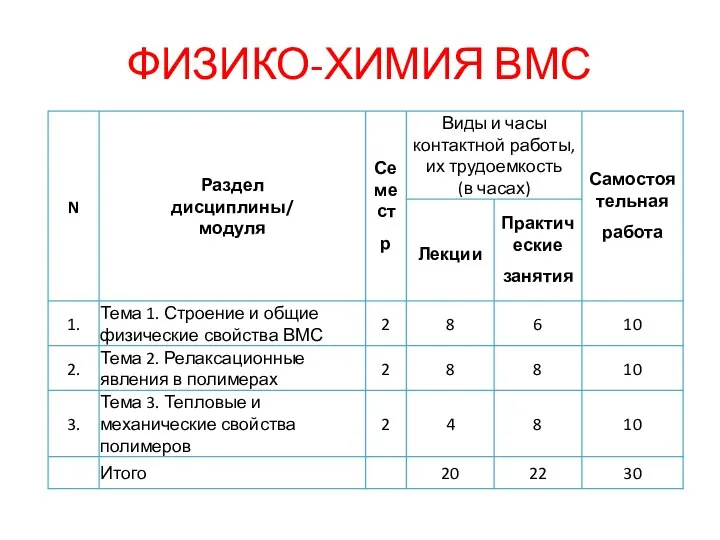 Строение и общие физические свойства ВМС. Релаксационные явления в полимерах. Тепловые и механические свойства полимеров
Строение и общие физические свойства ВМС. Релаксационные явления в полимерах. Тепловые и механические свойства полимеров Физические явления в химии. Чистые вещества и смеси
Физические явления в химии. Чистые вещества и смеси Класифікація пластмас
Класифікація пластмас  Биохимия и молекулярная биология. (Лекция 1)
Биохимия и молекулярная биология. (Лекция 1) Введение в биохимию. Биохимия белков
Введение в биохимию. Биохимия белков Абсолютное первенство по химии
Абсолютное первенство по химии Электрохимические методы анализа, часть 2. Кулонометрия. Вольтамперометрия
Электрохимические методы анализа, часть 2. Кулонометрия. Вольтамперометрия Камни и Рыбы
Камни и Рыбы Основы общей химии
Основы общей химии Химические формулы
Химические формулы Лекарственные растения, содержащие кумарины
Лекарственные растения, содержащие кумарины Задания на альдегиды и кетоны
Задания на альдегиды и кетоны Природные источники углеводородов
Природные источники углеводородов 04. Наблюдение за горящей свечой. Устройство и работа спиртовки
04. Наблюдение за горящей свечой. Устройство и работа спиртовки Хімічні методи підвищення продуктивності свердловини
Хімічні методи підвищення продуктивності свердловини Химия вокруг нас
Химия вокруг нас Некоторые аспекты физической и коллоидной химии
Некоторые аспекты физической и коллоидной химии Значение органической химии в жизни людей
Значение органической химии в жизни людей Каталитикалық риформинг
Каталитикалық риформинг Витамины алифатического ряда, пангамовая и пантотеновая кислоты. Витамины алициклического ряда, витамины А и D. (Тема 3)
Витамины алифатического ряда, пангамовая и пантотеновая кислоты. Витамины алициклического ряда, витамины А и D. (Тема 3) Разработка и исследование системы управления процессом ректификации бутанола
Разработка и исследование системы управления процессом ректификации бутанола Судың кермектілігі. Сілтілік металдар мен сілтілікжер металдардың табиғи қосылыстарының қазақстандағы кен орындары
Судың кермектілігі. Сілтілік металдар мен сілтілікжер металдардың табиғи қосылыстарының қазақстандағы кен орындары Цинк и его соединения
Цинк и его соединения Алкадиены
Алкадиены Аттестационная работа. Химия в нашей жизни
Аттестационная работа. Химия в нашей жизни Химическая связь
Химическая связь Химерні та трансгенні організми
Химерні та трансгенні організми  Презентация по Химии "Жиры животных" - скачать смотреть
Презентация по Химии "Жиры животных" - скачать смотреть