Содержание
- 2. УМК «ХИМИЯ» Тема лекции: Общие свойства металлов Лектор – Иванов М.Г.
- 3. Цель лекции: изложение основных понятий физических и химических свойств металлов в рамках современной химической теории Компетенции,
- 4. Нахождение в природы содержание Оксиды - Fe3O4, MnO2 Сульфиды - ZnS, FeS2 MnO2 SiO2 CaSO4.2H2O Соли-
- 5. содержание В свободном виде (самородки)- Au, Pt, Ag, Cu Нахождение в природы Pt Cu Au
- 8. Металлический блеск металлический блеск – электроны, заполняющие межатомное пространство отражают световые лучи, а не пропускают как
- 9. Ковкость и пластичность Механическое воздействие на кристалл с металлической решеткой вызывает только смещение слоев атомов и
- 10. Обладают тепло- и электропроводностью Хаотически движущиеся электроны под действием электрического поля приобретают направленное движение, в результате
- 11. Ртуть Вольфрам
- 12. Тантал Литий
- 13. Серебро Платина Золото
- 14. Магнитные свойства металлов Ферромагнетики – металлы способные сильно намагничиваться и долго сохранять это свойство (Fe, Co,
- 16. Сплавы металлов Сплавы - (твердые растворы) — это системы, состоящие из двух и более металлов или
- 17. Виды и свойства чугунов.
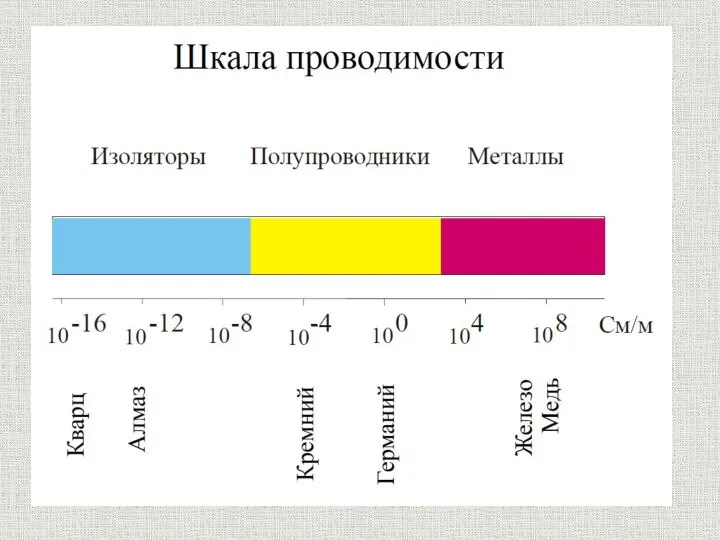
- 19. содержание Физические свойства металлов Металл Электропроводность Теплопроводность
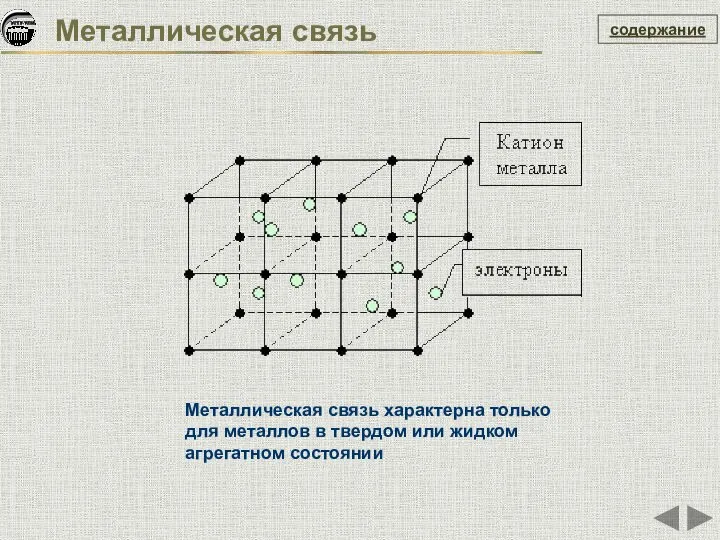
- 20. содержание Металлическая связь Металлическая связь характерна только для металлов в твердом или жидком агрегатном состоянии
- 21. содержание Основные типы кристаллических решеток металлов а) гранецентрированная кубическая (ГЦК); б) объемноцентрированная кубическая (ОЦК); в) гексагональная
- 30. содержание Химические свойства металлов По своим химическим свойствам все металлы являются восстановителями Взаимодействие с простыми веществами
- 31. содержание Электрохимический ряд напряжений металлов Li, K, Ca, Na, Mg, Al, Zn, Cr, Fe, Pb, H2,
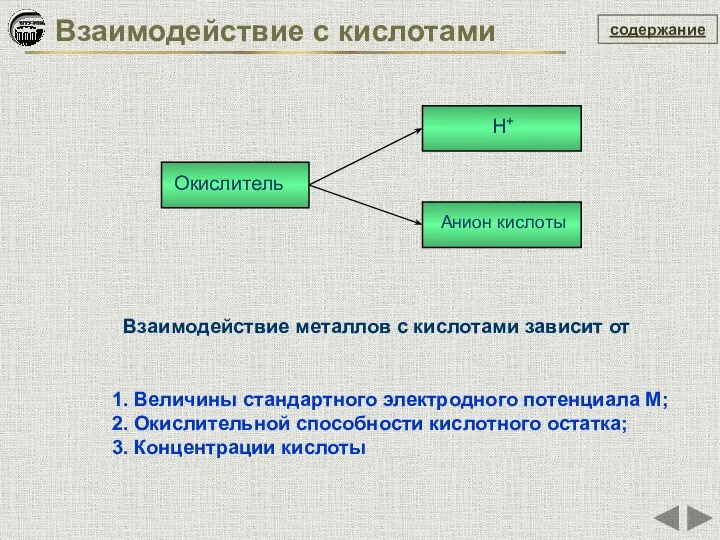
- 34. Взаимодействие с кислотами содержание Окислитель Н+ Анион кислоты 1. Величины стандартного электродного потенциала М; 2. Окислительной
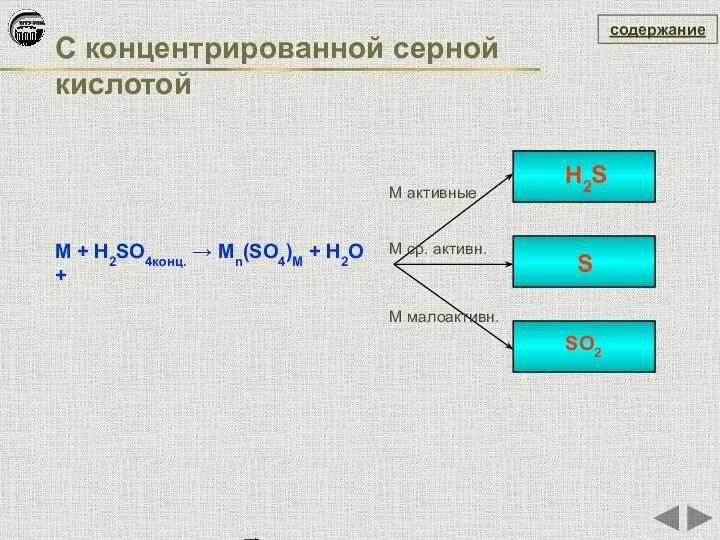
- 36. содержание С концентрированной серной кислотой М + H2SO4конц. → Мn(SO4)M + H2O + SO2 S H2S
- 39. содержание С концентрированной азотной кислотой М + HNO3конц. → М(NO3)M + H2O + NO2 3Re +
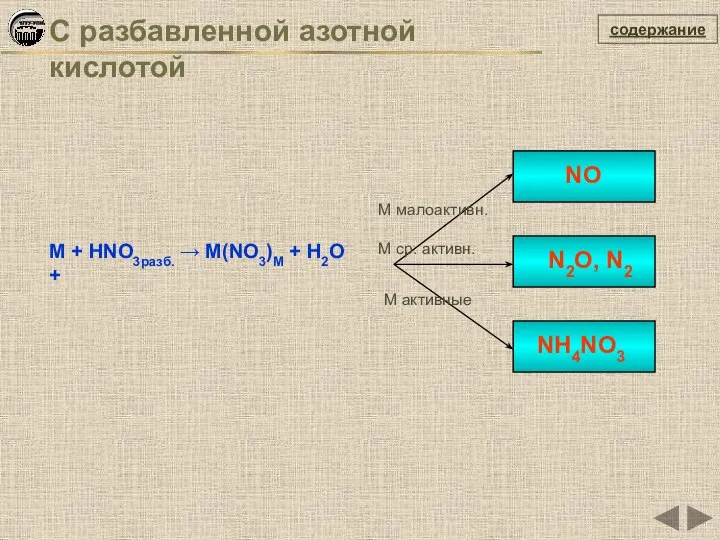
- 40. содержание С разбавленной азотной кислотой М + HNO3разб. → М(NO3)M + H2O + NO N2O, N2
- 43. содержание Взаимодействие с водой M + H2O → M(OH)n + H2 Явление глубокого торможения окисления металла,
- 44. содержание Взаимодействие с водными растворами щелочей при pH = 14 в растворах щелочей растворяются металлы, потенциалы
- 49. Скачать презентацию







































 Химический диктант как метод формирующего оценивания
Химический диктант как метод формирующего оценивания Типы кристаллических решеток. Вещества молекулярного и немолекулярного строения
Типы кристаллических решеток. Вещества молекулярного и немолекулярного строения Природный газ
Природный газ Химия биогенных элементов p -блока
Химия биогенных элементов p -блока Промышленные аварии с выбросом опасных химических веществ
Промышленные аварии с выбросом опасных химических веществ Химиялык байланыстар
Химиялык байланыстар Непредельные углеводороды. (Лекция 6)
Непредельные углеводороды. (Лекция 6) Зеленая химия и проблемы устойчивого развития Член-корреспондент РАН Н.П.Тарасова РХТУ им.Д.И.Менделеева Институт химии и про
Зеленая химия и проблемы устойчивого развития Член-корреспондент РАН Н.П.Тарасова РХТУ им.Д.И.Менделеева Институт химии и про Природный и синтетический каучуки
Природный и синтетический каучуки Физические и физико-химические свойства и характеристики грунтов. (Лекция 2)
Физические и физико-химические свойства и характеристики грунтов. (Лекция 2) Получение гидроксида никеля (II)
Получение гидроксида никеля (II) Процессы коксования
Процессы коксования Проектная деятельность школьников в процессе обучения химии
Проектная деятельность школьников в процессе обучения химии Оксиды
Оксиды Високомолекулярні сполуки. Полімери
Високомолекулярні сполуки. Полімери Основы теории сплавов. Типы сплавов. Диаграммы состояния сплавов, принцип их построения. (Лекция 2)
Основы теории сплавов. Типы сплавов. Диаграммы состояния сплавов, принцип их построения. (Лекция 2) Резеңке. Каучук
Резеңке. Каучук Мұнайдың құрамындағы тұз мөлшерін анықтау
Мұнайдың құрамындағы тұз мөлшерін анықтау Кислород, его общая характеристика и свойства
Кислород, его общая характеристика и свойства Растворы
Растворы Экстракция
Экстракция Хлорид калия KCI
Хлорид калия KCI Галогены
Галогены Предмет химии. Основные задачи курса
Предмет химии. Основные задачи курса Металлы. Классификация металлов
Металлы. Классификация металлов Презентация по Химии "КРИСТАЛЛИЧЕСКАЯ СЕРА" - скачать смотреть
Презентация по Химии "КРИСТАЛЛИЧЕСКАЯ СЕРА" - скачать смотреть  Судың құрамы және физикалық қасиеттері
Судың құрамы және физикалық қасиеттері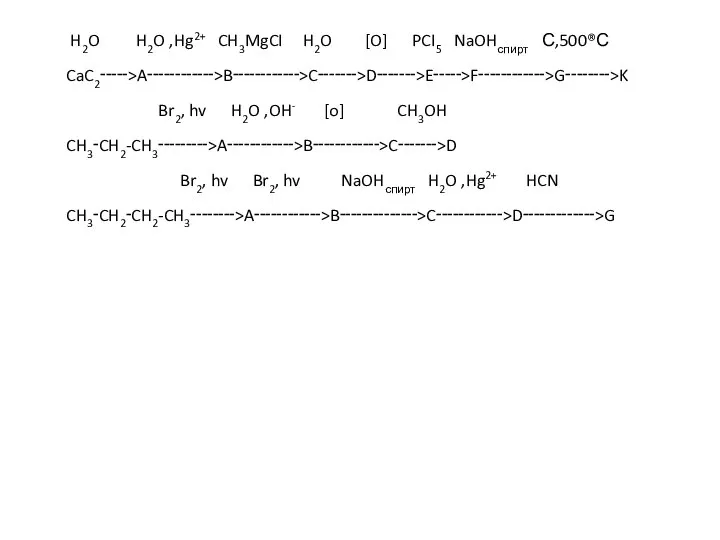 H2O, Hg2+ CH3MgCI
H2O, Hg2+ CH3MgCI