Содержание
- 2. СЛОВО «АТОМ» ПРИДУМАЛ БОЛЕЕ 2500 ЛЕТ НАЗАД ДРЕВНЕГРЕЧЕСКИЙ ФИЛОСОФ ДЕМОКРИТ АТОМ – ЭТО МЕЛЬЧАЙШАЯ ХИМИЧЕСКИ НЕДЕЛИМАЯ
- 3. Развитие представлений о строении атома Открытие рентгеновских лучей (1895 г., К. Рентген) Открытие катодных лучей (1897
- 4. Модель атома У.Томсона Уильям Томсон представляет атом как некую положительно заряженную субстанцию, в которую вкраплены электроны,
- 5. Модель атома Дж.Томсона Джозеф Джон Томсон представил свою модель строения атома в 1904 году. Он представляет
- 6. Модель атома Ленарда Ленард предложил свою модель строения атома в 1904 году. Он считает, что атом
- 7. Модель атома Нагаока Хантаро Нагаока предложил свою модель строения атома в 1904 году. Он считал, что
- 8. Опыт Резерфорда Ганс Вильгельм Гейгер Эрнест Марсден Эрнест Резерфорд
- 9. Квантовая модель Бора Постулаты Бора Электроны находятся на определенных стационарных орбитах, двигаясь по которым они не
- 10. Современная квантовая модель Н. Бор - создатель первой квантовой теории атома и активный участник разработки основ
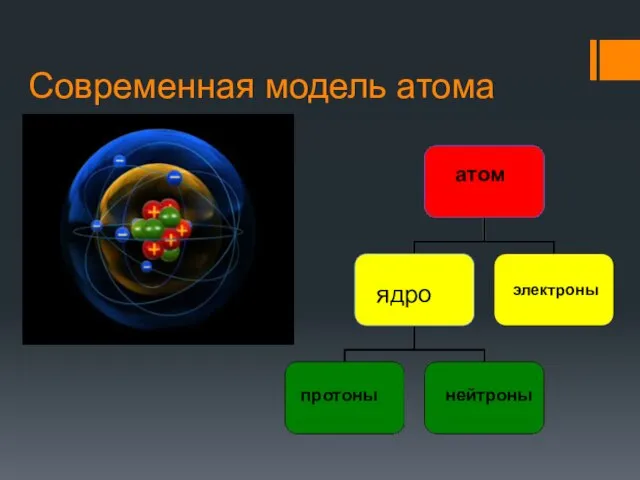
- 11. Современная модель атома ядро атом электроны нейтроны протоны
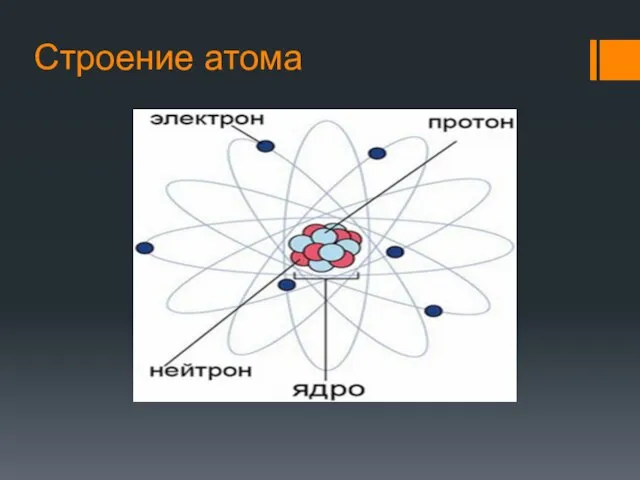
- 12. Строение атома
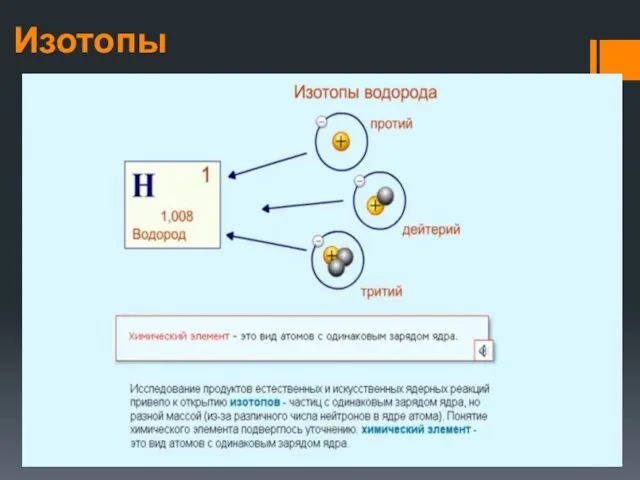
- 15. Изотопы
- 17. Электронная оболочка атома – совокупность всех электронов в атоме (число электронов в атоме равно числу протонов,
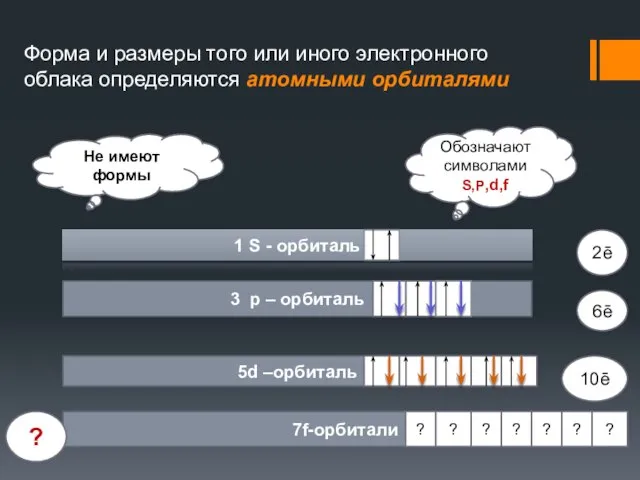
- 18. Формы электронных орбиталей S- облака (сферической формы) Р – облака (гантелеобразной формы) d – облака f
- 19. Форма и размеры того или иного электронного облака определяются атомными орбиталями Не имеют формы Обозначают символами
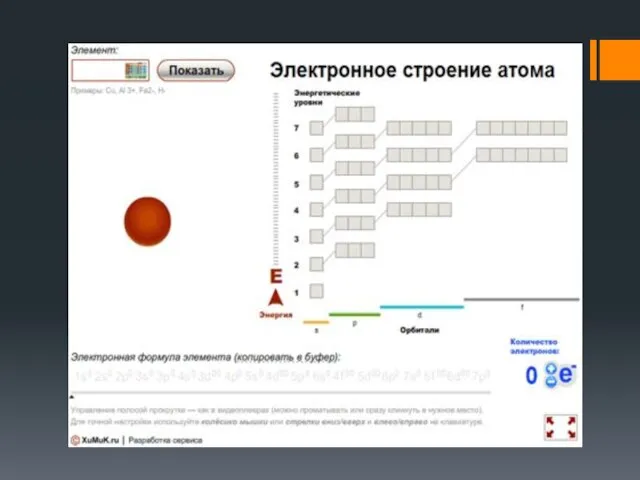
- 20. Электронные конфигурации атомов
- 23. Периодический закон и периодическая система элементов «Главный интерес химии – в изучении основных качеств элементов. Найти
- 24. Давайте вспомним, как же все свершилось, Каков был путь открытия и как Идея новая в науке
- 25. Предпосылки создания ПСХЭ Первые попытки систематизации химических элементов относятся к концу XVIII в., когда основываясь на
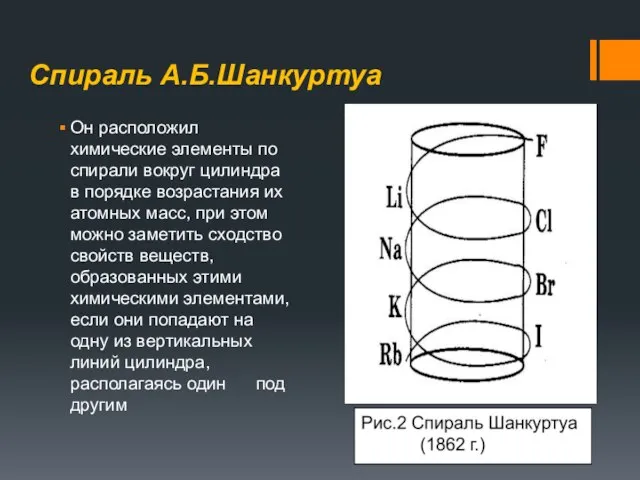
- 26. Спираль А.Б.Шанкуртуа Он расположил химические элементы по спирали вокруг цилиндра в порядке возрастания их атомных масс,
- 27. Американский химик Д.А.Р.Ньюлендс предложил свою классификацию, которую назвали законом октав. Если сходные химические элементы расположить друг
- 28. Немецкий ученый Ю.Л.Мейер расположил элементы в порядке возрастания их атомных масс с учетом их валентности по
- 29. Открытия Д.И.Менделеева Первый вариант таблицы элементов был закончен Менделеевым 17 февраля 1869 года по новому стилю,
- 30. «Опыт системы элементов, основанной на их атомном весе и химическом сходстве» (1 марта 1869 г.) Д.
- 31. И отметил в нём отрезки- периоды, в которых свойства элементов и образованных ими веществ изменяются сходным
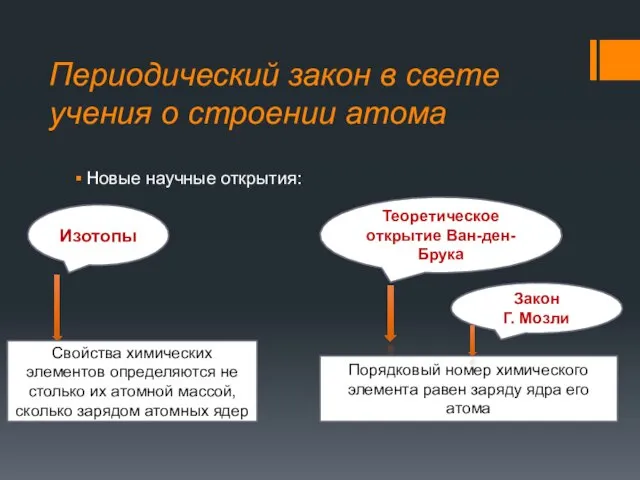
- 32. Периодический закон в свете учения о строении атома Новые научные открытия: Изотопы Теоретическое открытие Ван-ден-Брука Свойства
- 33. Периодический закон (современная формулировка) Свойства элементов, а также строение и свойства их соединений находятся в периодической
- 34. Вывод При построении периодической системы элементов Менделеев преодолел большие трудности, т. к. многие элементы ещё не
- 35. Практическое значение Периодической системы За всю историю П.С.Х.Э. было предложено большое количество (нескольких сотен) вариантов её
- 37. лестничная
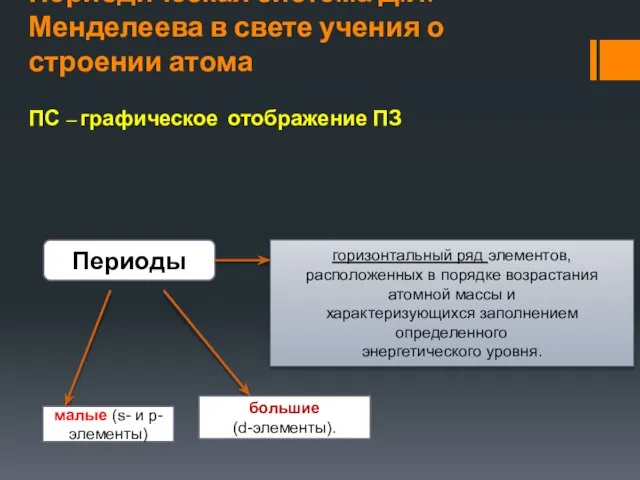
- 38. Периодическая система Д.И.Менделеева в свете учения о строении атома ПС – графическое отображение ПЗ Периоды горизонтальный
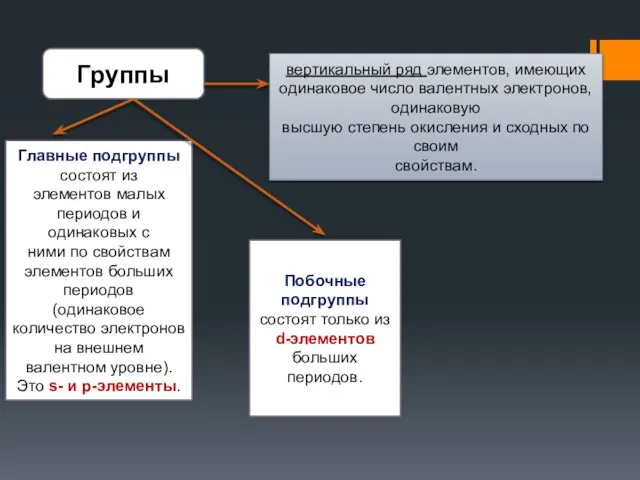
- 39. Группы вертикальный ряд элементов, имеющих одинаковое число валентных электронов, одинаковую высшую степень окисления и сходных по
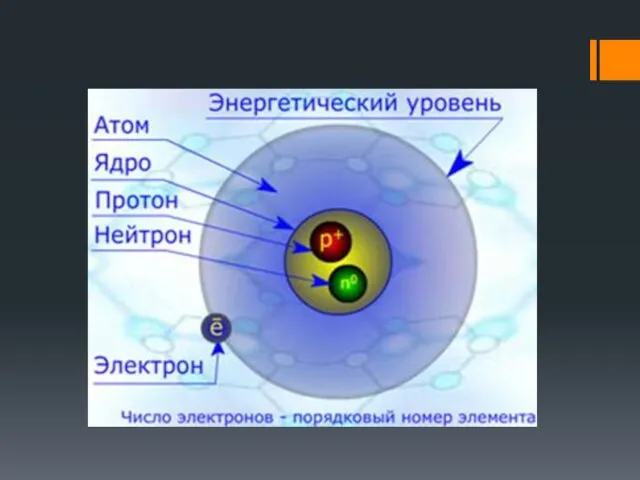
- 40. Порядковый номер элемента соответствует заряду атомного ядра, т.е. числу протонов и числу электронов в электронной оболочке
- 41. Закономерности элементов Строение атома элемента. (с ростом его порядкового номера) В пределах периода Увеличиваются заряды атомных
- 42. В пределах одной группы (главной подгруппы) Увеличиваются заряды атомных ядер элементов Число электронов на внешнем энергетическом
- 44. Скачать презентацию






























 Галогенидные и полигалогенидные комплексы висмута и теллура: синтез и физико-химические свойства
Галогенидные и полигалогенидные комплексы висмута и теллура: синтез и физико-химические свойства Обобщающий урок по теме «Неметаллы» 9 класс
Обобщающий урок по теме «Неметаллы» 9 класс Актиноиды и их применение
Актиноиды и их применение Минеральные вяжущие вещества и их назначение в строительстве. Классификация и номенклатура вяжущих веществ
Минеральные вяжущие вещества и их назначение в строительстве. Классификация и номенклатура вяжущих веществ Агрегатные состояния вещества
Агрегатные состояния вещества Химия элементов VA группы
Химия элементов VA группы Презентация по Химии "Атомы, молекулы, химические элементы. Формы существования элементов в природе" - скачать смотреть
Презентация по Химии "Атомы, молекулы, химические элементы. Формы существования элементов в природе" - скачать смотреть  Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды
Силикаты (класс). Подкласс филлосиликаты (слоистые/листовые силикаты). Семейство слюды Кислоты. Химические свойства
Кислоты. Химические свойства ХИМИЧЕСКИЕ ВЕЩЕСТВА И ОПАСНЫЕ ОБЪЕКТЫ.
ХИМИЧЕСКИЕ ВЕЩЕСТВА И ОПАСНЫЕ ОБЪЕКТЫ. Экстрагирование в химической промышленности
Экстрагирование в химической промышленности Аминокислоты – структурные единицы белков
Аминокислоты – структурные единицы белков Химияны оқыту әдістері
Химияны оқыту әдістері Получение и применение порфиринов и их аналогов
Получение и применение порфиринов и их аналогов Полезные геологические химические соединения. Получение меди из малахита
Полезные геологические химические соединения. Получение меди из малахита Явление изоморфизма в геохимии
Явление изоморфизма в геохимии Значення хімічних процесів у природі
Значення хімічних процесів у природі Презентация по Химии "Закон сохранения массы вещества" - скачать смотреть
Презентация по Химии "Закон сохранения массы вещества" - скачать смотреть  Трансляция. Биосинтез белка. (Лекция 8)
Трансляция. Биосинтез белка. (Лекция 8) Решение задач Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.
Решение задач Презентацию составила учитель МОУ «Ягринская гимназия» г.Северодвинска Шапошникова Т.С.  Флавоноидтар
Флавоноидтар Химическая связь. Электроотрицательность. Ковалентная связь
Химическая связь. Электроотрицательность. Ковалентная связь Фізичні та хімічні властивості води
Фізичні та хімічні властивості води Химические свойства алканов
Химические свойства алканов Массообменные процессы
Массообменные процессы Значення хімічних процесів у природі Виконала учениця 9-А класу, Велітченко Юлія
Значення хімічних процесів у природі Виконала учениця 9-А класу, Велітченко Юлія  Растворы. Способы выражения концентрации растворенного вещества
Растворы. Способы выражения концентрации растворенного вещества Презентация по Химии "Оксиды углерода" - скачать смотреть
Презентация по Химии "Оксиды углерода" - скачать смотреть